Trombin
Trombin (EC 3.4.21.5, fibrinogenaza, trombaza, trombofort, trombin-C, tropostazin, aktivirani faktor zgrušavanja krvi II, faktor zgrušavanja krvi IIa, faktor IIa, E-trombin, beta-trombin, gama-trombin) jest serin-proteaza, enzim koji je kod ljudi kodiran genom F2 sa hromosoma 11.[5][6] Protrombin (faktor zgrušavanja II) se proteolitski cijepa kako bi se formirao trombin u proces zgrušavanja. Trombin zauzvrat djeluje kao serinska proteaza koja pretvara rastvorljivi fibrinogen u netopive niti fibrina, katalizirajući i mnoge druge reakcije povezane sa koagulacijom.
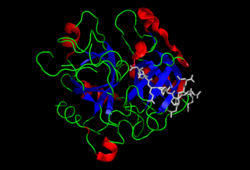
Struktura
urediMolekulska težina protrombina je približno 72.000 Da. Katalitski domen se oslobađa iz protrombinskog fragmenta 1.2, kako bi se stvorio aktivni enzim trombin, koji ima molekulsku težinu od 36.000 Da. Strukturno, član je velikog PA-klana proteaza.
Protrombin se sastoji od četiri domena; N-terminal Gla domen, dva Kringelova domen]]a i C-terminalni tripsinu-sličan domen serin-proteaza. Faktor Xa sa faktorom V kao kofaktorom dovodi do cijepanja Gla i dva Kringleova domena (formirajući zajedno fragment nazvan fragment 1.2) i ostavlja trombin, koji se sastoji isključivo od domen serinske proteaze.[8]
Kao što je slučaj sa svim serin-proteazama, protrombin se pretvara u aktivni trombin proteolizom unutrašnje peptidne veze, izlažući novi N-terminalni Ile-NH3. Historijski model aktivacije serinskih proteaza uključuje inserciju ovog novoformiranog N-kraja teškog lanca u β-barelsko podsticanje ispravne konformacije katalitskih ostataka.[9] Za razliku od kristalnih struktura aktivnog trombina, studije masene spektrometrije razmjene vodika i deuterija pokazuju da se ovaj N-terminalni Ile-NH3 ne ubacuje u β-barel u apo obliku trombina. Međutim, čini se da vezivanje aktivnog fragmenta trombomodulina alosterno promoviše aktivnu konformaciju trombina insercijom ovog N-terminalnog regiona.[10]
Gen
urediGen za trombin (protrombin) nalazi se na hromosomu 11, regija p11-q12.[5]
Procjenjuje se da u svijetu postoji oko 30 ljudi kojima je dijagnosticiran urođeni oblik nedostatka faktora II,[11] koji ne treba brkati sa mutacijom protrombin G20210A, koja se također naziva mutacijom faktora II. Prothrombin G20210A je urođen.[12]
Protrombin G20210A obično nije praćen drugim mutacijama faktora (tj. najčešći je faktora V Leiden). Gen može biti naslijeđen heterozigotno (1 par), ili mnogo rjeđe, homozigotno (2 para), i nije povezan sa spolom ili krvnom grupom. Homozigotne mutacije povećavaju rizik od tromboze više od heterozigotnih mutacija, ali relativno povećan rizik nije dobro dokumentiran. Ostali potencijalni rizici za trombozu, kao što su oralni kontraceptivi mogu biti dodatni. Prethodno prijavljeni odnos upalne bolesti crijeva (tj. Crohnova bolest ili ulcerozni kolitis) i mutacije protrombina G20210A ili faktor V Leidenove mutacije je suprotstavljen istraživanjima.[13]
Aminokiselinska sekvenca
urediDužina polipeptidnog lanca je 622 aminokiseline, a molekulska težina 70.037 Da.
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MAHVRGLQLP | GCLALAALCS | LVHSQHVFLA | PQQARSLLQR | VRRANTFLEE | ||||
| VRKGNLEREC | VEETCSYEEA | FEALESSTAT | DVFWAKYTAC | ETARTPRDKL | ||||
| AACLEGNCAE | GLGTNYRGHV | NITRSGIECQ | LWRSRYPHKP | EINSTTHPGA | ||||
| DLQENFCRNP | DSSTTGPWCY | TTDPTVRRQE | CSIPVCGQDQ | VTVAMTPRSE | ||||
| GSSVNLSPPL | EQCVPDRGQQ | YQGRLAVTTH | GLPCLAWASA | QAKALSKHQD | ||||
| FNSAVQLVEN | FCRNPDGDEE | GVWCYVAGKP | GDFGYCDLNY | CEEAVEEETG | ||||
| DGLDEDSDRA | IEGRTATSEY | QTFFNPRTFG | SGEADCGLRP | LFEKKSLEDK | ||||
| TERELLESYI | DGRIVEGSDA | EIGMSPWQVM | LFRKSPQELL | CGASLISDRW | ||||
| VLTAAHCLLY | PPWDKNFTEN | DLLVRIGKHS | RTRYERNIEK | ISMLEKIYIH | ||||
| PRYNWRENLD | RDIALMKLKK | PVAFSDYIHP | VCLPDRETAA | SLLQAGYKGR | ||||
| VTGWGNLKET | WTANVGKGQP | SVLQVVNLPI | VERPVCKDST | RIRITDNMFC | ||||
| AGYKPDEGKR | GDACEGDSGG | PFVMKSPFNN | RWYQMGIVSW | GEGCDRDGKY | ||||
| GFYTHVFRLK | KWIQKVIDQF | GE |
Sinteza
urediTrombin se proizvodi enzimskim cijepanjem dva mjesta na protrombinu aktiviranim faktorom X (Xa). Aktivnost faktora Xa je znatno poboljšana vezivanjem za aktivirani faktor V (Va), nazvan protrobinazni kompleks. Protrombin se proizvodi u jetri i kotranslacijski modificira u reakciji ovisnoj o vitaminu K koja pretvara 10-12 glutaminskih kiselina na N-kraju molekule u gama-karboksiglutaminsku kiselinu (Gla).[14] U prisustvu kalcija, Gla ostaci pospešuju vezivanje protrombina za fosfolipidne dvoslojeve. Nedostatak vitamina K ili primjena antikoagulansa varfarina inhibira proizvodnju ostataka gama-karboksiglutaminske kiseline, usporavajući aktivaciju koagulacijske kaskade.
Kod odraslih ljudi, normalan nivo aktivnosti antitrombina u krvi je izmjeren na oko 1,1 jedinica/mL. Nivo trombina u novorođenčadi se stalno povećava nakon rođenja, kako bi dostigao normalne nivoe kod odraslih, od nivoa od oko 0,5 jedinica/ml 1 dan nakon rođenja, do nivoa od oko 0,9 jedinica/ml nakon 6 mjeseci života.[15]
Klinički značaj
urediAktivacija protrombina je ključna u fiziološkoj i patološkoj koagulaciji. Opisane su različite rijetke bolesti koje uključuju protrombin (npr. hipoprotrombinemija). Antiprotrombinska antitela u autoimunskoj bolesti može biti faktor u formiranju lupus-antikoagulansa (također poznatog kao antifosfolipidni sindrom). Hiperprotrombinemija može biti uzrokovana mutacijom G20210A.
Trombin, snažan vazokonstriktor i mitogen, uključeni su kao glavni faktori u vazospazamu nakon subarahnoidalnog krvarenja. Krv iz rupture moždane aneurizme zgrušava se oko cerebralnih arterija, oslobađajući trombin. Ovo može izazvati akutno i produženo sužavanje krvnog suda, što može dovesti do cerebralne ishemije i infarkta (moždani udar).
Osim ključne uloge u dinamičkom procesu stvaranja tromba, trombin ima izražen proupalni karakter, koji može uticati na nastanak i napredovanje ateroskleroze. Djelujući preko svojih specifičnih receptora na ćelijskoj membrani (receptora aktiviranih proteazom: PAR-1, PAR-3 i PAR-4), koji su obilno eksprimirani u svim sastojcima zidova arterijskih sudova , trombin ima potencijal da ispoljava proaterogeno djelovanje kao što su upala, regrutacija leukocita u aterosklerotski plak, pojačani oksidativni stres, migracija i proliferacija vaskularnih glatkih mišićnih ćelija, apoptoza i angiogeneza.[16][17][18]
Trombin je uključen u fiziologiju krvnih ugruška. Njegovo prisustvo ukazuje na postojanje ugruška. U 2013. godini razvijen je sistem za detekciju prisustva trombina kod miševa. Kombinira peptidom obložen gvožđe-oksid povezan sa "reporterskim hemikalijama". Kada se peptid veže za molekulu trombina, oslobađa se reporter i pojavljuje u urinu, gdje se može otkriti. Testiranje na ljudima nije sprovedeno.[19]
Također pogledajte
urediReference
uredi- ^ a b c GRCh38: Ensembl release 89: ENSG00000180210 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000027249 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b Royle NJ, Irwin DM, Koschinsky ML, MacGillivray RT, Hamerton JL (maj 1987). "Human genes encoding prothrombin and ceruloplasmin map to 11p11-q12 and 3q21-24, respectively". Somatic Cell and Molecular Genetics. 13 (3): 285–92. doi:10.1007/BF01535211. PMID 3474786. S2CID 45686258.
- ^ Degen SJ, Davie EW (septembar 1987). "Nucleotide sequence of the gene for human prothrombin". Biochemistry. 26 (19): 6165–77. doi:10.1021/bi00393a033. PMID 2825773.
- ^ PDB 1nl2; Huang M, Rigby AC, Morelli X, Grant MA, Huang G, Furie B, Seaton B, Furie BC (septembar 2003). "Structural basis of membrane binding by Gla domains of vitamin K-dependent proteins". Nature Structural Biology. 10 (9): 751–6. doi:10.1038/nsb971. PMID 12923575. S2CID 7751100.
- ^ Davie EW, Kulman JD (april 2006). "An overview of the structure and function of thrombin". Seminars in Thrombosis and Hemostasis. 32 Suppl 1: 3–15. doi:10.1055/s-2006-939550. PMID 16673262.
- ^ Huber R, Bode W (1. 3. 1978). "Structural basis of the activation and action of trypsin". Accounts of Chemical Research. 11 (3): 114–122. doi:10.1021/ar50123a006. ISSN 0001-4842.
- ^ Handley LD, Treuheit NA, Venkatesh VJ, Komives EA (novembar 2015). "Thrombomodulin Binding Selects the Catalytically Active Form of Thrombin". Biochemistry. 54 (43): 6650–8. doi:10.1021/acs.biochem.5b00825. PMC 4697735. PMID 26468766.
- ^ Degen SJ, McDowell SA, Sparks LM, Scharrer I (februar 1995). "Prothrombin Frankfurt: a dysfunctional prothrombin characterized by substitution of Glu-466 by Ala". Thrombosis and Haemostasis. 73 (2): 203–9. doi:10.1055/s-0038-1653751. PMID 7792730.
- ^ Varga EA, Moll S (juli 2004). "Cardiology patient pages. Prothrombin 20210 mutation (factor II mutation)". Circulation. 110 (3): e15–8. doi:10.1161/01.CIR.0000135582.53444.87. PMID 15262854.
- ^ Bernstein CN, Sargent M, Vos HL, Rosendaal FR (februar 2007). "Mutations in clotting factors and inflammatory bowel disease". The American Journal of Gastroenterology. 102 (2): 338–43. doi:10.1111/j.1572-0241.2006.00974.x. PMID 17156138. S2CID 19895315.
- ^ Knorre DG, Kudryashova NV, Godovikova TS (oktobar 2009). "Chemical and functional aspects of posttranslational modification of proteins". Acta Naturae. 1 (3): 29–51. doi:10.32607/20758251-2009-1-3-29-51. PMC 3347534. PMID 22649613.
- ^ Andrew M, Paes B, Milner R, Johnston M, Mitchell L, Tollefsen DM, Powers P (juli 1987). "Development of the human coagulation system in the full-term infant". Blood. 70 (1): 165–72. doi:10.1182/blood.V70.1.165.165. PMID 3593964.
- ^ Borissoff JI, Spronk HM, Heeneman S, ten Cate H (juni 2009). "Is thrombin a key player in the 'coagulation-atherogenesis' maze?". Cardiovascular Research. 82 (3): 392–403. doi:10.1093/cvr/cvp066. PMID 19228706.
- ^ Borissoff JI, Heeneman S, Kilinç E, Kassák P, Van Oerle R, Winckers K, Govers-Riemslag JW, Hamulyák K, Hackeng TM, Daemen MJ, ten Cate H, Spronk HM (august 2010). "Early atherosclerosis exhibits an enhanced procoagulant state". Circulation. 122 (8): 821–30. doi:10.1161/CIRCULATIONAHA.109.907121. PMID 20697022.
- ^ Borissoff JI, Spronk HM, ten Cate H (maj 2011). "The hemostatic system as a modulator of atherosclerosis". The New England Journal of Medicine. 364 (18): 1746–60. doi:10.1056/NEJMra1011670. PMID 21542745.
- ^ Economist (5. 11. 2013). "Nanomedicine: Particle physiology". The Economist. Pristupljeno 15. 12. 2013.
Dopunska literatura
uredi- Esmon CT (juli 1995). "Thrombomodulin as a model of molecular mechanisms that modulate protease specificity and function at the vessel surface". FASEB Journal. 9 (10): 946–55. doi:10.1096/fasebj.9.10.7615164. PMID 7615164. S2CID 19565674.
- Wu H, Zhang Z, Li Y, Zhao R, Li H, Song Y, Qi J, Wang J (oktobar 2010). "Time course of upregulation of inflammatory mediators in the hemorrhagic brain in rats: correlation with brain edema". Neurochemistry International. 57 (3): 248–53. doi:10.1016/j.neuint.2010.06.002. PMC 2910823. PMID 20541575.
- Lenting PJ, van Mourik JA, Mertens K (decembar 1998). "The life cycle of coagulation factor VIII in view of its structure and function". Blood. 92 (11): 3983–96. doi:10.1182/blood.V92.11.3983. PMID 9834200.
- Plow EF, Cierniewski CS, Xiao Z, Haas TA, Byzova TV (juli 2001). "AlphaIIbbeta3 and its antagonism at the new millennium". Thrombosis and Haemostasis. 86 (1): 34–40. doi:10.1055/s-0037-1616198. PMID 11487023.
- Maragoudakis ME, Tsopanoglou NE, Andriopoulou P (april 2002). "Mechanism of thrombin-induced angiogenesis". Biochemical Society Transactions. 30 (2): 173–7. doi:10.1042/BST0300173. PMID 12023846.
- Howell DC, Laurent GJ, Chambers RC (april 2002). "Role of thrombin and its major cellular receptor, protease-activated receptor-1, in pulmonary fibrosis". Biochemical Society Transactions. 30 (2): 211–6. doi:10.1042/BST0300211. PMID 12023853. S2CID 32822567.
- Firth SM, Baxter RC (decembar 2002). "Cellular actions of the insulin-like growth factor binding proteins". Endocrine Reviews. 23 (6): 824–54. doi:10.1210/er.2001-0033. PMID 12466191.
- Minami T, Sugiyama A, Wu SQ, Abid R, Kodama T, Aird WC (januar 2004). "Thrombin and phenotypic modulation of the endothelium". Arteriosclerosis, Thrombosis, and Vascular Biology. 24 (1): 41–53. doi:10.1161/01.ATV.0000099880.09014.7D. PMID 14551154.
- De Cristofaro R, De Candia E (juni 2003). "Thrombin domains: structure, function and interaction with platelet receptors". Journal of Thrombosis and Thrombolysis. 15 (3): 151–63. doi:10.1023/B:THRO.0000011370.80989.7b. PMID 14739624.
- Tsopanoglou NE, Maragoudakis ME (februar 2004). "Role of thrombin in angiogenesis and tumor progression". Seminars in Thrombosis and Hemostasis. 30 (1): 63–9. doi:10.1055/s-2004-822971. PMID 15034798.
- Bode W (2007). "Structure and interaction modes of thrombin". Blood Cells, Molecules & Diseases. 36 (2): 122–30. doi:10.1016/j.bcmd.2005.12.027. PMID 16480903.
- Wolberg AS (maj 2007). "Thrombin generation and fibrin clot structure". Blood Reviews. 21 (3): 131–42. doi:10.1016/j.blre.2006.11.001. PMID 17208341.
- Degen S (1995). "Prothrombin". u High K, Roberts H (ured.). Molecular Basis of Thrombosis and Hemostasis. Marcel Dekker. str. 75. ISBN 9780824795016.
Vanjski linkovi
uredi- The MEROPS online database for peptidases and their inhibitors: S01.217 Arhivirano 19. 9. 2019. na Wayback Machine
- Kujovich JL (februar 2021). Adam MP, Ardinger HH, Pagon RA, et al. (ured.). "Prothrombin Thrombophilia". GeneReviews. Seattle WA: University of Washington, Seattle. PMID 20301327. NBK1148.
- Anti-coagulation & proteases na YouTubeu by The Proteolysis Map-animation
- [1] PMAP: The Proteolysis Map/Thrombin
- Thrombin: RCSB PDB Molecule of the Month Arhivirano 5. 10. 2013. na Wayback Machine
- Prothrombin Structure
- PDBe-KB provides an overview of all the structure information available in the PDB for Human Thrombin.
- PDBe-KB provides an overview of all the structure information available in the PDB for Mouse Thrombin.