BRCA2
BRCA2[5]) je ljudski gen, odnosno njegov proteinski proizvod. Službeni simbol (BRCA2, kurziv za gen, neitalik za protein) i službeni naziv (izvorno rak dojke 2, sada BRCA2 vezana popravka DNK) su podržane u HUGO Odboru za gensku nomenklaturu. Jedan alternativni simbol, FANCD1, prepoznaje njegovu povezanost sa kompleksom FANC proteina. Ortolozi, oblikovani kao Brca2 i Brca2, česti su i kod drugih kičmenjačnih vrsta.[6][7] BRCA2 ie tumor-supresorski gen[8][9] (posebno, domćinski gen), koji se nalazi u svih ljudi; njegov protein, koji se sinonimno naziva i protein osjetljiv na rak dojke tipa 2, odgovoran je za popravak DNK.[10]
| Ponavljanje BRCA2 | |
|---|---|
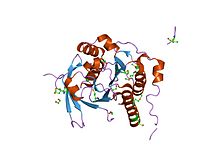 Kristalna struktura ponavlajajućeg kompleksa rad51-brca2 | |
| Identifikatori | |
| Simbol | BRCA2 |
| BRCA-2 heliks | |
|---|---|
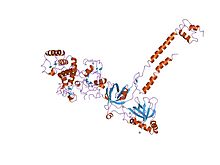 Struktura kompleksa brca2-dss1 | |
| Identifikatori | |
| Simbol | BRCA-2_helical |
| BRCA2, oligonukleotid/oligosaharid-vezujući domen 1 | |
|---|---|
 Struktura kompleksa brca2-dss1 | |
| Identifikatori | |
| Simbol | BRCA-2_OB1 |
| BRCA2, oligonuKleotid/oligosaharid-vezujući domen 3 | |
|---|---|
 Struktura kompleksa brca2-dss1 | |
| Identifikatori | |
| Simbol | BRCA-2_OB3 |
| Domrn Tower | |
|---|---|
 Struktura kompleksa brca2-dss1 | |
| Identifikatori | |
| Simbol | Tower |
BRCA2 i BRCA1 se normalno eksprimiraju u ćelijamama dojke i drugog tkiva, gdje pomažu u obnavljanju oštećene DNK ili uništavanju ćelija ako se DNK ne može popraviti. Uključeni su u popravak oštećenja hromosoma, s važnom ulogom u popravakama greašaka u formiranju dvostrukih lanaca.[11][12] Ako je sam BRCA1 ili BRCA2 oštećen BRCA mutacijama, oštećena DNK se ne popravlja ispravno, a to povećava rizik od raka dojke.[13][14] BRCA1 i BRCA2 opisani su kao "geni osjetljivosti na rak dojke" i "proteini osjetljivosti na rak dojke". Prevladavajući alel ima normalnu tumor-supresivnu funkciju, dok visoko penetrirane mutacije u tim genima uzrokuju gubitak tumorske supresivne funkcije, što je u korelaciji s povećanim rizikom od raka dojke.[15]
Gen BRCA2 nalazi se na dugom (q) kraku hromosoma 13, na poziciji 12.3 (13q12.3).[16] Ljudski referentni gen BRCA2 sadrži 27 egzona, a and the cDNK ima 10.254 baznih parova[17] za kodiranje proteina od 3.418 aminokiselina.[18][19] Karcinom dojke (uključujući i muški): Međuodnosi fenotip – genotip[20][21][22]
Aminokiselinska sekvenca
urediDužina polipeptidnog lanca je 3.418 aminokiselina, a molekulska težina 384.202 Da.[23]
- Simboli
C: Cistein
D: Asparaginska kiselina
E: Glutaminska kiselina
F: Fenilalanin
G: Glicin
H: Histidin
I: Izoleucin
K: Lizin
L: Leucin
M: Metionin
N: Asparagin
P: Prolin
Q: Glutamin
R: Arginin
S: Serin
T: Treonin
V: Valin
W: Triptofan
Y: Tirozin
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MPIGSKERPT | FFEIFKTRCN | KADLGPISLN | WFEELSSEAP | PYNSEPAEES | ||||
| EHKNNNYEPN | LFKTPQRKPS | YNQLASTPII | FKEQGLTLPL | YQSPVKELDK | ||||
| FKLDLGRNVP | NSRHKSLRTV | KTKMDQADDV | SCPLLNSCLS | ESPVVLQCTH | ||||
| VTPQRDKSVV | CGSLFHTPKF | VKGRQTPKHI | SESLGAEVDP | DMSWSSSLAT | ||||
| PPTLSSTVLI | VRNEEASETV | FPHDTTANVK | SYFSNHDESL | KKNDRFIASV | ||||
| TDSENTNQRE | AASHGFGKTS | GNSFKVNSCK | DHIGKSMPNV | LEDEVYETVV | ||||
| DTSEEDSFSL | CFSKCRTKNL | QKVRTSKTRK | KIFHEANADE | CEKSKNQVKE | ||||
| KYSFVSEVEP | NDTDPLDSNV | ANQKPFESGS | DKISKEVVPS | LACEWSQLTL | ||||
| SGLNGAQMEK | IPLLHISSCD | QNISEKDLLD | TENKRKKDFL | TSENSLPRIS | ||||
| SLPKSEKPLN | EETVVNKRDE | EQHLESHTDC | ILAVKQAISG | TSPVASSFQG | ||||
| IKKSIFRIRE | SPKETFNASF | SGHMTDPNFK | KETEASESGL | EIHTVCSQKE | ||||
| DSLCPNLIDN | GSWPATTTQN | SVALKNAGLI | STLKKKTNKF | IYAIHDETSY | ||||
| KGKKIPKDQK | SELINCSAQF | EANAFEAPLT | FANADSGLLH | SSVKRSCSQN | ||||
| DSEEPTLSLT | SSFGTILRKC | SRNETCSNNT | VISQDLDYKE | AKCNKEKLQL | ||||
| FITPEADSLS | CLQEGQCEND | PKSKKVSDIK | EEVLAAACHP | VQHSKVEYSD | ||||
| TDFQSQKSLL | YDHENASTLI | LTPTSKDVLS | NLVMISRGKE | SYKMSDKLKG | ||||
| NNYESDVELT | KNIPMEKNQD | VCALNENYKN | VELLPPEKYM | RVASPSRKVQ | ||||
| FNQNTNLRVI | QKNQEETTSI | SKITVNPDSE | ELFSDNENNF | VFQVANERNN | ||||
| LALGNTKELH | ETDLTCVNEP | IFKNSTMVLY | GDTGDKQATQ | VSIKKDLVYV | ||||
| LAEENKNSVK | QHIKMTLGQD | LKSDISLNID | KIPEKNNDYM | NKWAGLLGPI | ||||
| SNHSFGGSFR | TASNKEIKLS | EHNIKKSKMF | FKDIEEQYPT | SLACVEIVNT | ||||
| LALDNQKKLS | KPQSINTVSA | HLQSSVVVSD | CKNSHITPQM | LFSKQDFNSN | ||||
| HNLTPSQKAE | ITELSTILEE | SGSQFEFTQF | RKPSYILQKS | TFEVPENQMT | ||||
| ILKTTSEECR | DADLHVIMNA | PSIGQVDSSK | QFEGTVEIKR | KFAGLLKNDC | ||||
| NKSASGYLTD | ENEVGFRGFY | SAHGTKLNVS | TEALQKAVKL | FSDIENISEE | ||||
| TSAEVHPISL | SSSKCHDSVV | SMFKIENHND | KTVSEKNNKC | QLILQNNIEM | ||||
| TTGTFVEEIT | ENYKRNTENE | DNKYTAASRN | SHNLEFDGSD | SSKNDTVCIH | ||||
| KDETDLLFTD | QHNICLKLSG | QFMKEGNTQI | KEDLSDLTFL | EVAKAQEACH | ||||
| GNTSNKEQLT | ATKTEQNIKD | FETSDTFFQT | ASGKNISVAK | ESFNKIVNFF | ||||
| DQKPEELHNF | SLNSELHSDI | RKNKMDILSY | EETDIVKHKI | LKESVPVGTG | ||||
| NQLVTFQGQP | ERDEKIKEPT | LLGFHTASGK | KVKIAKESLD | KVKNLFDEKE | ||||
| QGTSEITSFS | HQWAKTLKYR | EACKDLELAC | ETIEITAAPK | CKEMQNSLNN | ||||
| DKNLVSIETV | VPPKLLSDNL | CRQTENLKTS | KSIFLKVKVH | ENVEKETAKS | ||||
| PATCYTNQSP | YSVIENSALA | FYTSCSRKTS | VSQTSLLEAK | KWLREGIFDG | ||||
| QPERINTADY | VGNYLYENNS | NSTIAENDKN | HLSEKQDTYL | SNSSMSNSYS | ||||
| YHSDEVYNDS | GYLSKNKLDS | GIEPVLKNVE | DQKNTSFSKV | ISNVKDANAY | ||||
| PQTVNEDICV | EELVTSSSPC | KNKNAAIKLS | ISNSNNFEVG | PPAFRIASGK | ||||
| IVCVSHETIK | KVKDIFTDSF | SKVIKENNEN | KSKICQTKIM | AGCYEALDDS | ||||
| EDILHNSLDN | DECSTHSHKV | FADIQSEEIL | QHNQNMSGLE | KVSKISPCDV | ||||
| SLETSDICKC | SIGKLHKSVS | SANTCGIFST | ASGKSVQVSD | ASLQNARQVF | ||||
| SEIEDSTKQV | FSKVLFKSNE | HSDQLTREEN | TAIRTPEHLI | SQKGFSYNVV | ||||
| NSSAFSGFST | ASGKQVSILE | SSLHKVKGVL | EEFDLIRTEH | SLHYSPTSRQ | ||||
| NVSKILPRVD | KRNPEHCVNS | EMEKTCSKEF | KLSNNLNVEG | GSSENNHSIK | ||||
| VSPYLSQFQQ | DKQQLVLGTK | VSLVENIHVL | GKEQASPKNV | KMEIGKTETF | ||||
| SDVPVKTNIE | VCSTYSKDSE | NYFETEAVEI | AKAFMEDDEL | TDSKLPSHAT | ||||
| HSLFTCPENE | EMVLSNSRIG | KRRGEPLILV | GEPSIKRNLL | NEFDRIIENQ | ||||
| EKSLKASKST | PDGTIKDRRL | FMHHVSLEPI | TCVPFRTTKE | RQEIQNPNFT | ||||
| APGQEFLSKS | HLYEHLTLEK | SSSNLAVSGH | PFYQVSATRN | EKMRHLITTG | ||||
| RPTKVFVPPF | KTKSHFHRVE | QCVRNINLEE | NRQKQNIDGH | GSDDSKNKIN | ||||
| DNEIHQFNKN | NSNQAAAVTF | TKCEEEPLDL | ITSLQNARDI | QDMRIKKKQR | ||||
| QRVFPQPGSL | YLAKTSTLPR | ISLKAAVGGQ | VPSACSHKQL | YTYGVSKHCI | ||||
| KINSKNAESF | QFHTEDYFGK | ESLWTGKGIQ | LADGGWLIPS | NDGKAGKEEF | ||||
| YRALCDTPGV | DPKLISRIWV | YNHYRWIIWK | LAAMECAFPK | EFANRCLSPE | ||||
| RVLLQLKYRY | DTEIDRSRRS | AIKKIMERDD | TAAKTLVLCV | SDIISLSANI | ||||
| SETSSNKTSS | ADTQKVAIIE | LTDGWYAVKA | QLDPPLLAVL | KNGRLTVGQK | ||||
| IILHGAELVG | SPDACTPLEA | PESLMLKISA | NSTRPARWYT | KLGFFPDPRP | ||||
| FPLPLSSLFS | DGGNVGCVDV | IIQRAYPIQW | MEKTSSGLYI | FRNEREEEKE | ||||
| AAKYVEAQQK | RLEALFTKIQ | EEFEEHEENT | TKPYLPSRAL | TRQQVRALQD | ||||
| GAELYEAVKN | AADPAYLEGY | FSEEQLRALN | NHRQMLNDKK | QAQIQLEIRK | ||||
| AMESAEQKEQ | GLSRDVTTVW | KLRIVSYSKK | EKDSVILSIW | RPSSDLYSLL | ||||
| TEGKRYRIYH | LATSKSKSKS | ERANIQLAAT | KKTQYQQLPV | SDEILFQIYQ | ||||
| PREPLHFSKF | LDPDFQPSCS | EVDLIGFVVS | VVKKTGLAPF | VYLSDECYNL | ||||
| LAIKFWIDLN | EDIIKPHMLI | AASNLQWRPE | SKSGLLTLFA | GDFSVFSASP | ||||
| KEGHFQETFN | KMKNTVENID | ILCNEAENKL | MHILHANDPK | WSTPTKDCTS | ||||
| GPYTAQIIPG | TGNKLLMSSP | NCEIYYQSPL | SLCMAKRKSV | STPVSAQMTS | ||||
| KSCKGEKEID | DQKNCKKRRA | LDFLSRLPLP | PPVSPICTFV | SPAAQKAFQP | ||||
| PRSCGTKYET | PIKKKELNSP | QMTPFKKFNE | ISLLESNSIA | DEELALINTQ | ||||
| ALLSGSTGEK | QFISVSESTR | TAPTSSEDYL | RLKRRCTTSL | IKEQESSQAS | ||||
| TEECEKNKQD | TITTKKYI |
Funkcija
urediIako se strukture gena BRCA1 i BRCA2 jako razlikuju, barem su neke funkcije međusobno povezane. Proteini koje proizvode oba gena neophodni su za popravak oštećene DNK (vidi sliku koraka rekombinacijske popravke). BRCA2 veže jednolančanu DNK i direktno stupa u interakciju s rekombinazom RAD51 radi stimulacije[31] i održavanja [32] invazija lanaca, što jer vitalni korak homologne rekombinacije. Lokalizacija RAD51 na prekid dvolančane DNK zahtijeva stvaranje kompleksa BRCA1-PALB2-BRCA2. PALB2 (partner i lokalizator BRCA2)[33] može djelovati sinergijski s himerom BRCA2 (zvanom piccolo ili piBRCA2) za daljnje promicanje invazije niti.[34] Ovi prekidi mogu biti uzrokovani prirodnim i medicinskim zračenjem ili drugom izloženošću okoliša, ali se također događaju kada hromosomi razmjenjuju genetički materijal tokom posebnog tipa ćelijske diobe, koja stvara spermu i jajne ćelije (mejoza). Dvolančani prekidi nastaju i tokom popravljanja unakrsnih veza DNK. Popravljajući DNK, ovi proteini imaju ulogu u održavanju stabilnosti ljudskog genoma i sprečavanju opasna preuređenja gena koji mogu dovesti do krvnih i drugih karcinoma.
Pokazalo se da BRCA2 ima ključnu ulogu u zaštiti od MRE11-ovisne nukleolitske degradacije obrnutih viljuški koje nastaju tokom zastoja replikacije DNK (uzrokovano preprekama kao što su mutacije, interkalirajući agensi itd.).[35]
Kao i BRCA1, BRCA2 vjerovatno regulira aktivnost drugih gena i igra ključnu ulogu u razvoju embrija.
Klinički značaj
urediOdređene varijacije gena BRCA2 povećavaju rizik za rak dojke, kao dio nasljednog sindroma raka dojke-jajnika. Istraživanem su identificirane stotine mutacija u genu BRCA2, od kojih mnoge uzrokuju povećan rizik od raka. BRCA2 mutacije obično su insercije ili delecije malog broja baznih parova DNK u genu. Kao rezultat ovih mutacija, proteinski proizvod gena BRCA2 je abnormalan i ne funkcionira pravilno. Vjeruje se da neispravan protein BRCA2 nije u stanju popraviti oštećenje DNK koje se događa u cijelom genomu. Kao rezultat toga, dolazi do povećanja učestalosti mutacija zbog sklonosti greškama u sintezi translezije, u prošlosti neopravljenih oštećenja DNK, a neke od ovih mutacija mogu uzrokovati nekontroliranu podjelu ćelija u obliku tumora.
Ljudi koji imaju dvije mutirane kopije gena BRCA2 imaju jedan tip Fanconijeve anemije. Ovo stanje uzrokovano je izrazito smanjenim nivoom BRCA2 proteina u stanicama, što omogućava nakupljanje oštećene DNK. Pacijenti sa Fanconijevom anemijom skloni su pojavi nekoliko tipova leukemija (tipova raka krvnih ćelija); solidni tumori, posebno glave, vrata, kože i reproduktivnih organa i supresija koštane srži (smanjena proizvodnja krvnih ćelija koja dovodi do anemija). Žene koje su naslijedile neispravan gen BRCA1 ili BRCA2 imaju rizik od raka dojke i jajnika koji je toliko visok i djeluje tako selektivno da se mnogi nositelji mutacija odluče za profilaksnu operaciju. Bilo je mnogo nagađanja za objašnjenje tako očigledno upečatljive specifičnosti tkiva. Glavne odrednice gdje se javljaju nasljedni karcinomi povezani sa BRCA1 i BRCA2 povezani su sa tkivnom specifičnošću patogena raka, uzročnika koji izaziva hroničnu upalu ili karcinogenom. Ciljano tkivo može imati receptore za patogene, postati selektivno izloženo kancerogenima i infektivnom procesu. Urođeni genomski deficit narušava normalne reakcije i pogoršava osjetljivost na bolesti na organu-meti. Ova teorija se također uklapa u podatke za nekoliko tumorskih supresora izvan BRCA1 ili BRCA2. Glavna prednost ovog modela je ta što sugerira da postoje i neke mogućnosti osim profilaksne operacije.[36]
Osim raka dojke kod muškaraca i žena, mutacije u BRCA2 također dovode do povećanog rizika od rakajajnika, jajovoda, prostate i guštrerače. U nekim studijama, mutacije u središnjem dijelu gena bile su povezane s većim rizikom od raka jajnika i manjim rizikom od raka prostate od mutacija u drugim dijelovima gena. Nekoliko drugih tipova raka također je viđeno u određenim porodicama s BRCA2 mutacijama.
Općenito, naslijeđene mutacije gena (uključujući mutacije u BRCA2) čine samo 5-10% slučajeva raka dojke; specifični rizik od dobijanja raka dojke ili drugog karcinoma za svakoga ko ima mutaciju BRCA2 ovisi o mnogim faktorima.[37]
Germinativne mutacije BRCA2 i efekt osnivača
urediSve dosad identificirane mutacije BRCA2 zametne linije naslijeđene su, što ukazuje na mogućnost velikog efekta "osnivača" u kojem je određena mutacija zajednička dobro definiranoj populacijskoj skupini i teorijski se može pratiti do zajedničkog pretka. S obzirom na složenost skrininga mutacija za BRCA2, ove uobičajene mutacije mogu pojednostaviti metode potrebne za skrining mutacija u određenim populacijama. Analiza mutacija koje se javljaju s visokom učestalošću također dopušta proučavanje njihove kliničke ekspresije.[38] Upečatljiv primjer osnivačke mutacije nalazi se na Islandu, gdje jedna BRCA2 (999del5) mutacija predstavlja gotovo sve porodice raka dojke/jajnika.[39][40] Ova mutacija pomjeranja okvira dovodi do visoko skraćenog proteinskog proizvoda. U velikoj studiji koja je ispitivala stotine karcinoma i kontrolne osobe, ova mutacija od 999del5 pronađena je u 0,6% opće populacije. Treba napomenuti da, dok je 72% pacijenata za koje je ustanovljeno da su nositelji imalo umjerenu ili jaku porodičnu istoriju raka dojke, 28% je imalo malu ili nikakvu porodičnu historiju bolesti. To snažno sugerira prisutnost modifikajijskih gena koji utiču na fenotipsku ekspresiju ove mutacije, ili možda interakciju BRCA2 mutacije s faktorima okruženja. Dodatni primjeri mutacija osnivača u BRCA2 dati su u donjoj tabeli. Šablon:Dynamic list
| Populacija ili podrgupa | BRCA2 mutacije[38][41] | Reference(s) |
|---|---|---|
| Aškenazi Jevreji | 6174delT | [42] |
| Nizozemci | 5579insA | [43] |
| Finci | 8555T>G, 999del5, IVS23-2A>G | [44][45] |
| Francuski Kanađani | 8765delAG, 3398delAAAAG | [46][47][48] |
| Mađari | 9326insA | [49] |
| Islanđani | 999del5 | [39][40] |
| Italijani | 8765delAG | [50] |
| Sjeverni Irci | 6503delTT | [51] |
| Pakistanci | 3337C>T | [52] |
| Škoti | 6503delTT | [51] |
| Slovenci | IVS16-2A>G | [53] |
| Španci | 3034delAAAC(codon936), 9254del5 | [54] |
| Šveđani | 4486delG | [55] |
Mejoza
urediU biljke Arabidopsis thaliana , gubitak BRCA2 homologa AtBRCA2 uzrokuje ozbiljne nedostatke i kod muške mejozr i u razvoju ženskih gametocita.[56] Protein AtBRCA2 potreban je za pravilnu lokalizaciju sinaptonemskog kompleksa proteina AtZYP1 i rekombinaza AtRAD51 i AtDMC1. Nadalje, AtBRCA2 je potreban za pravilnu mejotsku sinapsu. Stoga je AtBRCA2 vjerovatno važan za mejotsku rekombinaciju. Čini se da AtBRCA2 djeluje za vrijeme mejoze kako bi kontrolirao korake jednolančane invazije posredovane AtRAD51 i AtDMC1 koji se javljaju tokom mejotske homolognorekombinacijskog popravljanja oštećenja DNK.[56]
Homolozi BRCA2 takođe su bitni za mejozu u gljivice Ustilago maydis (žitna hrđa),[57] oble gliste Caenorhabditis elegans,[58][59] i vinske mšice Drosophila melanogaster.[60]
Miševi koji proizvode skraćene verzije BRCA2 su održivi, ali su sterilni.[61] :Simboli .[62] Aspermatogeneza u ovih mutiranih pacova posljedica je neuspjeha homologne hromosomske sinapse tokom mejoze.
Ponavljajuće sekvence BRC
urediDMC1 (DNK mejotska rekombinaza 1) je mejoza-specifični homolog RAD51, koji posreduje razmjenu lanaca tokom homologne rekombinacije u popravku. DMC1 promovira stvaranje proizvoda invazije lanca DNK (molekule zglobova) između homolognih molekula DNK. Ljudski DMC1 direktno stupa u interakciju sa svakim od niza ponavljajućih sekvenci u proteinu BRCA2 (zvanom BRC ponavljanja) koji stimulira stvaranje molekula zglobova pomoću DMC1.[63] BRC-ponavljanja u skladu su s motivom koji se sastoji od sekvence od oko 35 visoko konzerviranih aminokiselina koje su prisutne barem jednom u svim proteinima sličnim BRCA2. BRCA2 BRC ponavljanja stimuliraju stvaranje zglobnih molekula, podstičući interakciju jednolančane DNK (ssDNK) s DMC1.[63] ssDNK kompleksirana s DMC1 može se upariti s homolognom ssDNK iz drugog hromosoma tokom faze sinapsije u mejozi, kako bi se formirala zajednička molekula, središnji korak u homolognoj rekombinaciji. Stoga se čini da BRC ponavljajuće sekvence BRCA2 imaju ključnu ulogu u rekombinacijskom popravljanju oštećenja DNA tokom mejotske rekombinacije.
Sve u svemu, čini se da homologna rekombinacija tokom mejoze funkcionira za popravljanje oštećenja DNK i da BRCA2 ima ključnu ulogu u obavljanju ove funkcije.
Neurogeneza
urediBRCA2 je potreban miševima za neurogenezu i suzbijanje meduloblastoma.[64] Gubitak BRCA2 duboko utiče na neurogenezu, posebno tokom embrionskog i postnatalnog neuronskog razvoja. Ovi neurološki nedostaci proizlaze iz oštećenja DNK.[64]
Epigenetička kontrola
urediEpigenetičke promjene u ekspresiji BRCA2 (uzrokujući prekomjernu ili nedovoljnu ekspresiju) vrlo su česte kod sporadičnih karcinoma (vidi donju tabelu), dok se mutacije u BRCA2 rijetko nalaze.[65][66][67]
U karcinomu pluća nemalih ćelija, BRCA2 je epigenetički potisnut hipermetilacijom promotora.[68] U ovom slučaju, hipermetilacija promotora značajno je povezana s niskom ekspresijom iRNK i niskom ekspresijom proteina, ali ne i s gubitkom heterozigotnosti gena.
Kod sporadičnog karcinoma jajnika nađen je suprotan učinak. Promotori BRCA2 i 5'-UTR regije imaju relativno malo ili nimalo metiliranih CpG dinukleotida u DNK tumora, u usporedbi s onom netumorske DNK, a pronađena je i značajna korelacija između hipometilacije i > 3-puta veće ekspresije BRCA2.[69] Ovo ukazuje da hipometilacija BRCA2 promotora i 5'-UTR regija dovodi do prekomjerne ekspresije BRCA2-ine IRNK.
Jedan izvještaj ukazuje na određenu epigenetičku kontrolu ekspresije BRCA2 pomoću mikroRNK s miR-146a i miR-148a.[70]
Ekspresija BRCA2 kod raka
urediU eukariotima, protein BRCA2 ima važnu ulogu u homolognoj rekombinacijskoj popravci. Kod miševa i ljudi BRCA2 prvenstveno posreduje u urednom sastavljanju RAD51 na jednolančanoj (ss) DNK, obliku koji je aktivan za homologno uparivanje i invaziju lanaca..[71] BRCA2 također preusmjersava r RAD51 iz dvolančane DNK i sprečava disocijaciju od ssDNA.[71] Osim toga, četiri paralozi RAD51, koji se sastoje od RAD51B (RAD51L1), RAD51C (RAD51L2), RAD51D (RAD51L3), XRCC2 čine kompleks koji se naziva kompleks BCDX2 (vidi sliku: Rekombinacijska popravka DNK). Ovaj kompleks sudjeluje u regrutiranju ili stabilizaciji RAD51 na mjestima oštećenja.[30] Čini se da kompleks BCDX2 djeluje olakšavajući sastavljanje ili stabilnost RAD51 nukleoproteinskog filamenta. RAD51 katalizira prijenos niti između prekinute sekvence i njenog neoštećenog homologa, kako bi se omogućila ponovna sinteza oštećene regije (vidi homologni modeli rekombinacije).
Neke studije o raku izvještavaju o prekomjerno izraženom BRCA2, dok druge navode o nedovoljno ieksprimiranje BRCA2. Najmanje dva izvještaja su otkrila prekomjernu ekspresiju u nekim sporadičnim tumorima dojke i nedovoljnu ekspresiju u drugim sporadičnim tumorima dojke.[72][73] (vidi Tabelu). Mnogi karcinomi imaju epigenetičke nedostatke u različitim genima za obnavljanje DNK . Ovi nedostaci popravka vjerovatno uzrokuju povećana nepopravljena oštećenja DNK. Prekomjerna ekspresija BRCA2 uočena kod mnogih karcinoma može odražavati kompenzacijsku prekomjernu ekspresiju BRCA i povećanu homolognu rekombinacijsku popravku, kako bi se barem djelimično nosilo s takvim viškom oštećenja DNK. Egawa et al.[74] sugeriraju da se povećana ekspresija BRCA2 može objasniti genomskom nestabilnošću, koja se često javlja kod karcinoma, što indukuje ekspresiju BRCA2 iRNK, zbog povećane potrebe za BRCA2 za popravak DNK.
Karcinom dojke (uključujući i muški): Međuodnosi fenotip – genotip[20][21][22]
| Lokacija | Fenotip | Fenotipski MIM broj | Nasljeđivanje + oznaka mutacije |
Ključ fenotipskog mapiranja | Oznaka lokusa | Genski/lokusni MIM broj |
| 1p34.1 | Invazivni duktusni | 114480 | AD*, SMu | 3 | RAD54L | 603615 |
| 2q33.1 | Zaštitni | 114480 | AD, SMu | 3 | CASP8 | 601763 |
| 2q35 | Podložnost | 114480 | AD, SMu | 3 | BARD1 | 601593 |
| 3q26.32 | Somatski | 114480 | 3 | PIK3CA | 171834 | |
| 5q34 | Podložnost | 114480 | AD, SMu | 3 | HMMR | 600936 |
| 6p25.2 | Podložnost (?) | 114480 | AD, SMu | 1 | NQO2 | 160998 |
| 6q25 1-q25.2 | Somatski | 114480 | 3 | ESR1 | 133430 | |
| 8q11.23 | Somatski | 114480 | 3 | RB1CC1 | 606837 | |
| 11p15.4 | Somatski | 114480 | 3 | SLC22A1L | 602631 | |
| 11q22.3 | Podložnost | 114480 | AD, SMu | 3 | ATM | 607585 |
| 12p12.1 | Somatski | 114480 | 3 | KRAS | 190070 | |
| 13q13.1 | Podložnost, muški | 114480 | AD, SMu | 3 | BRCA2 | 600185 |
| 14q32.33 | Podložnost | 114480 | AD, SMu | 3 | XRCC3 | 600675 |
| 14q32.33 | Somatski | 114480 | 3 | AKT1 | 164730 | |
| 15q15.1 | Podložnost | 114480 | AD, SMu | 3 | RAD51 | 179617 |
| 16p12.2 | Podložnost | 114480 | AD, SMu | 3 | PALB2 | 610355 |
| 16q22.1 | Režanjski | 114480 | AD, SMu | 3 | CDH1 | 192090 |
| 17q21.33 | Podložnost | 114480 | AD, SMu | 3 | PHB | 176705 |
| 17p13.1 | Somatski | 114480 | 3 | TP53 | 191170 | |
| 17q23.2 | Somatski | 114480 | 3 | PPM1D | 605100 | |
| 17q23.2 | Ranopojavna podložnost | 114480 | AD, SMu | 3 | BRIP1 | 605882 |
| 22q12.1 | Podložnost | 114480 | AD, SMu | 3 | CHEK2 | 604373 |
Nedovoljna ekspresija BRCA2 sama bi dovela do povećanih nepopravljenih oštećenja DNK. Pogreške replikacije nakon ovih oštećenja dovele bi do povećanih mutacija i raka.
| Kancer | Nadekspresija/Posdekspresija | Učestalost izmijenjene ekspresije | Metod procjene | Reference |
|---|---|---|---|---|
| Sporadički kancer jajnika | Nadekspresija | 80% | iRNK | [69] |
| Sporadični kancer jajnika | Podekspresija | 42% | Imunohistohemija | [75] |
| (Studije istih gornjih kancera ) | Povećana ekspresija | 71% | Imunohistohemija | [75] |
| Plućni kancer nemalih ćelija | Podekspresija | 34% | Imunohistohemija | [68] |
| Rak dojke | Nadekspresija | 66% | iRNK | [74] |
| Rak dojkke | Nadekspresija | 20% | iRNK | [72] |
| (Studije istih gornjih kancera) | Podekspresija | 11% | iRNK | [72] |
| Rak dojke | Nadekspresija | 30% | Imunohistohemija | [73] |
| (Studije istih gornjih kancera) | Podekspresija | 30% | Imunohistohemija | [73] |
| Trostruko negativni kancer dojke | Podekspresija | 90% | Imunohistohemija | [76] |
Interakcije
urediPokazalo se da BRCA2 stupa u interakciju sa
- BRE,[77]
- BARD1,[77][78]
- BCCIP,[79]
- BRCA1,[77][80][81][82]
- BRCC3,[77]
- BUB1B,[83]
- CREBBP,[84]
- C11orf30,[85]
- FANCD2,[86][87][88]
- FANCG,[89]
- FLNA,[90]
- HMG20B,[91][92]
- P53,[77][93]
- PALB2,[33][94]
- PCAF,[95][96]
- PLK1,[95][97]
- RAD51,[77][80][95][98][99][100][101][102][103][104][79][81][93]
- RPA1,[105]
- SHFM1[106][107] and
- SMAD3.[108]
Reference
uredi- ^ a b c GRCh38: Ensembl release 89: ENSG00000139618 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000041147 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Hamel PJ (29. 5. 2007). "BRCA1 and BRCA2: No Longer the Only Troublesome Genes Out There". HealthCentral. Pristupljeno 2. 7. 2010.
- ^ "OrthoMaM phylogenetic marker: BRCA2 coding sequence". Arhivirano s originala, 3. 3. 2016. Pristupljeno 19. 2. 2010.
- ^ "BRCA2 gene tree". Ensembl.
- ^ Duncan JA, Reeves JR, Cooke TG (oktobar 1998). "BRCA1 and BRCA2 proteins: roles in health and disease". Molecular Pathology. 51 (5): 237–47. doi:10.1136/mp.51.5.237. PMC 395646. PMID 10193517.
- ^ Yoshida K, Miki Y (novembar 2004). "Role of BRCA1 and BRCA2 as regulators of DNA repair, transcription, and cell cycle in response to DNA damage". Cancer Science. 95 (11): 866–71. doi:10.1111/j.1349-7006.2004.tb02195.x. PMID 15546503. S2CID 24297965.
- ^ Check W (1. 9. 2006). "BRCA: What we know now". College of American Pathologists. Pristupljeno 23. 8. 2010.
- ^ Friedenson B (august 2007). "The BRCA1/2 pathway prevents hematologic cancers in addition to breast and ovarian cancers". BMC Cancer. 7 (1): 152–162. doi:10.1186/1471-2407-7-152. PMC 1959234. PMID 17683622.
- ^ Friedenson B (8. 6. 2008). "Breast cancer genes protect against some leukemias and lymphomas" (video). SciVee.
- ^ "Breast and Ovarian Cancer Genetic Screening". Palo Alto Medical Foundation. Arhivirano s originala, 4. 10. 2008. Pristupljeno 11. 10. 2008.
- ^ Friedenson B (2007). "The BRCA1/2 pathway prevents hematologic cancers in addition to breast and ovarian cancers". BMC Cancer. 7 (1): 152. doi:10.1186/1471-2407-7-152. PMC 1959234. PMID 17683622.
- ^ O'Donovan PJ, Livingston DM (april 2010). "BRCA1 and BRCA2: breast/ovarian cancer susceptibility gene products and participants in DNA double-strand break repair". Carcinogenesis. 31 (6): 961–7. doi:10.1093/carcin/bgq069. PMID 20400477.
- ^ Wooster R, Neuhausen SL, Mangion J, Quirk Y, Ford D, Collins N, Nguyen K, Seal S, Tran T, Averill D (septembar 1994). "Localization of a breast cancer susceptibility gene, BRCA2, to chromosome 13q12-13". Science. 265 (5181): 2088–90. Bibcode:1994Sci...265.2088W. doi:10.1126/science.8091231. PMID 8091231.
- ^ "BRCA2 breast cancer 2, early onset [Homo sapiens]". EntrezGene. National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Breast cancer type 2 susceptibility protein - Homo sapiens (Human)". P51587. UniProt.
- ^ Williams-Jones B (2002). Genetic testing for sale: Implications of commercial brca testing in Canada (Ph.D.). The University of British Columbia.
- ^ a b OMIM Entry Search - brca3
- ^ a b OMIM Entry - # 114480 - BREAST CANCER
- ^ a b https://omim.org/search?index=entry&sort=score+desc%2C+prefix_sort+desc&start=1&limit=10&search=brca3
- ^ "UniProt, P51587". Pristupljeno 11. 9. 2017.
- ^ D'Andrea AD (2010). "Susceptibility pathways in Fanconi's anemia and breast cancer". N. Engl. J. Med. 362 (20): 1909–19. doi:10.1056/NEJMra0809889. PMC 3069698. PMID 20484397.
- ^ Sobeck A, Stone S, Landais I, de Graaf B, Hoatlin ME (2009). "The Fanconi anemia protein FANCM is controlled by FANCD2 and the ATR/ATM pathways". J. Biol. Chem. 284 (38): 25560–8. doi:10.1074/jbc.M109.007690. PMC 2757957. PMID 19633289.
- ^ Castillo P, Bogliolo M, Surralles J (2011). "Coordinated action of the Fanconi anemia and ataxia telangiectasia pathways in response to oxidative damage". DNA Repair (Amst.). 10 (5): 518–25. doi:10.1016/j.dnarep.2011.02.007. PMID 21466974.
- ^ Stolz A, Ertych N, Bastians H (2011). "Tumor suppressor CHK2: regulator of DNA damage response and mediator of chromosomal stability". Clin. Cancer Res. 17 (3): 401–5. doi:10.1158/1078-0432.CCR-10-1215. PMID 21088254.
- ^ Taniguchi T, Garcia-Higuera I, Andreassen PR, Gregory RC, Grompe M, D'Andrea AD (2002). "S-phase-specific interaction of the Fanconi anemia protein, FANCD2, with BRCA1 and RAD51". Blood. 100 (7): 2414–20. doi:10.1182/blood-2002-01-0278. PMID 12239151.
- ^ Park JY, Zhang F, Andreassen PR (2014). "PALB2: the hub of a network of tumor suppressors involved in DNA damage responses". Biochim. Biophys. Acta. 1846 (1): 263–75. doi:10.1016/j.bbcan.2014.06.003. PMC 4183126. PMID 24998779.
- ^ a b Chun J, Buechelmaier ES, Powell SN (2013). "Rad51 paralog complexes BCDX2 and CX3 act at different stages in the BRCA1-BRCA2-dependent homologous recombination pathway". Mol. Cell. Biol. 33 (2): 387–95. doi:10.1128/MCB.00465-12. PMC 3554112. PMID 23149936.
- ^ Jensen RB, Carreira A, Kowalczykowski SC (oktobar 2010). "Purified human BRCA2 stimulates RAD51-mediated recombination". Nature. 467 (7316): 678–83. Bibcode:2010Natur.467..678J. doi:10.1038/nature09399. PMC 2952063. PMID 20729832.
- ^ Wang CX, Jimenez-Sainz J, Jensen RB, Mazin AV (mart 2019). "The Post-Synaptic Function of Brca2". Scientific Reports. 9 (1): 4554. Bibcode:2019NatSR...9.4554W. doi:10.1038/s41598-019-41054-y. PMC 6418147. PMID 30872704.
- ^ a b Xia B, Sheng Q, Nakanishi K, Ohashi A, Wu J, Christ N, Liu X, Jasin M, Couch FJ, Livingston DM (juni 2006). "Control of BRCA2 cellular and clinical functions by a nuclear partner, PALB2". Molecular Cell. 22 (6): 719–29. doi:10.1016/j.molcel.2006.05.022. PMID 16793542.
- ^ Buisson R, Dion-Côté AM, Coulombe Y, Launay H, Cai H, Stasiak AZ, Stasiak A, Xia B, Masson JY (oktobar 2010). "Cooperation of breast cancer proteins PALB2 and piccolo BRCA2 in stimulating homologous recombination". Nature Structural & Molecular Biology. 17 (10): 1247–54. doi:10.1038/nsmb.1915. PMC 4094107. PMID 20871615.
- ^ Mijic S, Zellweger R, Chappidi N, Berti M, Jacobs K, Mutreja K, Ursich S, Ray Chaudhuri A, Nussenzweig A, Janscak P, Lopes M (oktobar 2017). "Replication fork reversal triggers fork degradation in BRCA2-defective cells". Nature Communications (jezik: engleski). 8 (1): 859. Bibcode:2017NatCo...8..859M. doi:10.1038/s41467-017-01164-5. PMC 5643541. PMID 29038466.
- ^ Levin B, Lech D, Friedenson B (2012). "Evidence that BRCA1- or BRCA2-associated cancers are not inevitable". Molecular Medicine. 18 (9): 1327–37. doi:10.2119/molmed.2012.00280. PMC 3521784. PMID 22972572.
- ^ "High-Penetrance Breast and/or Ovarian Cancer Susceptibility Genes". National Cancer Institute. Pristupljeno 7. 12. 2012.
- ^ a b Lacroix M, Leclercq G (2005). "The "portrait" of hereditary breast cancer". Breast Cancer Research and Treatment. 89 (3): 297–304. doi:10.1007/s10549-004-2172-4. PMID 15754129. S2CID 23327569.
- ^ a b Thorlacius S, Olafsdottir G, Tryggvadottir L, Neuhausen S, Jonasson JG, Tavtigian SV, Tulinius H, Ogmundsdottir HM, Eyfjörd JE (1996). "A single BRCA2 mutation in male and female breast cancer families from Iceland with varied cancer phenotypes". Nature Genetics. 13 (1): 117–119. doi:10.1038/ng0596-117. PMID 8673089. S2CID 8443452.
- ^ a b Thorlacius S, Sigurdsson S, Bjarnadottir H, Olafsdottir G, Jonasson JG, Tryggvadottir L, Tulinius H, Eyfjörd JE (1997). "Study of a single BRCA2 mutation with high carrier frequency in a small population". American Journal of Human Genetics. 60 (5): 1079–1085. PMC 1712443. PMID 9150155.
- ^ den Dunnen JT, Antonarakis SE (2000). "Mutation nomenclature extensions and suggestions to describe complex mutations: a discussion". Human Mutation. 15 (1): 7–12. doi:10.1002/(SICI)1098-1004(200001)15:1<7::AID-HUMU4>3.0.CO;2-N. PMID 10612815.
- ^ Neuhausen S, Gilewski T, Norton L, Tran T, McGuire P, Swensen J, Hampel H, Borgen P, Brown K, Skolnick M, Shattuck-Eidens D, Jhanwar S, Goldgar D, Offit K (1996). "Recurrent BRCA2 6174delT mutations in Ashkenazi Jewish women affected by breast cancer". Nature Genetics. 13 (1): 126–128. doi:10.1038/ng0596-126. PMID 8673092. S2CID 11909356.
- ^ Verhoog LC, van den Ouweland AM, Berns E, van Veghel-Plandsoen MM, van Staveren IL, Wagner A, Bartels CC, Tilanus-Linthorst MM, Devilee P, Seynaeve C, Halley DJ, Niermeijer MF, Klijn JG, Meijers-Heijboer H (2001). "Large regional differences in the frequency of distinct BRCA1/BRCA2 mutations in 517 Dutch breast and/or ovarian cancer families". European Journal of Cancer. 37 (16): 2082–2090. doi:10.1016/S0959-8049(01)00244-1. PMID 11597388.
- ^ Huusko P, Pääkkönen K, Launonen V, Pöyhönen M, Blanco G, Kauppila A, Puistola U, Kiviniemi H, Kujala M, Leisti J, Winqvist R (1998). "Evidence of founder mutations in Finnish BRCA1 and BRCA2 families". American Journal of Human Genetics. 62 (6): 1544–1548. doi:10.1086/301880. PMC 1377159. PMID 9585608.
- ^ Pääkkönen K, Sauramo S, Sarantaus L, Vahteristo P, Hartikainen A, Vehmanen P, Ignatius J, Ollikainen V, Kääriäinen H, Vauramo E, Nevanlinna H, Krahe R, Holli K, Kere J (2001). "Involvement of BRCA1 and BRCA2 in breast cancer in a western Finnish sub-population". Genetic Epidemiology. 20 (2): 239–246. doi:10.1002/1098-2272(200102)20:2<239::AID-GEPI6>3.0.CO;2-Y. PMID 11180449.
- ^ Tonin PN, Mes-Masson AM, Narod SA, Ghadirian P, Provencher D (1999). "Founder BRCA1 and BRCA2 mutations in French Canadian ovarian cancer cases unselected for family history". Clinical Genetics. 55 (5): 318–324. doi:10.1034/j.1399-0004.1999.550504.x. PMID 10422801. S2CID 23931343.
- ^ Oros KK, Leblanc G, Arcand SL, Shen Z, Perret C, Mes-Masson AM, Foulkes WD, Ghadirian P, Provencher D, Tonin PN (2006). "Haplotype analysis suggests common founders in carriers of recurrent BRCA2 mutation, 3398delAAAAG, in French Canadian hereditary breast and/ovarian cancer families". BMC Medical Genetics. 7 (23): 23. doi:10.1186/1471-2350-7-23. PMC 1464093. PMID 16539696.
- ^ Tonin PN (2006). "The limited spectrum of pathogenic BRCA1 and BRCA2 mutations in the French Canadian breast and breast-ovarian cancer families, a founder population of Quebec, Canada". Bull Cancer. 93 (9): 841–846. PMID 16980226.
- ^ Van Der Looij M, Szabo C, Besznyak I, Liszka G, Csokay B, Pulay T, Toth J, Devilee P, King MC, Olah E (2000). "Prevalence of founder BRCA1 and BRCA2 mutations among breast and ovarian cancer patients in Hungary". International Journal of Cancer. 86 (5): 737–740. doi:10.1002/(SICI)1097-0215(20000601)86:5<737::AID-IJC21>3.0.CO;2-1. PMID 10797299.
- ^ Pisano M, Cossu A, Persico I, Palmieri G, Angius A, Casu G, Palomba G, Sarobba MG, Rocca PC, Dedola MF, Olmeo N, Pasca A, Budroni M, Marras V, Pisano A, Farris A, Massarelli G, Pirastu M, Tanda F (2000). "Identification of a founder BRCA2 mutation in Sardinia". British Journal of Cancer. 82 (3): 553–559. doi:10.1054/bjoc.1999.0963. PMC 2363305. PMID 10682665.
- ^ a b Scottish/Northern Irish BRCAI/BRCA2 Consortium (2003). "BRCA1 and BRCA2 mutations in Scotland and Northern Ireland". British Journal of Cancer. 88 (8): 1256–1262. doi:10.1038/sj.bjc.6600840. PMC 2747571. PMID 12698193.
- ^ Liede A, Malik IA, Aziz Z, Rios Pd Pde L, Kwan E, Narod SA (2002). "Contribution of BRCA1 and BRCA2 mutations to breast and ovarian cancer in Pakistan". American Journal of Human Genetics. 71 (3): 595–606. doi:10.1086/342506. PMC 379195. PMID 12181777.
- ^ Krajc M, De Grève J, Goelen G, Teugels E (2002). "BRCA2 founder mutation in Slovenian breast cancer families". European Journal of Human Genetics. 10 (12): 879–882. doi:10.1038/sj.ejhg.5200886. PMID 12461697.
- ^ Osorio A, Robledo M, Martínez B, Cebrián A, San Román JM, Albertos J, Lobo F, Benítez J (1998). "Molecular analysis of the BRCA2 gene in 16 breast/ovarian cancer Spanish families". Clin. Genet. 54 (2): 142–7. doi:10.1111/j.1399-0004.1998.tb03717.x. PMID 9761393. S2CID 30388365.
- ^ Neuhausen SL (2000). "Founder populations and their uses for breast cancer genetics". Cancer Research. 2 (2): 77–81. doi:10.1186/bcr36. PMC 139426. PMID 11250694.
- ^ a b Seeliger K, Dukowic-Schulze S, Wurz-Wildersinn R, Pacher M, Puchta H (2012). "BRCA2 is a mediator of RAD51- and DMC1-facilitated homologous recombination in Arabidopsis thaliana". New Phytol. 193 (2): 364–75. doi:10.1111/j.1469-8137.2011.03947.x. PMID 22077663.
- ^ Kojic M, Kostrub CF, Buchman AR, Holloman WK (2002). "BRCA2 homolog required for proficiency in DNA repair, recombination, and genome stability in Ustilago maydis". Mol. Cell. 10 (3): 683–91. doi:10.1016/s1097-2765(02)00632-9. PMID 12408834.
- ^ Ko E, Lee J, Lee H (2008). "Essential role of brc-2 in chromosome integrity of germ cells in C. elegans". Mol. Cells. 26 (6): 590–4. PMID 18779660.
- ^ Martin JS, Winkelmann N, Petalcorin MI, McIlwraith MJ, Boulton SJ (2005). "RAD-51-dependent and -independent roles of a Caenorhabditis elegans BRCA2-related protein during DNA double-strand break repair". Mol. Cell. Biol. 25 (8): 3127–39. doi:10.1128/MCB.25.8.3127-3139.2005. PMC 1069622. PMID 15798199.
- ^ Klovstad M, Abdu U, Schüpbach T (2008). "Drosophila brca2 is required for mitotic and meiotic DNA repair and efficient activation of the meiotic recombination checkpoint". PLOS Genet. 4 (2): e31. doi:10.1371/journal.pgen.0040031. PMC 2233675. PMID 18266476.
- ^ Connor F, Bertwistle D, Mee PJ, Ross GM, Swift S, Grigorieva E, Tybulewicz VL, Ashworth A (1997). "Tumorigenesis and a DNA repair defect in mice with a truncating Brca2 mutation". Nat. Genet. 17 (4): 423–30. doi:10.1038/ng1297-423. PMID 9398843. S2CID 42462448.
- ^ Cotroneo MS, Haag JD, Zan Y, Lopez CC, Thuwajit P, Petukhova GV, Camerini-Otero RD, Gendron-Fitzpatrick A, Griep AE, Murphy CJ, Dubielzig RR, Gould MN (2007). "Characterizing a rat Brca2 knockout model". Oncogene. 26 (11): 1626–35. doi:10.1038/sj.onc.1209960. PMID 16964288.
- ^ a b Martinez JS, von Nicolai C, Kim T, Ehlén Å, Mazin AV, Kowalczykowski SC, Carreira A (2016). "BRCA2 regulates DMC1-mediated recombination through the BRC repeats". Proc. Natl. Acad. Sci. U.S.A. 113 (13): 3515–20. Bibcode:2016PNAS..113.3515M. doi:10.1073/pnas.1601691113. PMC 4822569. PMID 26976601.
- ^ a b Frappart PO, Lee Y, Lamont J, McKinnon PJ (2007). "BRCA2 is required for neurogenesis and suppression of medulloblastoma". EMBO J. 26 (11): 2732–42. doi:10.1038/sj.emboj.7601703. PMC 1888666. PMID 17476307.
- ^ Teng DH, Bogden R, Mitchell J, Baumgard M, Bell R, Berry S, Davis T, Ha PC, Kehrer R, Jammulapati S, Chen Q, Offit K, Skolnick MH, Tavtigian SV, Jhanwar S, Swedlund B, Wong AK, Kamb A (1996). "Low incidence of BRCA2 mutations in breast carcinoma and other cancers". Nat. Genet. 13 (2): 241–4. doi:10.1038/ng0696-241. PMID 8640236. S2CID 9831745.
- ^ Miki Y, Katagiri T, Kasumi F, Yoshimoto T, Nakamura Y (1996). "Mutation analysis in the BRCA2 gene in primary breast cancers". Nat. Genet. 13 (2): 245–7. doi:10.1038/ng0696-245. PMID 8640237. S2CID 3203046.
- ^ Lancaster JM, Wooster R, Mangion J, Phelan CM, Cochran C, Gumbs C, Seal S, Barfoot R, Collins N, Bignell G, Patel S, Hamoudi R, Larsson C, Wiseman RW, Berchuck A, Iglehart JD, Marks JR, Ashworth A, Stratton MR, Futreal PA (1996). "BRCA2 mutations in primary breast and ovarian cancers". Nat. Genet. 13 (2): 238–40. doi:10.1038/ng0696-238. PMID 8640235. S2CID 26808443.
- ^ a b Lee MN, Tseng RC, Hsu HS, Chen JY, Tzao C, Ho WL, Wang YC (2007). "Epigenetic inactivation of the chromosomal stability control genes BRCA1, BRCA2, and XRCC5 in non-small cell lung cancer". Clin. Cancer Res. 13 (3): 832–8. doi:10.1158/1078-0432.CCR-05-2694. PMID 17289874.
- ^ a b Chan KY, Ozçelik H, Cheung AN, Ngan HY, Khoo US (2002). "Epigenetic factors controlling the BRCA1 and BRCA2 genes in sporadic ovarian cancer". Cancer Res. 62 (14): 4151–6. PMID 12124354.
- ^ Gu Y, Zhang M, Peng F, Fang L, Zhang Y, Liang H, Zhou W, Ao L, Guo Z (2015). "The BRCA1/2-directed miRNA signature predicts a good prognosis in ovarian cancer patients with wild-type BRCA1/2". Oncotarget. 6 (4): 2397–406. doi:10.18632/oncotarget.2963. PMC 4385859. PMID 25537514.
- ^ a b Holloman WK (2011). "Unraveling the mechanism of BRCA2 in homologous recombination". Nat. Struct. Mol. Biol. 18 (7): 748–54. doi:10.1038/nsmb.2096. PMC 3647347. PMID 21731065.
- ^ a b c Bièche I, Noguès C, Lidereau R (1999). "Overexpression of BRCA2 gene in sporadic breast tumours". Oncogene. 18 (37): 5232–8. doi:10.1038/sj.onc.1202903. PMID 10498873.
- ^ a b c Hedau S, Batra M, Singh UR, Bharti AC, Ray A, Das BC (2015). "Expression of BRCA1 and BRCA2 proteins and their correlation with clinical staging in breast cancer". J Cancer Res Ther. 11 (1): 158–63. doi:10.4103/0973-1482.140985. PMID 25879355.
- ^ a b Egawa C, Miyoshi Y, Taguchi T, Tamaki Y, Noguchi S (2002). "High BRCA2 mRNA expression predicts poor prognosis in breast cancer patients". Int. J. Cancer. 98 (6): 879–82. doi:10.1002/ijc.10231. PMID 11948466. S2CID 9083282.
- ^ a b Swisher EM, Gonzalez RM, Taniguchi T, Garcia RL, Walsh T, Goff BA, Welcsh P (2009). "Methylation and protein expression of DNA repair genes: association with chemotherapy exposure and survival in sporadic ovarian and peritoneal carcinomas". Mol. Cancer. 8 (1): 48. doi:10.1186/1476-4598-8-48. PMC 2719582. PMID 19602291.
- ^ Thike AA, Tan PH, Ikeda M, Iqbal J (2016). "Increased ID4 expression, accompanied by mutant p53 accumulation and loss of BRCA1/2 proteins in triple-negative breast cancer, adversely affects survival". Histopathology. 68 (5): 702–12. doi:10.1111/his.12801. PMID 26259780. S2CID 3566545.
- ^ a b c d e f Dong Y, Hakimi MA, Chen X, Kumaraswamy E, Cooch NS, Godwin AK, Shiekhattar R (novembar 2003). "Regulation of BRCC, a holoenzyme complex containing BRCA1 and BRCA2, by a signalosome-like subunit and its role in DNA repair". Mol. Cell. 12 (5): 1087–99. doi:10.1016/S1097-2765(03)00424-6. PMID 14636569.
- ^ Ryser S, Dizin E, Jefford CE, Delaval B, Gagos S, Christodoulidou A, Krause KH, Birnbaum D, Irminger-Finger I (februar 2009). "Distinct roles of BARD1 isoforms in mitosis: full-length BARD1 mediates Aurora B degradation, cancer-associated BARD1beta scaffolds Aurora B and BRCA2". Cancer Res. 69 (3): 1125–34. doi:10.1158/0008-5472.CAN-08-2134. PMID 19176389.
- ^ a b Liu J, Yuan Y, Huan J, Shen Z (januar 2001). "Inhibition of breast and brain cancer cell growth by BCCIPalpha, an evolutionarily conserved nuclear protein that interacts with BRCA2". Oncogene. 20 (3): 336–45. doi:10.1038/sj.onc.1204098. PMID 11313963.
- ^ a b Sarkisian CJ, Master SR, Huber LJ, Ha SI, Chodosh LA (oktobar 2001). "Analysis of murine Brca2 reveals conservation of protein-protein interactions but differences in nuclear localization signals". J. Biol. Chem. 276 (40): 37640–8. doi:10.1074/jbc.M106281200. PMID 11477095.
- ^ a b Chen J, Silver DP, Walpita D, Cantor SB, Gazdar AF, Tomlinson G, Couch FJ, Weber BL, Ashley T, Livingston DM, Scully R (septembar 1998). "Stable interaction between the products of the BRCA1 and BRCA2 tumor suppressor genes in mitotic and meiotic cells". Mol. Cell. 2 (3): 317–28. doi:10.1016/S1097-2765(00)80276-2. PMID 9774970.
- ^ Reuter TY, Medhurst AL, Waisfisz Q, Zhi Y, Herterich S, Hoehn H, Gross HJ, Joenje H, Hoatlin ME, Mathew CG, Huber PA (oktobar 2003). "Yeast two-hybrid screens imply involvement of Fanconi anemia proteins in transcription regulation, cell signaling, oxidative metabolism, and cellular transport". Exp. Cell Res. 289 (2): 211–21. doi:10.1016/S0014-4827(03)00261-1. PMID 14499622.
- ^ Futamura M, Arakawa H, Matsuda K, Katagiri T, Saji S, Miki Y, Nakamura Y (mart 2000). "Potential role of BRCA2 in a mitotic checkpoint after phosphorylation by hBUBR1". Cancer Res. 60 (6): 1531–5. PMID 10749118.
- ^ Siddique H, Rao VN, Reddy ES (august 2009). "CBP-mediated post-translational N-glycosylation of BRCA2". Int J Oncol. 35 (2): 16387–91. doi:10.3892/ijo_00000351. PMID 19578754.
- ^ Hughes-Davies L, Huntsman D, Ruas M, Fuks F, Bye J, Chin SF, Milner J, Brown LA, Hsu F, Gilks B, Nielsen T, Schulzer M, Chia S, Ragaz J, Cahn A, Linger L, Ozdag H, Cattaneo E, Jordanova ES, Schuuring E, Yu DS, Venkitaraman A, Ponder B, Doherty A, Aparicio S, Bentley D, Theillet C, Ponting CP, Caldas C, Kouzarides T (novembar 2003). "EMSY links the BRCA2 pathway to sporadic breast and ovarian cancer". Cell. 115 (5): 523–35. doi:10.1016/S0092-8674(03)00930-9. PMID 14651845. S2CID 18911371.
- ^ Wang X, Andreassen PR, D'Andrea AD (juli 2004). "Functional interaction of monoubiquitinated FANCD2 and BRCA2/FANCD1 in chromatin". Mol. Cell. Biol. 24 (13): 5850–62. doi:10.1128/MCB.24.13.5850-5862.2004. PMC 480901. PMID 15199141.
- ^ Hussain S, Wilson JB, Medhurst AL, Hejna J, Witt E, Ananth S, Davies A, Masson JY, Moses R, West SC, de Winter JP, Ashworth A, Jones NJ, Mathew CG (juni 2004). "Direct interaction of FANCD2 with BRCA2 in DNA damage response pathways". Hum. Mol. Genet. 13 (12): 1241–8. doi:10.1093/hmg/ddh135. PMID 15115758.
- ^ Hejna J, Holtorf M, Hines J, Mathewson L, Hemphill A, Al-Dhalimy M, Olson SB, Moses RE (april 2008). "Tip60 is required for DNA interstrand cross-link repair in the Fanconi anemia pathway". J. Biol. Chem. 283 (15): 9844–51. doi:10.1074/jbc.M709076200. PMC 2398728. PMID 18263878.
- ^ Hussain S, Witt E, Huber PA, Medhurst AL, Ashworth A, Mathew CG (oktobar 2003). "Direct interaction of the Fanconi anaemia protein FANCG with BRCA2/FANCD1". Hum. Mol. Genet. 12 (19): 2503–10. doi:10.1093/hmg/ddg266. PMID 12915460.
- ^ Yuan Y, Shen Z (decembar 2001). "Interaction with BRCA2 suggests a role for filamin-1 (hsFLNa) in DNA damage response". J. Biol. Chem. 276 (51): 48318–24. doi:10.1074/jbc.M102557200. PMID 11602572.
- ^ Marmorstein LY, Kinev AV, Chan GK, Bochar DA, Beniya H, Epstein JA, Yen TJ, Shiekhattar R (januar 2001). "A human BRCA2 complex containing a structural DNA binding component influences cell cycle progression". Cell. 104 (2): 247–57. doi:10.1016/S0092-8674(01)00209-4. PMID 11207365. S2CID 5822368.
- ^ Hakimi MA, Bochar DA, Chenoweth J, Lane WS, Mandel G, Shiekhattar R (maj 2002). "A core-BRAF35 complex containing histone deacetylase mediates repression of neuronal-specific genes". Proc. Natl. Acad. Sci. U.S.A. 99 (11): 7420–5. Bibcode:2002PNAS...99.7420H. doi:10.1073/pnas.112008599. PMC 124246. PMID 12032298.
- ^ a b Marmorstein LY, Ouchi T, Aaronson SA (novembar 1998). "The BRCA2 gene product functionally interacts with p53 and RAD51". Proc. Natl. Acad. Sci. U.S.A. 95 (23): 13869–74. Bibcode:1998PNAS...9513869M. doi:10.1073/pnas.95.23.13869. PMC 24938. PMID 9811893.
- ^ "Entrez Gene: PALB2 partner and localizer of BRCA2".
- ^ a b c Lin HR, Ting NS, Qin J, Lee WH (septembar 2003). "M phase-specific phosphorylation of BRCA2 by Polo-like kinase 1 correlates with the dissociation of the BRCA2-P/CAF complex". J. Biol. Chem. 278 (38): 35979–87. doi:10.1074/jbc.M210659200. PMID 12815053.
- ^ Fuks F, Milner J, Kouzarides T (novembar 1998). "BRCA2 associates with acetyltransferase activity when bound to P/CAF". Oncogene. 17 (19): 2531–4. doi:10.1038/sj.onc.1202475. PMID 9824164.
- ^ Lee M, Daniels MJ, Venkitaraman AR (januar 2004). "Phosphorylation of BRCA2 by the Polo-like kinase Plk1 is regulated by DNA damage and mitotic progression". Oncogene. 23 (4): 865–72. doi:10.1038/sj.onc.1207223. PMID 14647413.
- ^ Sharan SK, Morimatsu M, Albrecht U, Lim DS, Regel E, Dinh C, Sands A, Eichele G, Hasty P, Bradley A (april 1997). "Embryonic lethality and radiation hypers
ensitivity mediated by Rad51 in mice lacking Brca2". Nature. 386 (6627): 804–10. Bibcode:1997Natur.386..804S. doi:10.1038/386804a0. hdl:11858/00-001M-0000-0010-5059-F. PMID 9126738. S2CID 4238943. line feed character u
|title=na mjestu 41 (pomoć) - ^ Yu DS, Sonoda E, Takeda S, Huang CL, Pellegrini L, Blundell TL, Venkitaraman AR (oktobar 2003). "Dynamic control of Rad51 recombinase by self-association and interaction with BRCA2". Mol. Cell. 12 (4): 1029–41. doi:10.1016/S1097-2765(03)00394-0. PMID 14580352.
- ^ Chen PL, Chen CF, Chen Y, Xiao J, Sharp ZD, Lee WH (april 1998). "The BRC repeats in BRCA2 are critical for RAD51 binding and resistance to methyl methanesulfonate treatment". Proc. Natl. Acad. Sci. U.S.A. 95 (9): 5287–92. Bibcode:1998PNAS...95.5287C. doi:10.1073/pnas.95.9.5287. PMC 20253. PMID 9560268.
- ^ Wong AK, Pero R, Ormonde PA, Tavtigian SV, Bartel PL (decembar 1997). "RAD51 interacts with the evolutionarily conserved BRC motifs in the human breast cancer susceptibility gene brca2". J. Biol. Chem. 272 (51): 31941–4. doi:10.1074/jbc.272.51.31941. PMID 9405383.
- ^ Katagiri T, Saito H, Shinohara A, Ogawa H, Kamada N, Nakamura Y, Miki Y (mart 1998). "Multiple possible sites of BRCA2 interacting with DNA repair protein RAD51". Genes Chromosomes Cancer. 21 (3): 217–22. doi:10.1002/(SICI)1098-2264(199803)21:3<217::AID-GCC5>3.0.CO;2-2. PMID 9523196.
- ^ Pellegrini L, Yu DS, Lo T, Anand S, Lee M, Blundell TL, Venkitaraman AR (novembar 2002). "Insights into DNA recombination from the structure of a RAD51-BRCA2 complex". Nature. 420 (6913): 287–93. Bibcode:2002Natur.420..287P. doi:10.1038/nature01230. PMID 12442171. S2CID 4359383.
- ^ Tarsounas M, Davies AA, West SC (januar 2004). "RAD51 localization and activation following DNA damage". Philos. Trans. R. Soc. Lond. B Biol. Sci. 359 (1441): 87–93. doi:10.1098/rstb.2003.1368. PMC 1693300. PMID 15065660.
- ^ Wong JM, Ionescu D, Ingles CJ (januar 2003). "Interaction between BRCA2 and replication protein A is compromised by a cancer-predisposing mutation in BRCA2". Oncogene. 22 (1): 28–33. doi:10.1038/sj.onc.1206071. PMID 12527904.
- ^ Marston NJ, Richards WJ, Hughes D, Bertwistle D, Marshall CJ, Ashworth A (juli 1999). "Interaction between the product of the breast cancer susceptibility gene BRCA2 and DSS1, a protein functionally conserved from yeast to mammals". Mol. Cell. Biol. 19 (7): 4633–42. doi:10.1128/MCB.19.7.4633. PMC 84261. PMID 10373512.
- ^ Yang H, Jeffrey PD, Miller J, Kinnucan E, Sun Y, Thoma NH, Zheng N, Chen PL, Lee WH, Pavletich NP (septembar 2002). "BRCA2 function in DNA binding and recombination from a BRCA2-DSS1-ssDNA structure". Science. 297 (5588): 1837–48. Bibcode:2002Sci...297.1837Y. doi:10.1126/science.297.5588.1837. PMID 12228710.
- ^ Preobrazhenska O, Yakymovych M, Kanamoto T, Yakymovych I, Stoika R, Heldin CH, Souchelnytskyi S (august 2002). "BRCA2 and Smad3 synergize in regulation of gene transcription". Oncogene. 21 (36): 5660–4. doi:10.1038/sj.onc.1205732. PMID 12165866.
Dopunska literatura
uredi- Zou JP, Hirose Y, Siddique H, Rao VN, Reddy ES (1999). "Structure and expression of variant BRCA2a lacking the transactivation domain". Oncology Reports. 6 (2): 437–40. doi:10.3892/or.6.2.437. PMID 10023017.
- Venkitaraman AR (2001). "Chromosome stability, DNA recombination and the BRCA2 tumour suppressor". Current Opinion in Cell Biology. 13 (3): 338–43. doi:10.1016/S0955-0674(00)00217-9. PMID 11343905.
- Orelli BJ, Bishop DK (2001). "BRCA2 and homologous recombination". Breast Cancer Research. 3 (5): 294–8. doi:10.1186/bcr310. PMC 138691. PMID 11597317.
- Daniel DC (2002). "Highlight: BRCA1 and BRCA2 proteins in breast cancer". Microscopy Research and Technique. 59 (1): 68–83. doi:10.1002/jemt.10178. PMID 12242698. S2CID 30091586.
- Tutt A, Ashworth A (2003). "The relationship between the roles of BRCA genes in DNA repair and cancer predisposition". Trends in Molecular Medicine. 8 (12): 571–6. doi:10.1016/S1471-4914(02)02434-6. PMID 12470990.
- Gonçalves A, Viens P, Sobol H, Maraninchi D, Bertucci F (2005). "[Molecular alterations in breast cancer: clinical implications and new analytical tools]". Revue de Médecine Interne. 26 (6): 470–8. doi:10.1016/j.revmed.2004.11.012. PMID 15936476.
- Hay T, Clarke AR (2005). "DNA damage hypersensitivity in cells lacking BRCA2: a review of in vitro and in vivo data". Biochemical Society Transactions. 33 (Pt 4): 715–7. doi:10.1042/BST0330715. PMID 16042582.
- Domchek SM, Weber BL (2006). "Clinical management of BRCA1 and BRCA2 mutation carriers". Oncogene. 25 (43): 5825–31. doi:10.1038/sj.onc.1209881. PMID 16998496.
- Honrado E, Osorio A, Palacios J, Benitez J (2006). "Pathology and gene expression of hereditary breast tumors associated with BRCA1, BRCA2 and CHEK2 gene mutations". Oncogene. 25 (43): 5837–45. doi:10.1038/sj.onc.1209875. PMID 16998498. S2CID 20960561.
Vanjski linkovi
uredi- BRCA2 Protein na US National Library of Medicine Medical Subject Headings (MeSH)





