Smith–Lemli–Opitzov sindrom
Smith–Lemli–Opitzov sindrom je urođena greška sinteze holesterola.[1] To je autosomni recesivni, sindrom višestruke malformacije uzrokovan mutacijom u genu DHCR7za kodiranje enzima 7-dehidrokolesterol-reduktaza. Izaziva širok spektar efekata, u rasponu od blage intelektualne nesposobnosti i problema u ponašanju do smrtonosnih malformacija.[2]
| Smith–Lemli–Opitzov sindrom | |
|---|---|
| Drugi nazivi | SLOS, nedostatak 7-dehidroholesterol-reduktaze |
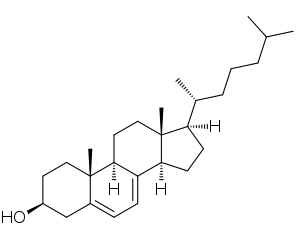 | |
| 7-Dehidrokolesterol je toksični steroidni metabolit koji se akumulira u organizmima osoba sa SLOS | |
| Specijalnost | Medicinska genetika |
| Uobičajeno pojavljivanje | Pri rođenju (urođeni poremećaj |
| Frekvencija | 1/20.000 do 1/60.000 |
Znakovi i simptomi
urediSLOS se može različito predstaviti u različitim slučajevima, u zavisnosti od težine mutacije i drugih faktora. Prvobitno, SLOS pacijenti su klasifikovani u dvije kategorije (klasične i teške), a na osnovu fizičkih i mentalnih obilježja, uz druge kliničke karakteristike. Od otkrića specifičnog biohemijskog defekta odgovornog za SLOS, pacijentima se daje ocjena ozbiljnosti na osnovu njihovih nivoa cerebralnih, očnih, oralnih i genitalnih defekata. Zatim se koristi za klasifikaciju pacijenata na blage, klasične ili teške SLOS.[3]
Fizička obilježja
urediNajčešće crte lica SLOS-a su mikrocefalija, bisljepočno suženje (smanjena udaljenost između slepoočnica), ptoza, kratak i uvrnut nos, mikrognatija, epikantusni nabori i kapilarni hemangiom nosa.[3] Ostale fizičke karakteristike uključuju:
- Nisko postavljene i stražnje rotirane uši
- Visoko savijeno, usko, tvrdo nepce
- rascjep usne i/ilinepca
- Ageneza ili hipoplazija corpus callosum
- Cerebelumska hipoplazija
- Povećana veličina komornog sistema
- Smanjena veličina čeonog režnja.
- Polidaktilija šaka ili stopala
- Kratak, proksimalno postavljen palac
- Ostale malformacije prstiju
- Sindaktilija drugog i trećeg prsta
- Dvosmislene ili ženske genitalije
- Urođene srčane mane
- Abnormalnosti bubrega, pluća, jetre i očiju
S obzirom da je SLOS uzrokovan mutacijom enzima uključenog u sintezu holesterola, rezultirajuće biohemijske karakteristike mogu biti predvidljive. Većina pacijenata ima snižene nivoe holesterola u plazmi (hipoholesterolemija). Međutim, otprilike 10% može imati normalne nivoe holesterola,[3] i smanjene koncentracije holesterola nisu samo indikativni za SLOS. Povećani nivoi prekursora holesterola su takođe česti kod SLOS. Konkretno, povišeni nivoi 7-dehidrokolesterola su prilično specifični za SLOS.
Genetika
urediDHCR7
urediGen koji kodira DHCR7 (označen kao DHCR7) kloniran je 1998. godine i mapiran je na hromosomu 11, pozicija q12-13.[1] Dužine je 14.100 baznih parova DNK i sadrži devet egzona,[4] odgovarajuća iRNK ima dužinu od 2.786 parova baza (preostala sekvenca DNK je intronska). Struktura pacovskog gena DHCR7 vrlo je slična strukturi ljudskog gena.[1]
Najviši nivoi ekspresije DHCR7 otkriveni su u nadbubrežna žlijezdama, sjemenicima, jetri i u moždanom tkivu.[1] Njegova ekspresija je indukovana smanjenim koncentracijama sterola, putem proteina koji se regulišu na sterol (SREBP). Također postoje dokazi da se njegova aktivnost može regulisati transkripcijom specifičnom za tkivo i alternativnom preradom.
Kao što je gore navedeno, enzim DHCR7 katalizira redukciju 7DHC u holesterol, kao i redukciju 7-dehidrodezmosterola u dezmosterol. Za ovu redukciju potreban je i NADPH kao kofaktor i može uključivati aktivnost citohrom-P450 oksidoreduktaze. Takođe se smatra da sadrži gvožđe.[1] DHCR7 je integralni membranski protein endoplazmatskog retikuluma, a kompjuterski modeli su predvideli do devet transmembranskih domena. DHCR7 je najefikasniji u redukciji 7DHC, ali je poznato da smanjuje dvostruku vezu ugljika 7 drugih sterola, što ukazuje na raspon specifičnost supstrata. Predviđa se da ljudska verzija ovog enzima ima molekulsku težinu od 54,489 kDa i izoelektričnu tačku od 9,05.[1]
Predviđa se da sekvenca ostataka koju kodira DHCR7 sadrži 475 aminokiselina, kao i nekoliko proteinskih motiva. Sadrži više motiva sterol-reduktaza, kao što bi se očekivalo s obzirom na njegovu funkciju. Sadrži potencijalni sterolni domen (SSD), čija je funkcija nepoznata, ali se smatra da je neophodna za vezivanje sterolnih supstrata. Također obuhvata višestruka mesta fosforilacije, uključujući potencijalna mjeste protein-kinaza C i tirozin-kinaza (regulatorni enzimi odgovorni za fosforilaciju). Tačna funkcija fosforilacija DHCR7 još nije poznata, ali se smatra da je uključena u regulaciju njegove aktivnosti.[1]
Mutacije i incidencija
urediSLOS je autosomni recesivni poremećaj.[5] Identificirano je više od 130 različitih tipova mutacija.[2] Misens mutacija (promjena jedne nukleotide koja rezultira kodom za drugu aminokiselinu) su najčešće, čineći 87,6 % SLOS spektra. Obično smanjuju funkciju enzima, ali je ne moraju potpuno inhibirati. Mnogo ovisi o prirodi mutacije (tj. koja je aminokiselina zamijenjena i gdje i kojom). Nulte mutacije su mnogo rjeđe, koje proizvode ili potpuno nefunkcionalan enzim ili ga uopće nemaju.[5] Dakle, misens mutacije mogu biti češće općenito jer su manje smrtonosne nego nonsens mutacije.
IVS8-1G>C je najčešće prijavljivana mutacija u DHCR7. Ovo ometa spajanje eksona osam i devet i rezultira umetanjem 134 nukleotida u transkript DHCR7. Ovo je nonsens mutacija, tako da su pacijenti koji su homozigotni za ove alele ozbiljno pogođeni. Smatra se da se ova mutacija prvi put dogodila na Britanskim otocima i da ima nositelja (oni koji su heterozigotni za alele, ali nisu zahvaćeni) oko 1,09 % za kavkazoide evropske baštine. Učestalost mutacija se razlikuje za različite etničke grupe, ovisno o porijeklu mutacije. U svim populacijama kavkaskih podrasa, ova određena mutacija ima procijenjenu frekvenciju nositelja od 3%.[1]
Sljedeća najčešća mutacija je 278C >T, koja rezultira treoninom na poziciji aminokiseline 93. To je misens mutacija i obično je povezana sa manje ozbiljnim simptomima. Ova mutacija je najčešća kod pacijenata [[Italija|italijanskog, kubanskog i mediteranskog porijekla.[1] Treća najčešća mutacija je 452G >A. Ova nonsens mutacija uzrokuje terminaciju proteina, tako da se ne bi formirao enzim DHCR7. Smatra se da je nastao u južnoj Poljskoj i da je najčešći u sjevernoj Evropi.[6]
Ostale mutacije su manje uobičajene, iako se čini da više ciljaju na određene proteinske domene od drugih. Naprimjer, motivi sterol-reduktaze su uobičajena mjesta mutacije.[1] Sveukupno, postoji procijenjena frekvencija nositelja (za bilo koju mutaciju DHCR7 koja uzrokuje SLOS) od 3-4% u populaciji kavkazoida (tj. rjeđi je među azijskim i afričkim populacijama.[7]). Ovaj broj ukazuje na hipotetsko rođenje incidencija između 1/2500 i 1/4500. Međutim, izmjerena incidencija je između 1/10.000 do 1/60.000 (razlikuje se u zavisnosti od naslijeđa i porijekla).[5] Ovo je mnogo niže od očekivanog. Ukazuje na to da su mnogi slučajevi SLOS-a neotkriveni i vjerovatno su posljedica ili spontanog pobačaja uzrokovanog teškim mutacijama (pobačaj) ili blagih slučajeva koji nisu dijagnosticirani. Žene nemaju karakteristične genitalne malformacije koje imaju muškarci, pa je manja vjerovatnoća da će biti ispravno dijagnosticirana.[7]
Patogeneza
urediS obzirom da funkcija holesterola obuhvata vrlo širok raspon, malo je vjerovatno da su simptomi SLOS-a posljedica jednog molekulskog mehanizma. Neki od molekulskih efekata još nisu poznati, ali bi se mogli ekstrapolirati na osnovu uloge holesterola. Općenito, negativni efekti su uzrokovani sniženim nivoima holesterola i povećanim nivoima prekursora holesterola – prije svega, 7DHC. Iako je 7DHC strukturno sličan holesterolu, a potencijalno bi mogao djelovati kao zamjena, efekti ovoga se još uvijek proučavaju.[2] Većina pacijenata sa SLOS ima snižene nivoe holesterola, posebno u mozgu (gde se nivoi holesterola prvenstveno oslanjaju na novu sintezu). To također znači da bi svi sterolni derivati kolesterola također imali smanjene koncentracije. Naprimjer, smanjeni nivoi neuosteroida mogu se vidjeti u SLOS-u. To su lipidi koji učestvuju u signaliziranju unutar mozga i moraju se proizvoditi u samom mozgu. Oni su odgovorni za interakciju sa jedarnim steroidnim receptorima i vezuju se za neurotransmiter-zavisne onske kanale. Konkretno, oni moduliraju efekte receptora GABA i NMDA, što rezultira umirujućim efektima, poboljšanom memorijom i još mnogo toga. Dakle, s obzirom da su neke karakteristike SLOS-a suprotne od ovih efekata (hiperaktivnost, anksioznost), smanjenje neurosteroida moglo bi uticati i na neurološki razvoj i na ponašanje.[8]
Nadalje, kao što je gore navedeno, holesterol je važan aspekt u signalizaciji zvučnog ježa. Sa nižim nivoom holesterola, proteini ježa ne bi bili podvrgnuti neophodnoj kovalentnoj modifikaciji i naknadnoj aktivaciji. To bi rezultiralo poremećenim embrionskim razvojem i moglo bi doprinijeti uočenim fizičkim urođenim defektima u SLOS-u. Jedan određeni signalni protein ježa, sonični jež (SHH), važan je u obrascu centralnog nervnog sistema, crtama lica i udovima.[9] Drugi proteini ježa mogu biti uključeni u razvoj genitalnog trakta i skeleta.[10]
Promijenjeni nivoi sterola u SLOS-u posebno su relevantni za ćelijske membrane, koje su prvenstveno napravljene od lipida. Pacijenti sa SLOS-om mogu pokazati ćelijske membrane sa abnormalnim svojstvima ili sastavom, a smanjeni nivoi holesterola uveliko utiču na stabilnost i proteine lipidnih splavova.[2] Uprkos njihovoj strukturnoj sličnosti, 7DHC nije u stanju da učini tako da zamijeni holesterol u lipidnim splavovima.<.[11] Osim toga, nedostatak holesterola doprinosi povećanju fluidnosti ćelijske membrane i može uzrokovati abnormalne granulskee sekrecije.[4] Sve ove promjene u membranama vjerovatno doprinose promjenama u transportnim funkcijama koje se primjećuju u SLOS. One mogu uzrokovati defekte u degranulaciji IgE mastocita posredovanoj receptorima i proizvodnji citokina, a to su ćelije uključene u alergijske i imunske odgovore.[2] Pogođen je NMDA receptor, kao i sposobnost vezivanja hipokampusnog serotoninskog receptora.[12] Interakcija između ćelije i ćelije] , koja je veoma važna u razvoju, može biti poremećena.[3] Pokazalo se da je egzocitoza u sinapsnim vezikulama smanjena, vjerovatno zbog oštećenja fuzija vezikula sa ćelijskom membranom ili loša reciklaža vezikula.[13] Konačno, holesterol je visoko rasprostranjen u mijelinu, zbog čega pacijenti sa SLOS-om pokazuju smanjenu mijelinizaciju moždane hemisfere, perifernih nerava i glavenih nerava.[8]
Pored sniženog nivoa holesterola, mnogi simptomi prikazani u SLOS-u potiču od toksičnih efekata 7DHC. Poznato je da 7DHC ometa unutarćelijski transport holesterola. Također povećava razgradnju HMG-CoA reduktaze (enzim koji katalizira korak koji ograničava brzinu u sintezi holesterola). 7DHC dovodi do novih derivata oksisterola i steroida, a mnoge njihove funkcije ili efekti još uvijek su nepoznati.[2] Vrlo važan nalaz u vezi sa 7DHC je da je najreaktivniji lipid za lipidnu peroksidaciju i rezultira sistemskim oksidativnim stresom. Poznato je da lipidna peroksidacija uništava ćelijske membrane i organele vezane za membranu. Derivat 7DHC koji se koristi za indikaciju oksidativnog stresa je 3β,5α-dihidroksi-holest-7-en-6-on (DHCEO) nastaje iz primarnog produkta 7DHC peroksidacije, 7-DHC-5α,6α-epoksida. DHCEO je toksičan za korteksne neuronske i glijne ćelije i ubrzava njihovu diferencijaciju i arborizaciju.[14] Zbog oksidativnog stresa, smatra se da je 7DHC odgovoran za povećanu fotosenzitivnosti prikazanu kod pacijenata sa SLOS-om. Normalno izlaganje UVA zračenju može dovesti do oksidativnog stresa u ćelijama kože. S obzirom na to da se 7DHC lakše oksidira, on pojačava efekte UVA, što dovodi do povećane oksidacije membranskih lipida i povećane proizvodnje reaktivnih vrsta kisika (ROS).[11]
Tipski, više izmijenjeni nivoi 7DHC i holesterola dovode do težih simptoma SLOS-a. Nivoi ovih metabolita također odgovaraju ozbiljnosti mutacije (nonsens nasuprot misens); neke mutacije DHCR7 i dalje mogu pokazivati sintezu rezidualnog holesterola, a druge možda ne. Međutim, čak i osobe s istim mutacijama ili genotipom mogu i dalje pokazati varijabilnost u svojim simptomima. Ovo može biti uzrokovano faktorima majke, kao što je prijenos holesterola na fetus tokom trudnoće, kao i količina holesterola prisutnog u mozgu prije nego što se krvno-moždana barijera formira prenatalno. Brzina akumulacije i izlučivanja toksičnih metabolita može varirati od osobe do osobe. Majčinski apolipoprotein E je također impliciran u individualnu varijabilnost u SLOS-u, iako je tačna priroda ovog odnosa nepoznata.[5] Vjerovatno postoji više faktora koji doprinose širokom spektru efekata u SLOS-u koji imaju još nije otkriveno djelovanje.
Liječenje
urediUpravljanje pojedincima sa SLOS-om je složeno i često zahtijeva tim stručnjaka. Neke od kongenitalnih malformacija (rascjep nepca) mogu se ispraviti operacijom.[7] Drugi tretmani tek treba biti dokazani uspješnim u randomiziranim studijama, međutim anegdotskim se čini da uzrokuju poboljšanja.
Suplementacija holesterola
urediZa sada, najčešći oblik liječenja SLOS-a uključuje dodatak holesterolu u ishrani.[15] Anegdotski izvještaji pokazuju da ovo ima neke prednosti; može rezultirati povećanim rastom, nižom razdražljivosti, poboljšanom društvenošću, manje samopovređivanjem, manje taktilne odbrane, manjim brojem infekcija , više mišićnog tonusa, manje fotoosjetljivosti i manje autističkih ponašanja.[16] Suplementacija holesterola počinje sa dozom od 40–50 mg/kg/dan, povećavajući se po potrebi. Primjenjuje se ili konzumiranjem hrane s visokim sadržajem holesterola (jaja, vrhnje, jetra) ili kao prečišćeni holesterol za hranu. Mlađoj djeci i dojenčadima može biti potrebno hranjenje putem sonde.[3] Međutim, holesterol u ishrani ne smanjuje nivoe 7DHC, a ne može preći krvno-moždanu barijeru i ne čini se da se poboljšava razvojni ishod.[16] Jedna empirijska studija pokazala je da suplementacija holesterolom nije poboljšala razvojno kašnjenje, bez obzira na dob u kojoj je počela. Ovo je vjerovatno zato što većina kašnjenja u razvoju potiče od malformacija mozga, koji holesterol u ishrani ne može poboljšati zbog nemogućnosti da pređe krvno-moždanu barijeru.[17] thumb|right|350px| Simvastatin je inhibitor HMG-CoA reduktaze i koristi se za liječenje SLOS.
Genetički modeli
urediGenetički modeli SLOS-a stvoreni su putemnokaut gena DHCR7. Jedna studija je koristila homolognu rekombinaciju da poremeti DCHR7 u mišjim embrionskim matičnim ćelijama. Slično onome što je pronađeno kod ljudi, heterozigotni miševi (koji imaju samo jedan mutirani alel) bili su fentotipski normalni i ukršteni su da bi se dobili homozigotni mladi (mladi miševi) za mutirani alel. Iako su ovi umrli u prvom danu života zbog nemogućnosti da se hrane, pokazali su karakteristike slične ljudima sa SLOS-om. Imali su smanjen nivo holesterola, povećan nivo 7- i 8DHC, pokazali su manji rast i manju porođajnu težinu, imali su kraniofacijalne malformacije i manje pokreta. Mnogi su takođe imali rascjep nepca i smanjene neuronske reakcije na glutamat. Sve u svemu, imali su manje dismorfnih osobina od ljudskih pacijenata sa SLOS-om; nisu imali malformacije ekstremiteta, bubrega, nadbubrežne žlijezde ili centralnog nervnog sistema. Ovo se objašnjava činjenicom da kod glodara majčin holesterol može proći posteljicu, i zapravo je neophodan za razvoj fetusa. Kod ljudi se vrlo malo majčinog holesterola prenosi na fetus. Ukratko, genetički model miša od pomoći je da se objasni neuropatofiziologija SLOS-a.[18]
Eponim
urediSindrom je imenovan po Davidu Weyheu Smithu (1926-1981), američkom pedijatru; Lucu Lemliju (1935–?), belgijskom ljekaru i Johnu Mariusu Opitzu (1935–?), njemačko-američkom ljekaru. Ovo su istraživači koji su prvi opisali simptome SLOS-a.[19]
Reference
uredi- ^ a b c d e f g h i j Correa-Cerro, Lina S.; Porter, Forbes D. (2005). "3β-Hydroxysterol Δ7-reductase and the Smith–Lemli–Opitz syndrome". Molecular Genetics and Metabolism. 84 (2): 112–26. doi:10.1016/j.ymgme.2004.09.017. PMID 15670717.
- ^ a b c d e f Porter, Forbes D (2008). "Smith–Lemli–Opitz syndrome: Pathogenesis, diagnosis and management". European Journal of Human Genetics. 16 (5): 535–41. doi:10.1038/ejhg.2008.10. PMID 18285838.
- ^ a b c d e Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomSLOS novel met - ^ a b Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomSLOS recenzija - ^ a b c d Yu, H; Patel, SB (2005). "Recent insights into the Smith-Lemli-Opitz syndrome". Clinical Genetics. 68 (5): 383–91. doi:10.1111/j.1399-0004.2005.00515.x. PMC 1350989. PMID 16207203.
- ^ Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomDHCR7 i SLOS - ^ a b c Nowaczyk, Malgorzata JM (20. 6. 2013). "Smith-Lemli-Opitz Syndrome". u Pagon, Roberta A; Adam, Margaret P; Bird, Thomas D; Dolan, Cynthia R; Fong, Chin-To; Smith, Richard JH; Stephens, Karen (ured.). GeneReviews. National Library of Medicine. Pristupljeno 5. 12. 2013.
- ^ a b Marcos, Josep; Guo, Li-Wei; Wilson, William K; Porter, Forbes D; Shackleton, Cedric (2004). "The implications of 7-dehydrosterol-7-reductase deficiency (Smith–Lemli–Opitz syndrome) to neurosteroid production". Steroids. 69 (1): 51–60. doi:10.1016/j.steroids.2003.09.013. PMID 14715377. S2CID 900728.
- ^ Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomSLOS pregled - ^ Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomSLOS roman met - ^ a b Valencia, Antonio; Rajadurai, Anpuchchelvi; Carle, A. Bjorn; Kochevar, Irene E. (2006). "7-Dehydrocholesterol enhances ultraviolet A-induced oxidative stress in keratinocytes: Roles of NADPH oxidase, mitochondria, and lipid rafts". Free Radical Biology and Medicine. 41 (11): 1704–18. doi:10.1016/j.freeradbiomed.2006.09.006. PMC 1880892. PMID 17145559.
- ^ Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomserotonin - ^ Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomvesicula - ^ Korade, Zeljka; Xu, Libin; Mirnics, Karoly; Porter, Ned A. (2012). "Lipid biomarkers of oxidative stress in a genetic mouse model of Smith-Lemli-Opitz syndrome". Journal of Inherited Metabolic Disease. 36 (1): 113–22. doi:10.1007/s10545-012-9504-z. PMC 3674764. PMID 22718275.
- ^ Wassif, Christopher A.; Krakowiak, Patrycja A.; Wright, Brooke S.; Gewandter, Jennifer S.; Sterner, Allison L.; Javitt, Norman; Yergey, Alfred L.; Porter, Forbes D. (2005). "Residual cholesterol synthesis and simvastatin induction of cholesterol synthesis in Smith–Lemli–Opitz syndrome fibroblasts". Molecular Genetics and Metabolism. 85 (2): 96–107. doi:10.1016/j.ymgme.2004.12.009. PMID 15896653.
- ^ a b Correa-Cerro, L. S.; Wassif, CA; Kratz, L; Miller, GF; Munasinghe, JP; Grinberg, A; Fliesler, SJ; Porter, FD (2006). "Development and characterization of a hypomorphic Smith-Lemli-Opitz syndrome mouse model and efficacy of simvastatin therapy". Human Molecular Genetics. 15 (6): 839–51. doi:10.1093/hmg/ddl003. PMID 16446309.
- ^ Sikora, Darryn M; Ruggiero, Mark; Petit-Kekel, Kersti; Merkens, Louise S; Connor, William E; Steiner, Robert D (2004). "Cholesterol supplementation does not improve developmental progress in Smith-Lemli-Opitz syndrome". The Journal of Pediatrics. 144 (6): 783–91. doi:10.1016/j.jpeds.2004.02.036. PMID 15192627.
- ^ Wassif, C. A.; Zhu, P; Kratz, L; Krakowiak, PA; Battaile, KP; Weight, FF; Grinberg, A; Steiner, RD; Nwokoro, NA; Kelley, RI; Stewart, RR; Porter, FD (2001). "Biochemical, phenotypic and neurophysiological characterization of a genetic mouse model of RSH/Smith-Lemli-Opitz syndrome". Human Molecular Genetics. 10 (6): 555–64. doi:10.1093/hmg/10.6.555. PMID 11230174.
- ^ Smith, David W.; Lemli, Luc; Opitz, John M. (1964). "A newly recognized syndrome of multiple congenital anomalies". The Journal of Pediatrics. 64 (2): 210–7. doi:10.1016/S0022-3476(64)80264-X. PMID 14119520.
Ovaj članak uključuje materijal u javnom vlasništvu sa Nacionalna medicinska biblioteka Sjedinjenih Američkih Država dokument: "Genetics Home Reference".