Norepinefrin
Noradrenalin (NA) ili norepinefrin (NE) je organski spoj u porodici kateholamina, koji funkcionira u mozgu i tijelu kao hormon i neurotransmiter. Naziv "noradrenalin", izveden iz latinskih korijena što znači "pored / pored bubrega", češće se koristi u Velikoj Britaniji i većem dijelu ostalih evropskih zamalja, uključujući i Balkan. U Sjedinjenim Državama se obično preferira „norepinefrin“, izveden iz grčkih korijena koji imaju isto značenje.[1]"Norepinefrin" je takođe međunarodno nevlasničko ime norepinefrin.[2] Bez obzira koje se ime koristi za samu tvar, dijelovi tijela koji je stvaraju ili na nju utiču nazivaju se "noradrenergični" ili noradrenergni.
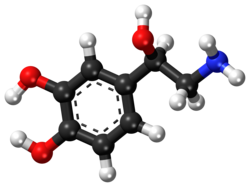
| Noradrenalin | |
|---|---|
 | |
| Općenito | |
| Hemijski spoj | Noradrenalin |
| Druga imena | (R)-(–)-Norepinefrin, |
| Molekularna formula | C8H11NO3 |
| CAS registarski broj | 51-41-2 |
| InChI | 1S/C8H11NO3/c9-4-8(12)5-1-2-6(10)7(11)3-5/h1-3,8,10-12H,4,9H2/t8-/m0/s1 |
| Osobine1 | |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
Opća funkcija norepinefrina je mobiliziranje mozga i tijela za djelovanje. Otpuštanje norepinefrina je najniže za vrijeme spavanja, povećava se tokom budnosti i dostiže mnogo više razine za vrijeme stresa ili opasnosti, u takozvanoj reakciji odgovor na borbu ili bijeg. U mozgu, norepinefrin povećava uzbuđenje i budnost, podstiče budnost, pojačava formiranje i pronalaženje pamćenja i usredotočuje pažnju; također povećava nemir i anksioznost. U ostatku tijela norepinefrin povećava broj otkucaja srca i krvni pritisak, aktivira oslobađanje glukoze iz zaliha energije, povećava protok krvi do skeletnih mišića , smanjuje protok krvi u gastrointestinalnom sistemu, te sprečava pržnjenje mokraćnog mjehura ipokretljivost u gastrointestinalnom sistemu.
U mozgu se noradrenalin proizvodi u jezgrima koja su mala, ali imaju snažne efekte na druga područja mozga. Najvažnija od ovih jezgara je locus coeruleus, koja se nalazi u ponsu. Izvan mozga, norepinefrin se koristi kao neurotransmiter simpatičke simpatičke ganglije koji se nalazi u blizini kičmene moždine ili u trbuhu, a također se oslobađa izravno u krvotok iz nadbubrežnih žlijezda. Bez obzira na to kako se i gdje oslobađa, norepinefrin djeluje na ciljne ćelije vezanjem i aktiviranjem adrenergnih receptora koji se nalaze na površini ćelije.
Različiti medicinski važni lijekovi djeluju mijenjanjem djelovanja noradrenalinskih sistema. Noradrenalin se široko koristi kao lijek za ubrizgavanje u liječenju kritično niskog krvnog pritiska. Beta blokatori, koji suzbijaju neke od efekata noradrenalina, blokirajući njihove receptore, često se koriste za lečenje glaukoma, migrene i niza kardiovaskularnih problema. Alfa blokatori, koji suzbijaju različit skup efekata noradrenalina, koristi se za liječenje nekoliko kardiovaskularnih i psihijatrijskih stanja. Agonisti alfa-2 često imaju efekt sediranja i obično se koriste kao sredstva za poboljšanje anestezije u hirurgiji, kao i u liječenju zavisnosti od lijekova ili zavisnosti od alkohola. Mnogi važni psihijatrijski lijekovi vrše snažne efekte na noradrenalinske sisteme u mozgu, što rezultira nuspojavama koje mogu biti korisne ili štetne.
Struktura
urediNoradrenalin je kateholamin i fenetilamin.[3] Njegova struktura razlikuje se od strukture epinefrina samo po tome što epinefrin ima metilnu grupu vezanu za njegov dušik, dok je u norepinefrinu metilna grupa zamijenjena atomom vodika. Prefiks nor- izveden je kao kratica riječi "normalno", koja se koristi za označavanje demetiliranog. spoja.[4]
Biohemijski mehanizmi
urediBiosinteza
urediU ljudskom tijelu, norepinefrin se sintetizira iz dopamina pomoću enzima dopamin β-hidroksilaza (DBH).
Norepinefrin ae sintetizira iz aminokiseline tirozin nizom enzimskih koraka u srži nadbubrežne žlijezde i postganglijskim neuronima simpatičkog nervnog sistema. Dok se pretvorba tirozina u dopamin odvija pretežno u citoplazmi, pretvaranje dopamina u norepinefrin pomoću dopamin β-monooksigenaza odvija se pretežno unutar neurotransmiterske vezikule.[5] Metabolički put je:
- Fenilalanin → Tirozin → L-DOPA → Dopamin → Norepinefrin[5]
Stoga je direktni prekursor norepinefrina dopamin, koji se sintetizira posredno iz esencijalne aminokiseline fenilalanin ili neesencijalne aminokiseline tirozin.[5] Ove aminokiseline nalaze se u gotovo svakom proteinu i kao takve obezbeđuju se unosom hrane koja sadrži proteine, a tirozin je najčešći.
Fenilalanin se pretvara u tirozin enzimom fenilalanin hidroksilaza, s molekulskim [[kisik]om]] (O2)i tetrahidrobiopterinom kao kofaktorom. Tirozin se pretvara u L-DOPA- enzimom tirozin hidroksilaza, sa tetrahidrobiopterinom, O2 i vjerovatno gvožđem (Fe2+) kao kofaktorima.[5] L-DOPA se pretvara u dopamin enzimom aromatskaL-aminokiselinska dekarboksilaza (poznata i kao DOPA dekarboksilaza), sa piridoksal-fosfatom kao kofaktorom.[5] Dopamin se enzimom dopamin β-monooksigenaza (ranije poznat kao dopamin β-hidroksilaza ) pretvara u norepinefrin s O2 i askorbinskom kiselinom kao kofaktorima.[5]
Sam Norepinefrin može se dalje pretvoriti u epinefrin enzimom feniletanolamin N -metiltransferaza sa S-adenozil-L-metioninom kao kofaktorom.[5]
Degradacija
urediKod sisara, norepinefrin se brzo razgrađuje do različitih metabolita. Početni korak u raspadu može katalizirati bilo koji od enzima monoamin-oksidaza (uglavnom monoamin-oksidaza A) ili COMT.[6] Odatle se razlaganje može nastaviti raznim putevima. Glavni krajnji proizvodi su ili vanililmandelinska kiselina ili konjugirani oblik MHPG, za koje se smatra da su oba biološki neaktivni i izlučuju se mokračom.[7]
Funkcije
urediĆelijski efekti
uredi| Porodica | Receptor | Tip | Mehanizam |
|---|---|---|---|
| Alfa | α1 | Gq-spregnuti | Porast IP3 i kalcija aktiviranjem enzima fosfolipaza C. |
| α2 | Gi/Go-spregnuti | Smanjene cAMP inhibiranjem enzima adenilat-ciklaza. | |
| Beta | β1 | Gs-spregnuti | Povećanje cAMP aktivacijom enzima adenilat-ciklaza. |
| β2 | |||
| β3 |
Skladištenjenje, oslobađanje i ponovno preuzimanje
urediUnutar mozga, norepinefrin funkcionira kao neurotransmiter, a kontrolira ga skup mehanizama koji su zajednički svim monoaminskim neurotransmiterima . Nakon sinteze, norepinefrin se transportuje iz citosol u sinapsne vezikule vazikulskog transportema monoamina (VMAT).[8] Norepinefrin se čuva u tim vezikulama sve dok se ne izbaci u sinapsni rascjep, obično nakon što potencijal djelovanja uzrokuje da vezikule izbace njihov sadržaj izravno u sinagopsku hemijsku sinapsu u procesu zvanom egzocitoza.
Jednom kada dođe u sinapsu, norepinefrin se veže i aktivira receptore. Nakon akcijskog potencijala, molekule norepinefrina brzo se nepovezuju sa njihovim receptorima. Zatim se apsorbiraju natrag u presinapsnu ćeliju, putem ponovnog preuzimanja posredovanog prvenstveno norepinefrin-transporterom (NET).[9] Kada se vrati u citosol, norepinefrin se može razgraditi pomoću monoamin-oksidaze ili ih prepakivati u vezikule VMAT, čineći ga dostupnim za buduće oslobađanje.[8]
Simpatički nervni sistem
urediNorepinefrin/noradrenalin je glavni neurotransmiter simpatičkog nervnog sistema, a sastoji se od oko dvije desetine simpatičkih lanaca ganglija smještenih pored kičmene moždine, plus skup pršljenskih ganglija koji se nalazi u grudnom košu i trbuhu.[10] Ove simpatičke ganglije povezane su s brojnim organima, uključujući oči, pljuvačne žlijezde, srce, pluća, jetru, žučni mjehur, želudac, crijeva, bubrege, mokraćni mjehur, reproduktivne organe, mišiće, kožu i nadbubrežne žlijezde.[10] Simpatička aktivacija nadbubrežne žlezde uzrokuje da se dio zvani kora nadbubrežne žlijezde oslobađa noradrenalin (kao i epinefrin) u krvotok, odakle, funkcionirajući kao hormon, dobija daljnji pristup širokom rasponu tkiva.[10]
Općenito govoreći, učinak noradrenalina na svaki ciljni organ je da modificira njegovo stanje tako što ga čini pogodnijim za aktivno kretanje tijela, često uz cijenu povećane potrošnje energije i povećanog trošenja i habanja.[11] Ovo se može usporediti s acetilholinom posredovanim efektima parasimpatičkog nervnog sistema, koji većinu istih organa modificira u stanje pogodnije za odmor, oporavak i probavu hrane i obično manje skupo, u smislu potrošnje energije.[11]
Simpatički efekti norepinefrina/noradrenalina uključuju:
- U očima se povećava produkcija suza, čime oči postaju vlažnije ,[12] i širi zjenice kontrakcijom dilatatora šarenice.
- U srcu povećaa vkoličinu ispumpane krvi.[13]
- U smeđem masnom tkivu povećava se sagorijevanje kalorija koje stvaraju tjelesnu toplinu (termogeneza).[14]
- Multipli efekti zahvataju imunski sistem. Simpatički nervni sistem je primarni put interakcije imunoskog sistema i mozga, a nekoliko komponenti prima simpatički unos, uključujući timus, slezinu i limfne čvorove . Međutim, efekti su složeni, pri čemu se neki imunski procesi aktiviraju, dok su drugi inhibirani.[15]
- U arterijama sužava krvne sudove, uzrokujući porast krvnog pritiska.[16]
- U bubrezima, otpušta renin i zadržavanje natrija u krvotoku.[17]
- U jetri povećanje proizvodnje glukoze, bilo glikogenolizom nakon obroka, bilo lukoneogenezom kada se hrana nedavno nije konzumirala. Glukoza je glavni energetski izvor tijela u većini uvjeta.
- U gušterači, pojačano je oslobađanje glukagona, hormona čiji je glavni učinak povećavanje proizvodnje glukoze u jetri.[17]
- keletnim mišićima raste unos glukoze.[17]
- U masnom tkivu (tj. masnim ćelijama) dolazi do povećanja lipolize, odnosno pretvaranja masti u tvari koje mišići i druga tkiva mogu direktno koristiti kao energente.[17]
- U želucu i crevima, smanjuju se probavne aktivnosti. Ovo je rezultat opšte inhibicijskog učinka norepinefrina na crijevni nervni sistem, uzrokujući smanjenje pokretljivosti gastrointestinalnog trakta, protoka krvi i izlučivanja probavnih supstanci.[18]
Noradrenalin i ATP su simpatički koneurotransmiteri. Utvrđeno je da endokanabinoid, anandamid, kanabinoid Noradrenaline i WIN 55,212-,2 mogu izmijeniti cjelokupni odgovor na stimulaciju simpatičkog nerva i naznačiti da predspojni CB1 receptori posreduju jelovanja stimulacija – inhibicija. Stoga kanabinoidi inhibiraju i noradrenerginske i purinergičnske komponente simpatičke neurotransmisije.[19]
Centralni nervni sistem
urediNoradrenergni neuroni u mozgu tvore neurotransmiterski sistem koji, kada se aktivira, utiče na velike površine mozga. Efekti se manifestuju u budnosti, uzbuđenju i spremnosti za akciju.
Noradrenergnih neurona (tj. neuroni čiji je primarni neurotransmiter noradrenalin/norepinefrin) relativno je mali broj, a njihova ćelijska tijela su ograničena na nekoliko relativno malih područja mozga, ali šalju projekcije na mnoga druga područja mozga i vrše snažne efekte na njihove mete. Ove noradrenergične ćelijske grupe prvi put su mapirali Annica Dahlström i Kjell Fuxe, 1964., koji su im dodijelili oznake počevši sa slovom "A" (za "aminergično").[20] U njihovoj shemi područja A1 do A7 sadrže neurotransmiter noradrenalin (A8 do A14 sadrže dopamin). Noradrenergička ćelijska grupa A1 nalazi se u repnom ventrolateralnom dijelu medulena i ima ulogu u kontroli metabolizma tjelesnih tekućina.[21] Noradrenergička ćelijska grupa A2 nalazi se u području mozga nazvanom solitarno jezgro; ove ćelije su bile aktivirane u različite reakcije, uključujući kontrolu unosa hrane i reakcije na stres.[22] Ćelijske grupe A5 i A7 projiciraju se uglavnom na kičmenu moždinu.[23]
Najvažniji izvor noradrenalina u mozgu je locus coeruleus LC), koji sadrži noradrenergičku ćelijsku grupu A6 i pridružuje se ćelijskoj grupi A4. Locus coeruleus je prilično mali u apsolutnom smislu – za primate se procenjuje da sadrže oko 15.000 neurona, manje od jednog miliona neurona u mozgu – ali šalje projekcije na svaki veći deo mozga, pa i na kičmenu moždinu.[24]
Razina aktivnosti u locus coeruleus (LC) u velikoj mjeri povezana je s budnošću i brzinom reakcije. Njegova aktivnost je niska za vrijeme spavanja i pada na gotovo ništa tokom stanja REM (snova).[25] Kreće se ka početnoj razini za vrijeme budnosti, ali se privremeno povećava kada je osoba pobuđena bilo kakvim podražajem koji privlači pažnju. Neprijatni podražaji kao što su bol, otežano disanje, distezija mokraćnog mjehura, vrućina ili hladnoća povećavaju porast. Izuzetno neugodna stanja poput intenzivnog straha ili intenzivnog bola povezana su s vrlo visokim nivoima njegove aktivnosti.[24]
Noradrenalin koji oslobađa locus coeruleus (LC) utiče na funkciju mozga na više načina. Pojačava obradu senzornih ulaza, pojačava pažnju, pospješuje formiranje i pronalaženje dugotrajne i radne memorije i povećava sposobnost mozga da reagira na ulaze mijenjajući obrazac aktivnosti u predfrontalnom korteksu i drugim područjima.[26] Kontrola razine uzbuđenja je dovoljno jaka da suzbijanje LC izazvano lijekovima ima snažan efekt sediranja.[25]
Velika je sličnost između situacija koje aktiviraju locus coeruleus u mozgu i one koje aktiviraju simpatički živčani sistem na periferiji: locus coeruleus u osnovi mobilizira mozak za djelovanje dok simpatički sistem mobilizira tijelo. Tvrdi se da ova sličnost nastaje zato što su oba u velikoj mjeri pod kontrolom istih moždanih struktura, posebno dijela mozga nazvanog nucleus gigantocellularis.[24]
Farmakologija
urediVeliki broj važnih lijekova ispoljava svoje djelovanje interakcijom s norepinefrinskim sistemima u mozgu ili tijelu. Njihove primjene uključuju liječenje kardiovaskularnih problema, šoka i raznih psihijatrijskih stanja. Ovi lijekovi se dijele na: simpatomimetički lijek koji oponašaju ili pojačavaju barem neke od učinaka norepinefrina koji oslobađa simpatički nervni sistem; simpatilitički lijekovi, nasuprot tome, blokiraju barem neke od efekata.[27] Both of these are large groups with diverse uses, depending on exactly which effects are enhanced or blocked.[27]
Sam Norepinefrin klasificiran je kao simpatomimetički lijek: njegovi učinci kada se daju intravenskim ubrizgavanjem povećavajući broj otkucaja srca i sile i sužavanje krvnih žila čine ga vrlo korisnim za liječenje hitnih slučajeva koji uključuju kritično nizak krvni prizisak.[27] Proizvođasč Surviving Sepsis Campaign preporučio je norepinefrin kao sredstvo prve linije u liječenju sepsnog šoka koji ne reagira na oživljavanje tekućinom, dopunjen vazopresin om i epinefrinom. Upotreba dopamina ograničena je samo na vrlo odabrane pacijente.[28]
Beta blokatori
urediOvo su simpatilitski lijekovi koji blokiraju efekte adrenergičkih receptora, a imaju mali ili nikakav efekat na alfa receptore. Oni se ponekad koriste za liječenje visokog krvnog pritiska, pretkomorne fibrilacije i kongestivnog zatajenja srca, ali nedavni pregledi zaključuju da su druge vrste lijekova obično superiorni u te svrhe.[29][30] Beta blokatori mogu biti održiv izbor za druga kardiovaskularna stanja, uključujući anginu i Marfanov sindrom.[31] > Također se široko koriste za liječenje glaukoma, najčešće u obliku kapljica za oči.[32] Zbog svojih učinaka u smanjenju simptoma anksioznosti i drhtavice, ponekad ih zabavljači, javni govornici i sportisti koriste za smanjenje anksioznosti, iako nisu medicinski odobreni u tu svrhu i zabranjeni su od strane Međunarodnog olimpijskog olimpijskog komiteta.[33][34]
Međutim, korisnost beta blokatora ograničena je nizom ozbiljnih nuspojava, uključujući usporavanje otkucaja srca, pad krvnog pritiska, astmu i reaktivnu hipoglikemiju.[32] Negativni efekti mogu biti posebno ozbiljnj kod ljudi koji pate od dijabetesa. .[29]
Alfa blokatori
urediOvo su simpatolitski lijekovi koji blokiraju efekte adrenergičkih alfa receptora, dok imaju mali ili nikakav učinak na beta receptore.[35] Lijekovi koji pripadaju ovoj grupi mogu imati vrlo različite efekte, ovisno o tome blokiraju li primarno alfa-1 receptore, alfa-2 receptore ili oboje. Alfa-2 receptori, kako je opisano na drugom mjestu u ovom članku, često su locirani na samim neuronima koji oslobađaju norepinefrin i na njih imaju inhibitorne efekte; posljedično, blokada alfa-2 receptora obično rezultira povećanjem oslobađanja norepinefrina.[35] Alpha-1 receptori obično se nalaze na ciljnim ćelijama i imaju pobudne efekte na njih; posljedično, blokada alfa-1 receptora obično rezultira blokiranjem nekih učinaka norepinefrina.[35] Lijekovi poput fentolamina, koji djeluju na obje vrste receptora, mogu proizvesti složenu kombinaciju oba efekta. U većini slučajeva kada se termin "alfa blokator" upotrebljava bez kvalifikacije, odnosi se na selektivni antagonist alfa-1.
Selektivni alfa-1 blokatori imaju različite namene. Kako je jedan od njihovih efekata inhibiranje kontrakcije glatkog mišića u prostati, često se koriste za liječenje simptoma benigne hiperplazije prostate.[36] Alfa-blokatori takođe pomažu ljudima da izbace bubrežne kamence.[37] Njihovi efekti na centralni nervni sistem čine ih korisnim za liječenje generaliziranog anksioznog poremećaja, paničnog poremećaja i postraumatskog stresnog poremećaja.[38] Međutim, mogu imati značajne nuspojave, uključujući pad krvnog pritiska.[35]
Neki antidepresivi djeluju dijelom kao selektivni alfa-2 blokatori, ali najpoznatiji lijek u toj klasi je johimbin, koji se ekstrahira iz kore afričke stablašice Pausinystalia johimbe.[39] Johimbin djeluje kao pojačavač muške potencije, ali njegova korisnost u tu svrhu je ograničena ozbiljnim nuspojavama uključujući anksioznost i nesanicu.[39] Predoziranje može uzrokovati opasno povećanje krvnog pritiska.[39] Johimbin je zabranjen u mnogim zemljama, a u Sjedinjenim Državama, zato što je ekstrahiran iz biljke, a ne hemijski sintetiziran, prodaje se iznad šanka (javno) kao dodatak prehrani.[40]
Alpha-2 agonisti
urediTo su simpatomimetski lijekovi koji aktiviraju alfa-2 receptore ili pojačavaju njihov efekat.[41] Budući da su alfa-2 receptori inhibitorni i mnogi su locirani presinapsno na ćelijama koje oslobađaju norepinefrin, neto efekat ovih lijekova je obično smanjenje količine oslobođenog norepinefrina.[41] Lijekovi iz ove skupine koji mogu ući u mozak često imaju snažne sedacijske efekte, uslijed inhibicijskog djelovanja na locus coeruleus. Naprimjer,[41] klonidin se koristi za tretman anksioznih poremećaja i nesanice, kao i prethodni sedativ za pacijente koji treba da se podvrgnu operaciji.[42] Ksilazin, još jedan lijek iz ove grupe, također je moćan sedativ i često se koristi u kombinaciji sa ketaminom, kao opći anestetik za veterinarsku hirurgiju,a u Sjedinjenim Državama nije odobren za upotrebu kod ljudi.[43]
Stimulansi i antidepresivi
urediTo su lijekovi za koje se smatra da posreduju u različitim neurotransmiternim sistemima: dopamin za stimulanse), serotonin za antidepresive, ali mnogi povećavaju razinu norepinefrina u mozgu.[44] Amfetamin, naprimjer, stimulans je koji povećava oslobađanje norepinefrina kao i dopamina.[45] Inhibitor monoamin oksidaze je antidepresiv koji inhibira metaboličku razgradnju norepinefrina, kao i serotonina i dopamina.[46] U nekim slučajevima teško je razlikovati učinke posredovane norepinefrinom od efekata povezanih s drugim neurotransmiterima.
Bolesti i poremećaji
urediBrojni važni medicinski problemi uključuju disfunkciju norepinefrinog sistema u mozgu ili tijelu.
Simpatička hiperaktivacija
urediHiperaktivacija simpatičkog nervnog sistema sama po sebi nije posebno prepoznato stanje, ali je sastavni dio niza drugih, kao i moguća posljedica uzimanja simpatikomimetskog lijeka. Izaziva izrazit skup simptoma, uključujući bolove, ubrzan rad srca, povišen krvni pritisak, znojenje, palpitacije, tjeskobu, glavobolju, bespomoćnost i pad glukoze u krvi. Ako se simpatička aktivnost povećava duže vrijeme, to može uzrokovati gubitak težine i druge promjene u tijelu povezane sa stresom.
Popis stanja koja mogu izazvati simpatičku hiperaktivaciju uključuje teške ozljede mozga,[47] oštećenja kičmene moždine,[48] otkazivanje srca,[49] visok krvni pritisak,[50] bolesti bubrega,[51] i različiti tipovi stresa.
Feohromocitom
urediFeohromocitom je tumor rijetke vrste (srži nadbubrežne žlijezde), izazvan bilo genetičkim faktorima ili određenim vrstama karcinoma. Posljedica toga je masivno povećanje količine norepinefrina i epinefrina ispuštenog u krvotok. Najočitiji simptomi su znaci simpatičke hiperaktivacije, uključujući naročito porast krvnog pritiska koji može dostići fatalnu razinu. Najefikasnije liječenje je hirurško uklanjanje tumora.
Stres
urediStres u fiziologiji znači svaku situaciju koja prijeti kontinuiranoj stabilnosti tijela i njegovih funkcija.[52] Stres utiče na širok raspon tjelesnih sistema: dva najčešće aktivirana su hipotalamsko-hipofizno-adrenalna osovina i norepinefrinski sistem, uključujući i simpatički nervni sistem i locus coeruleus – centriranog sistema u mozgu.[52] Stresori mnogih vrsta izazivaju porast noradrenergičke aktivnosti, koja mobilizira mozak i tijelo da odbije prijetnju.[52] Hronični stres, ako se nastavi dugo , može oštetiti mnoge dijelove tijela. Značajan dio štete je posljedica dugotrajnog oslobađanja norepinefrina zbog njegove opće funkcije u usmjeravanju resursa dalje od održavanja, regeneracije i reprodukcije te prema sistemima koji su potrebni za aktivno kretanje. Posljedice mogu uključivati usporavanje rasta (kod djece), besanicu, gubitak libida, gastrointestinalne probleme, oslabljenu otpornost na bolesti, sporije stope zacjeljivanja ozljeda, depresiju i povećanu ranjivost na ovisnost.[52]
ADHD
urediPoremećaj hiperaktivnosti i deficita pažnje je psihijatrijsko stanje koje uključuje probleme sa pažnjom, hiperaktivnost i impulzivnost.[53] Najčešće se liječi upotrebom stimulanase kao što je metilfenidat (Ritalin), čiji je osnovni efekat povećanje razine dopamina u mozgu, ali lijekovi iz ove grupe uglavnom povećavaju razinu norepinefrina i bilo je teško utvrditi uključuju li ti postupci njihovu kliničku vrijednost. Postoje takođe značajni dokazi da mnogi ljudi s ADHD-om imaju biomarker za uključivanje izmenjene norepinefrine obrade.[54] Nekoliko lijekova čiji su primarni učinci na norepinefrin, uključujući guanfacin, klonidin i atomoksetin, isprobani su kao tretmani za ADHD, a otkriveno je da imaju učinke uporedive s efektima stimulansa.[55][56]
Autonomni poremćaj
urediNekoliko stanja, uključujući Parkinsonovu bolest, dijabetes i takozvano čisto autonomno zatajenje, može prouzrokovati gubitak neurona koji izlučuju norepinefrin u simpatičkom nervnom sistemu. Simptomi su mnogobrojni, a najozbiljniji je smanjenje broja otkucaja srca i ekstremni pad krvnog pritiska u mirovanju, što onemogućuje teško pogođenim osobama da stoje duže od nekoliko sekundi bez nesvjestice. Liječenje može uključivati promjene prehrane ili lijekove.[57]
Uporedna biologija i evolucija
urediZa norepinefrin se navodi da postoji u velikom broju različitih životinjskih vrsta, uključujući protozoa,[58] Placozoa i Cnidaria (meduze i srodne vrste),[59] ali ne i kod Ctenophora, čiji se živčani sistem uveliko razlikuje od ostalih životinja.[60] Obično je prisutan u deuterostomia (kičmenjaci itd.), ali u protostomia (artropodi, mehkušci, pljosnati crvi, nematode, anelide itd.) Zamjenjuje ga hobotopin, usko povezana hemikalija s blisko srodnim putem sinteze.[58] U insekata, oktopamin ima alarmirajuće i aktivirajuće funkcije koje (barem otprilike) odgovaraju funkcijama norepinefrina u kičmenjaka.[61] Utvrđeno je da je oktopamin evoluirao da zamijeni norepinefrin umjesto obrnuto; međutim, objavljeno je da nervni sistem amfioksusa (primitivni hordat) sadrži oktopamin, ali ne i norepinefrin, što predstavlja teškoće za tu hipotezu.[58]
Historija
urediPočetkom dvadesetog stoljeća Walter Cannon, koji je popularizirao ideju o simpatiadrenalnom sistemu pripremajući tijela za borbu i bijeg, i njegov kolega Arturo Rosenblueth razvili su teoriju o dva simpatina, simpatiin E (podražavajući) i simpatin I (inhibitorni). Smatraju ih odgovornim za ove akcije.[62] Belgijski farmakolog Zénon Bacq, kao i kanadski i SAD-američki farmakolozi između 1934. i 1938. sugerirali su da bi noradrenalin mogao biti simpatički transmiter.[62] U 1939., Hermann Blaschko i Peter Holtz, nezavisno su identificirali biosintetski mehanizam za norepinefrin u tijelu kičmenjaka.[63][64] U 1945., Ulf von Euler objavio je prvi u nizu radova kojima je utvrđena uloga norepinefrina kao neurotransmitera.[65] Dokazao je prisustvo norepinefrina u simpatički innerviranom tkivu i mozgu, te pridodao dokaze da je to simpatin Cannona i Rosenblueta.
Reference
uredi- ^ Aronson JK (Feb 2000). "'Where name and image meet'—the argument for 'adrenaline'". British Medical Journal. 320 (7233): 506–9. doi:10.1136/bmj.320.7233.506. PMC 1127537. PMID 10678871.
- ^ "(-)-noradrenaline". IUPHAR database. International Union of Basic and Clinical Pharmacology. Arhivirano s originala, 3. 4. 2019. Pristupljeno 2. 1. 2016.
- ^ "Norepinephrine". PubChem. Pristupljeno 6. 11. 2015.
- ^ Gaddum JH (juni 1956). "The Prefix 'Nor' in Chemical Nomenclature". Nature. 177 (1046): 1046. Bibcode:1956Natur.177.1046G. doi:10.1038/1771046b0.
- ^ a b c d e f g Musacchio JM (2013). "Chapter 1: Enzymes involved in the biosynthesis and degradation of catecholamines". u Iverson L (ured.). Biochemistry of Biogenic Amines. Springer. str. 1–35. ISBN 978-1-4684-3171-1.
- ^ Griffith, Robert K. (2013). "Chapter 10: Adrenergic Receptors and Drugs Affecting Adrenergic Neurotransmission". u Lemke, Thomas L.; Williams, David A.; Zito, S. William; Roche, Victoria F. (ured.). Foye's Principles of Medicinal Chemistry (7th izd.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. str. 343. ISBN 978-1-60913-345-0. Nepoznati parametar
|name-list-format=zanemaren (prijedlog zamjene:|name-list-style=) (pomoć) - ^ a b Rang HP, Ritter JM, Flower R, Henderson G (2014). "Chapter 14: Noradrenergic transmission". Rang & Dale's Pharmacology. Elsevier Health Sciences. str. 177–196. ISBN 978-0-7020-5497-6.
- ^ a b Eiden LE, Schäfer MK, Weihe E, Schütz B (2004). "The vesicular amine transporter family (SLC18): amine/proton antiporters required for vesicular accumulation and regulated exocytotic secretion of monoamines and acetylcholine". Pflügers Arch. 447 (5): 636–40. doi:10.1007/s00424-003-1100-5. PMID 12827358.
- ^ Torres GE, Gainetdinov RR, Caron MG (2003). "Plasma membrane monoamine transporters: structure, regulation and function". Nature Reviews Neuroscience. 4 (1): 13–25. doi:10.1038/nrn1008. PMID 12511858.
- ^ a b c Hamill RW, Shapiro RE, Vizzard MA (2012). "Peripheral Autonomic Nervous System". u Robertson D, Biaggioni I, et al. (ured.). Primer on the Autonomic Nervous System. Academic Press. str. 17–20. ISBN 978-0-12-386525-0.
- ^ a b Schacter D, Gilbert D, Wegner D, Hood B (2011). Psychology: European Edition. Palgrave Macmillan. str. 93. ISBN 978-0-230-34367-2.
- ^ Dartt DA (maj 2009). "Neural regulation of lacrimal gland secretory processes: relevance in dry eye diseases". Progress in Retinal and Eye Research. 28 (3): 155–77. doi:10.1016/j.preteyeres.2009.04.003. PMC 3652637. PMID 19376264.
- ^ Tank AW, Lee Wong D (januar 2015). Peripheral and central effects of circulating catecholamines. Comprehensive Physiology. 5. str. 1–15. doi:10.1002/cphy.c140007. ISBN 9780470650714. PMID 25589262.
- ^ Bahler L, Molenaars RJ, Verberne HJ, Holleman F (septembar 2015). "Role of the autonomic nervous system in activation of human brown adipose tissue: A review of the literature". Diabetes & Metabolism. 41 (6): 437–445. doi:10.1016/j.diabet.2015.08.005. PMID 26404650.
- ^ Kenney MJ, Ganta CK (juli 2014). Autonomic nervous system and immune system interactions. Comprehensive Physiology. 4. str. 1177–200. doi:10.1002/cphy.c130051. ISBN 9780470650714. PMC 4374437. PMID 24944034.
- ^ Chistiakov DA, Ashwell KW, Orekhov AN, Bobryshev YV (2015). "Innervation of the arterial wall and its modification in atherosclerosis". Auton Neurosci. 193: 7–11. doi:10.1016/j.autneu.2015.06.005. PMID 26164815.
- ^ a b c d Thorp AA, Schlaich MP (2015). "Relevance of Sympathetic Nervous System Activation in Obesity and Metabolic Syndrome". J Diabetes Res. 2015: 1–11. doi:10.1155/2015/341583. PMC 4430650. PMID 26064978.
- ^ Konturek SJ, Konturek JW, Pawlik T, Brzozowski T (2004). "Brain-gut axis and its role in the control of food intake" (PDF). J. Physiol. Pharmacol. 55 (1 Pt 2): 137–54. PMID 15082874.
- ^ Pakdeechote, P; Dunn, W R; Ralevic, V (2007). "Cannabinoids inhibit noradrenergic and purinergic sympathetic cotransmission in the rat isolated mesenteric arterial bed". British Journal of Pharmacology. 152 (5): 725–733. doi:10.1038/sj.bjp.0707397. ISSN 0007-1188. PMC 2190027. PMID 17641668.
- ^ Dahlstroem A, Fuxe K (1964). "Evidence for the existence of monoamine-containing neurons in the central nervous system. I. Demonstration of monoamines in the cell bodies of brain stem neurons". Acta Physiologica Scandinavica. Supplementum. 232 (Supplement 232): 1–55. PMID 14229500.
- ^ Antunes-Rodrigues J, de Castro M, Elias LL, Valença MM, McCann SM (januar 2004). "Neuroendocrine control of body fluid metabolism" (PDF). Physiological Reviews. 84 (1): 169–208. doi:10.1152/physrev.00017.2003. PMID 14715914. Arhivirano s originala (PDF), 6. 3. 2019. Pristupljeno 14. 8. 2020.
- ^ Rinaman L (februar 2011). "Hindbrain noradrenergic A2 neurons: diverse roles in autonomic, endocrine, cognitive, and behavioral functions". American Journal of Physiology. Regulatory, Integrative and Comparative Physiology. 300 (2): R222–35. doi:10.1152/ajpregu.00556.2010. PMC 3043801. PMID 20962208.
- ^ Bruinstroop E, Cano G, Vanderhorst VG, Cavalcante JC, Wirth J, Sena-Esteves M, Saper CB (juni 2012). "Spinal projections of the A5, A6 (locus coeruleus), and A7 noradrenergic cell groups in rats". The Journal of Comparative Neurology. 520 (9): 1985–2001. doi:10.1002/cne.23024. PMC 3508755. PMID 22173709.
- ^ a b c Sara SJ, Bouret S (2012). "Orienting and reorienting: the locus coeruleus mediates cognition through arousal". Neuron. 76 (1): 130–41. doi:10.1016/j.neuron.2012.09.011. PMID 23040811.
- ^ a b Berridge CW, Schmeichel BE, España RA (2012). "Noradrenergic modulation of wakefulness/arousal". Sleep Med Rev. 16 (2): 187–97. doi:10.1016/j.smrv.2011.12.003. PMC 3278579. PMID 22296742.
- ^ Sara SJ (2015). "Locus Coeruleus in time with the making of memories". Curr. Opin. Neurobiol. 35: 87–94. doi:10.1016/j.conb.2015.07.004. PMID 26241632.
- ^ a b c Gardenhire DS (2013). Rau's Respiratory Care Pharmacology. Elsevier Health Sciences. str. 88. ISBN 978-0-323-27714-3.
- ^ Rhodes, Andrew; Evans, Laura E (mart 2017). "Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock 2016" (PDF). Critical Care Medicine. 45 (3): 486–552. doi:10.1097/CCM.0000000000002255. PMID 28098591. Arhivirano s originala (PDF), 1. 3. 2021. Pristupljeno 14. 8. 2020.
We recommend norepinephrine as the first-choice vasopressor (strong recommendation, moderate quality of evidence).
- ^ a b Deedwania PC (2015). "Management of Patients With Stable Angina and Type 2 Diabetes". Rev Cardiovasc Med. 16 (2): 105–13. PMID 26198557.
- ^ Mareev Y, Cleland JG (2015). "Should β-Blockers Be Used in Patients With Heart Failure and Atrial Fibrillation?". Clin Ther. 37 (10): 2215–24. doi:10.1016/j.clinthera.2015.08.017. PMID 26391145.
- ^ Kumar A, Agarwal S (2014). "Marfan syndrome: An eyesight of syndrome". Meta Gene. 2: 96–105. doi:10.1016/j.mgene.2013.10.008. PMC 4287801. PMID 25606393.
- ^ a b Inoue K (2014). "Managing adverse effects of glaucoma medications". Clin Ophthalmol. 8: 903–13. doi:10.2147/OPTH.S44708. PMC 4025938. PMID 24872675.
- ^ Brugués AO (2011). "Music performance anxiety-part 2. a review of treatment options". Med Probl Perform Art. 26 (3): 164–71. PMID 21987072.
- ^ Fitch K (2012). "Proscribed drugs at the Olympic Games: permitted use and misuse (doping) by athletes". Clin Med. 12 (3): 257–60. doi:10.7861/clinmedicine.12-3-257. PMC 4953490. PMID 22783779.
- ^ a b c d Lilley LL, Collins SR, Snyder JS (2014). Pharmacology and the Nursing Process (7th izd.). Elsevier Health Sciences. str. 313–316. ISBN 978-0-323-29361-7.
- ^ Hollingsworth, John M; Wilt, Timothy J (14. 8. 2014). "Lower urinary tract symptoms in men". The BMJ. 349. doi:10.1136/bmj.g4474. ISSN 0959-8138. PMC 4688452. PMID 25125424.
- ^ Campschroer, Thijs; Zhu, Xiaoye; Vernooij, Robin Wm; Lock, Mtw Tycho (5. 4. 2018). "Alpha-blockers as medical expulsive therapy for ureteral stones". The Cochrane Database of Systematic Reviews. 4: CD008509. doi:10.1002/14651858.CD008509.pub3. ISSN 1469-493X. PMC 6494465. PMID 29620795.
- ^ Green B (2014). "Prazosin in the treatment of PTSD". J Psychiatr Pract. 20 (4): 253–9. doi:10.1097/01.pra.0000452561.98286.1e. PMID 25036580.
- ^ a b c Corazza O, Martinotti G, Santacroce R, Chillemi E, Di Giannantonio M, Schifano F, Cellek S (2014). "Sexual enhancement products for sale online: raising awareness of the psychoactive effects of yohimbine, maca, horny goat weed, and Ginkgo biloba". Biomed Res Int. 2014: 1–13. doi:10.1155/2014/841798. PMC 4082836. PMID 25025070.
- ^ EFSA Panel on Food Additives and Nutrient Sources Added to Food (2013). "Scientific Opinion on the evaluation of the safety in use of Yohimbe". EFSA Journal. 11 (7): 3302. doi:10.2903/j.efsa.2013.3302.
- ^ a b c Lemke KA (2004). "Perioperative use of selective alpha-2 agonists and antagonists in small animals". Can. Vet. J. 45 (6): 475–80. PMC 548630. PMID 15283516.
- ^ Belkin MR, Schwartz TL (2015). "Alpha-2 receptor agonists for the treatment of posttraumatic stress disorder". Drugs in Context. 4: 1–5. doi:10.7573/dic.212286. PMC 4544272. PMID 26322115.
- ^ Greene SA, Thurmon JC (1988). "Xylazine—a review of its pharmacology and use in veterinary medicine". J. Vet. Pharmacol. Ther. 11 (4): 295–313. doi:10.1111/j.1365-2885.1988.tb00189.x. PMID 3062194.
- ^ Sofuoglu, Mehmet; Sewell, R. Andrew (april 2009). "Norepinephrine and Stimulant Addiction". Addiction biology. 14 (2): 119–129. doi:10.1111/j.1369-1600.2008.00138.x. ISSN 1355-6215. PMC 2657197. PMID 18811678.
- ^ Heal, David J.; Smith, Sharon L.; Gosden, Jane; Nutt, David J. (juni 2013). "Amphetamine, past and present—a pharmacological and clinical perspective". Journal of Psychopharmacology. 27 (6): 479–496. doi:10.1177/0269881113482532. PMC 3666194. PMID 23539642.
- ^ Finberg, John P. M.; Rabey, Jose M. (2016). "Inhibitors of MAO-A and MAO-B in Psychiatry and Neurology". Frontiers in Pharmacology (jezik: English). 7. doi:10.3389/fphar.2016.00340. ISSN 1663-9812.
Selective inhibition of MAO-A leads to increased levels of neurotransmitter within noradrenergic (NA-ergic) and 5-HT-ergic neurons of the CNS, and clinical antidepressant action, while inhibition of MAO-B leads to increased levels of DA in the Parkinsonian brain...
CS1 održavanje: nepoznati jezik (link) - ^ Lump D, Moyer M (2014). "Paroxysmal sympathetic hyperactivity after severe brain injury". Curr Neurol Neurosci Rep. 14 (11): 494. doi:10.1007/s11910-014-0494-0. PMID 25220846.
- ^ Amzallag M (1993). "Autonomic hyperreflexia". Int Anesthesiol Clin. 31 (1): 87–102. doi:10.1097/00004311-199331010-00009. PMID 8440534.
- ^ McCrink KA, Brill A, Lymperopoulos A (2015). "Adrenal G protein-coupled receptor kinase-2 in regulation of sympathetic nervous system activity in heart failure". World J Cardiol. 7 (9): 539–43. doi:10.4330/wjc.v7.i9.539. PMC 4577680. PMID 26413230.
- ^ Malpas SC (2010). "Sympathetic nervous system overactivity and its role in the development of cardiovascular disease". Physiol. Rev. 90 (2): 513–57. doi:10.1152/physrev.00007.2009. PMID 20393193.
- ^ Ksiazek A, Załuska W (2008). "Sympathetic overactivity in uremia". J Ren Nutr. 18 (1): 118–21. doi:10.1053/j.jrn.2007.10.024. PMID 18089457.
- ^ a b c d Chrousos GP (2009). "Stress and disorders of the stress system". Nat Rev Endocrinol. 5 (7): 374–81. doi:10.1038/nrendo.2009.106. PMID 19488073.
- ^ Kooij SJ, Bejerot S, et al. (2010). "European consensus statement on diagnosis and treatment of adult ADHD: The European Network Adult ADHD". BMC Psychiatry. 10: 67. doi:10.1186/1471-244X-10-67. PMC 2942810. PMID 20815868.
- ^ Faraone SV, Bonvicini C, Scassellati C (2014). "Biomarkers in the diagnosis of ADHD--promising directions". Curr Psychiatry Rep. 16 (11): 497. doi:10.1007/s11920-014-0497-1. PMID 25298126.
- ^ Bello NT (2015). "Clinical utility of guanfacine extended release in the treatment of ADHD in children and adolescents". Patient Prefer Adherence. 9: 877–85. doi:10.2147/PPA.S73167. PMC 4494608. PMID 26170637.
- ^ Clemow DB, Bushe CJ (2015). "Atomoxetine in patients with ADHD: A clinical and pharmacological review of the onset, trajectory, duration of response and implications for patients". J. Psychopharmacol. (Oxford). 29 (12): 1221–30. doi:10.1177/0269881115602489. PMID 26349559.
- ^ Shibao C, Okamoto L, Biaggioni I (2012). "Pharmacotherapy of autonomic failure". Pharmacol. Ther. 134 (3): 279–86. doi:10.1016/j.pharmthera.2011.05.009. PMC 3358114. PMID 21664375.
- ^ a b c Pflüger HJ, Stevensonb PA (2005). "Evolutionary aspects of octopaminergic systems with emphasis on arthropods". Arthropod Structure & Development. 34 (3): 379–396. doi:10.1016/j.asd.2005.04.004.
- ^ Kass-Simon G, Pierobon P (2007). "Cnidarian chemical neurotransmission, an updated overview". Comp. Biochem. Physiol., Part a Mol. Integr. Physiol. 146 (1): 9–25. doi:10.1016/j.cbpa.2006.09.008. PMID 17101286.
- ^ Moroz LL (2015). "Convergent evolution of neural systems in ctenophores". J. Exp. Biol. 218 (Pt 4): 598–611. doi:10.1242/jeb.110692. PMC 4334147. PMID 25696823.
- ^ Verlinden H, Vleugels R, Marchal E, Badisco L, Pflüger HJ, Blenau W, Broeck JV (2010). "The role of octopamine in locusts and other arthropods". J. Insect Physiol. 56 (8): 854–67. doi:10.1016/j.jinsphys.2010.05.018. PMID 20621695.
- ^ a b Bacq ZM (1983). "Chemical transmission of nerve impulses". u Parnham MJ, Bruinvels J (ured.). Discoveries in Pharmacology, Volume 1. Amsterdam: Elsevier. str. 49–103. ISBN 978-0-444-80493-8.
- ^ Herman Blaschko (1987). "A half-century of research on catecholamine biosynthesis". Journal of Applied Cardiology: 171–183.
- ^ P. Holtz (1939). "Dopadecarboxylase". Die Naturwissenschaften (jezik: German). 27 (43): 724–725. Bibcode:1939NW.....27..724H. doi:10.1007/bf01494245.CS1 održavanje: nepoznati jezik (link)
- ^ von Euler US (1945). "A sympathomimetic pressor substance in animal organ extracts". Nature. 156 (3949): 18–19. Bibcode:1945Natur.156...18V. doi:10.1038/156018b0.