Akcijski potencijal
Akcijski potencijal (AP) je pojava snažnih, brzih i povratnih promjena membranskog potencijala, koji se javlja kao odgovor na dovoljnu razinu depolarizacije. Ovaj potencijal je fenomen koji se obično označava kao nervni impuls, podražaj, razdraženje, nadražaj, a sve češće i tuđicom ekscitacija. One ćelijr koje su sposobne da generiraju akcijski potencijal nazivaju se ekscitabilne ćelije (nadražljive ćelije), a to su:

Pojava akcijskog potencijala za "hop" preskakanje od čvora do čvora
Aksoni neurona su umotani u nekoliko mijelinskih ovojnica, koje štite akson od izvanstanične tekućine. Između mijelinskih ovojnica, postoji kratki jaz poznat kao Ranvjierovi čvorovi gdje je akson direktno izložen izvanstaničnom prostoru.
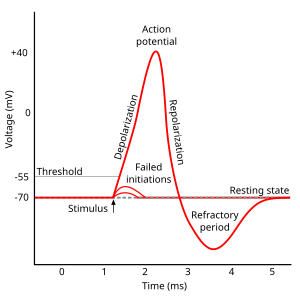
Membranski potencijal počinje na -70 mV u vremenu nula. Poticaj se javlja u vremenu = 1 ms, što otvara potencijal membrane iznad -55 mV (prag potencijala).
Nakon što primi stimulans, membranski potencijal brzo raste do vrhunca – potencijal +40 mV u vrijeme = 2 ms.
Baš kao što brzo raste, potencijal onda padne i prekorači do -90 mV za vrijeme = 3 ms, a na kraju, potencijal mirovanja je od -70 mV dostignut za vrijeme = 5 ms.


Brzina provođenja ' 'V' ' mijelinskih neurona varira približno linearno promjeru aksona D(koji je, Valfa ' 'D' 'crvena i plava kriva su prikazi eksperimentalnih podataka, a isprekidane linije su teorijske ekstrapolacije.
Log-log dijelovi brzine provodljivosti (m/s) vs promjera aksona ((μm)


Membranski potencijal ostaje blizu razine osnovnog, dok se u nekom trenutku vrh ide naglo prema gore, a zatim brzo pada.
Faze
urediNa početku akcijskog potencijala, Na+otvoraraju kanale i Na + kreće u aksona, uzrokujući depolarizaciju. Repolarizacija nastaje kada K+otvori i kanale K+ i kreće iz aksona.
To stvara promjenu odnosa polarizacije između van- i unutarstanične sredine.
Impuls putuje niz akson samo u jednom pravcu, u aksonski terminal, gdje prenosi signal drugim neuronima.
Membranski potencijal živčanih vlakana u stanju mirovanja iznosi oko -90 mV, što znači da je potencijal u citosolu za 90 mV negativniji u odnosu na potencijal izvanćelijskog prostora. Akcijski potencijal se ispoljava kao brza promjena membranskog potencijala u mirovanju koja se brzo širi duž živčanog vlakna. Taj polazni membranski potencijal označava se kao prvi stadij nastanka akcijskog potencijala, tzv.
- stadij mirovanja (MMP), a zatim
- stadij depolarizacije.
Tada membrana iznenada postane vrlo propustljiva za natrijeve ione, dozvoljavajući protok ogromnog broja pozitivno nabijenih Na+ iona u unutrašnjost stanice. To izaziva porast membranskog potencijala mirovanja, sa uobičajenih -90 mV, u pozitivnom smjeru. Kod debelih nervnih vlakana, ogromna količina Na+ iona dovodi do prebacivanja MMP preko nulte razine u malo pozitivnu vrijednost, dok se potencijal u tanjim vlaknima i mnogobrojnim neuronima centralnog nervnog sistema samo približava nultoj razini, ali je ne prelazi. Tokom nekoliko 1/10.000 dijelova sekunde, nakon što je membrana postala visoko propustljiva za Na+ ione, natrijski kanali počinju da se zatvaraju, dok se kalijski otvaraju više nego što je normalno. Brza difuzija K+ iz citosola u izvanstaničnu sredinu uspostavlja normalan membranski potencijal mirovanja, što se naziva stadij repolarizacije. Prema tome, u nastajanju i nestajanju akcijskih potencijala živčanih vlakana ključnu ulogu imaju naponsko-zavisni natrijski i naponski-zavisni kalijski kanali.
Akcijski potencijal nastaje uključivanjem mehanizma pozitivne povratne sprege (circulus vitiosusa): rastući električni napon izaziva otvaranje naponsko-zavisnih natrijskih kanala. To omogućava brzu difuziju ogromne količine Na+ u stanicu, što dodatno povećava razinu membranskog potencijala mirovanja, otvarajući tako još naponski zavisnih natrijskih kanala i još obimniju difuziju Na+iona. Akcijski potencijali prenose se po principu sve-ili-ništa, što znači da se, u odsustvu svih uvjeta, rasprostire bez gubitka, sa konstantnom amplitudom, dok se, ako uvjeti nisu ispunjeni, uopće se ne širi. Formiraju se samo na inicijalnom segmentu neurona jer se tu nalazi sedam puta više Na+ iona nego drugdje.[1][2][3][4]
Saltacijsko provođenje akcijskog potencijala
urediCentralni dio aksona ispunjen je specijalnom citoplazmom (aksoplazmom), u obliku žitke unutarstaničnog prostora. Većinu aksona okružuje mijelinski omotač koji djeluje kao izolator. Ovaj omotač je često znatno deblji od samog aksona, a za njegovo stvaranje, u CNS su odgovorni oligodendrociti, dok tu funkciju u perifernim nervnim vlaknima obavljaju Schwannove stanica. Pritom, jedan oligodendrocit stvara mijelin čak za do 40 aksona, dok jedna Schwannova stanica oblaže samo jedan segment perifernog aksona. Membrana Schwannove stanice obavija se oko aksona, a zatim stanica rotira oko njega, oblažući ga izolatorom koji, i do 5.000 puta, smanjuje protok iona kroz membranu. Na spoju dvije sukcesivne Schwannove stanice, nalaze se mala neizolirana područja, dugačka svega 2-3 mikrometra, koja se zovu Ranvijerovi čvorovi. Iako ioni skoro da ne mogu teći kroz mijelinski omotač mijeliziranih živaca, oni sa lakoćom protječu kroz Ranvijerove čvorove. Način na koji se akcijski potencijal kreće od čvora do čvora naziva se saltacijska kondukcija. To znači da elektricitet teče kroz okolni izvanstanični prostor koji oplakuje mijelinsku opnu, kao i kroz aksoplazmu unutar aksona, podražavajući sukcesivne čvorove jedan za drugim, tj. 'preskačući' od jednog čvora do drugog, nadražujući ih. Saltacijsko provođenje izaziva pojavu da proces depolarizacije skače u dugim intervalima duž osovine nervnog vlakna, pa tako povećava brzinu nervne transmisije u mijeliniziranim vlaknima, za 5-50 puta. Ovakav način provođenja akcijskog potencijala također čuva energiju za akson, time što se depolariziraju samo Ranvijerovi čvorovi, omogućavajući i do 100 puta manji gubitak iona. Brzina kondukcije u živčanim vlaknima varira od takonniskih razina kao što je 0,25 m/s (u malim nemijeliniziranim nervnim vlaknima), do tako visoke, kao što je 120 m/s (u veoma debelim mijeliziranim).
Naponski-zavisni natrijski kanali
urediNapon-zavisni Na+ kanal ima dva izlaza : jedan je na vanjskom dijelu stanice, zvani aktivacijska vrata, a drugi je – inaktivacijska vrata, koja su u kontaktu sa citosolom. Pri normalnom membranskom potencijalu mirovanja od -90 mV, aktivacijska vrata su zatvorena, što onemogućuje ulaženje natrijevih iona kroz ove kanale. Međutim, kada taj potencijal počne gubiti negativnu polarizaciju i raste prema pozitivnom, i kada dostigne napon između -70 i -50 mV, izaziva konformacijsku promjenu u aktivacijskim vratima, koja se odmah otvaraju. Ovo stanje povećava propustljivost membrane za Na+ ione za oko 500 do 5.000 puta. To je stadij depolarizacije. Međutim, nekoliko 1/10.000 dijelova sekunde nakon otvaranja aktivacijskih vrata, zatvaraju se inaktivacijska, a njihovo zatvaranje izaziva istu konformacijsku promjenu koja je i dovela do otvaranja aktivacijskih. Kada se zatvore inaktivacijska vrata, membranski potencijal se počinje obnavljati prema normalnih -90 mV, što je proces repolarizacije. Ponovno otvaranje natrijskih kanala neće se dogoditi ako se prethodno MMP ne vrati na normalnu razinu od -90 mV ili na približnu vrijednost, tj. ako se vlakno ne repolarizira.
Naponski-zavisni kalijevi kanali
urediKalijski kanal ima vrata na citoplazmatskom dijelu membrane, koja su tokom membranskog potencijala u mirovanju zatvorena, što sprečava difuziju K+ iona u izvanćelijsku tekućinu. Porast MMP ka nuli izaziva konformacijsko otvaranje vrata i pojačan dotok kalija spolja. Međutim, zbog neznatno odloženog otvaranja kalijevih kanala, oni se otvaraju istovremeno sa početkom zatvaranje natrijskih, a zbog inaktivacije. Tako i dolazi do smanjenog ulaska Na+ u stanicui povećanog izlaska K+ iz stanice, što smanjuje naelektriziranost i dovodi do obnavljanja normalnog membranskog potencijala u mirovanju.[5][6]
Također pogledajte
urediReference
uredi- ^ Kandel E. R. , Schwartz J. H., Jessell T. M. (2000): Principles of neural science, 4th Ed. McGraw-Hill, New York, ISBN 0-8385-7701-6.
- ^ Nelson D. L., Cox M. M. (2008): Lehninger principles of biochemistry, 5th Ed. W. H. Freeman, New York, ISBN 978-0-7167-7108-1.
- ^ Purves D, Augustine G. J., Fitzpatrick D., Hall W. C., Lamantia A-S., McNamara J. O., Williams S. M. (2001): Neuroscience, 2nd Ed. Sinauer Associates, Sunderland, MA, Release of Transmitters from Synaptic Vesicles, ISBN 0-87893-725-0: chapterurl=http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=neurosci.section.326.
- ^ Purves D., Augustine G. J., Fitzpatrick D., Hall W. C., Lamantia A-S., McNamara J. O., White L. E. (2008): Neuroscience, 4th Ed., Sinauer Associates, Sunderland, MA, ISBN 978-0-87893-697-7.
- ^ Aidley DJ, Stanfield PR (1996). Ion Channels: Molecules in Action. Cambridge: Cambridge University Press. ISBN 978-0-521-49882-1.
- ^ Bear MF, Connors BW, Paradiso MA (2001). Neuroscience: Exploring the Brain. Baltimore: Lippincott. ISBN 0-7817-3944-6.CS1 održavanje: više imena: authors list (link)
Vanjski linkovi
uredi- https://web.archive.org/web/20050625075706/http://www.blackwellpublishing.com/matthews/channel.html Ionic flow in action potentials] at Blackwell Publishing
- https://web.archive.org/web/20070615135508/http://www.blackwellpublishing.com/matthews/actionp.html Action potential propagation in myelinated and unmyelinated axons] at Blackwell Publishing
- http://thevirtualheart.org/CAPindex.html Generation of AP in cardiac cells] *http://thevirtualheart.org/java/neuron/apneuron.html generation of AP in neuron cells]
- https://web.archive.org/web/20080414190744/http://bcs.whfreeman.com/thelifewire/content/chp44/4402001.html Resting membrane potential] from Life: The Science of Biology, by WK Purves, D Sadava, GH Orians, and HC Heller, 8th edition, New York: WH Freeman, ISBN 978-0-7167-7671-0.
- http://www.nernstgoldman.physiology.arizona.edu/ Arhivirano 8. 8. 2010. na Wayback Machine Ionic motion and the Goldman voltage for arbitrary ionic concentrations] at The University of Arizona