Polifenoli
Polifenoli su velika porodica prirodnih organskih spojeva koje karakterišu višestruke jedinice fenola.[1] Bogati su biljkama i strukturno su raznoliki.[1][2][3] Polifenoli uključuju flavonoide, taninsku kiselinu i elagitanin, od kojih su neki korišteni u prošlosti kao boje i za štavljenje odjevnih predmeta.

Etimologija
urediIme potiče od starogrčke riječi πολύς - polus, što značii mnogo, više") i riječi fenol koja se odnosi na hemijsku strukturu formiranu vezivanjem za aromatski benzenoid (fenil) prsten u hidroksil (-OH) grupu koja se nalazi u alkoholima (otuda sufiks -ol). Termin polifenol je u upotrebi najmanje od 1894.[4]
Definicija
urediTermin polifenol nije dobro definiran, ali se općenito slaže da su to prirodni proizvodi "koji imaju polifenolnu strukturu (tj. nekoliko hidroksilnih grupa na aromatskim prstenovima)" uključujući četiri glavne klase: "fenolne kiseline, flavonoide, stilbene i lignane".[5]
- Flavonoidi uključuju flavone, flavonole, flavanole, flavanone, izoflavone, proantocijanidine i antocijanine. Posebno bogati flavanoidi u hrani su katehin (čaj, voće), hesperetin (agrumi), cijanidin (crveno voće i bobice), daidzein (soja ), proantocijanidin (jabuka, grožđe, kakao) i kvuercetin (luk, čaj, jabuke).[2]
- Fenolna kiselina uključuje kafeinsku kiselinu
- Lignani su polifenoli dobijeni iz fenilalanina koji se nalaze u lanenom sjemenu i drugim žitaricama.
WBSSH definicija
urediWhite–Bate-Smith–Swain–Haslamova (WBSSH) definicija [6] karakterizira strukturna obilježja uobičajena za biljne fenole koji se koriste u štavljenje (tj. tanini).[7]
U pogledu svojstava, WBSSH opisuje polifenole na sljedeći način:
- općenito umjereno vodotopivi spojevi
- sa molekulskom težinom od 500–4000 Da
- sa >12 fenolnih hidroksilnih grupa
- sa 5-7 aromatskih rstenova na 1000 Da
Što se tiče struktura, WBSSH prepoznaje dvije porodice koje imaju ova svojstva:
- proantocijanidini i njihovi derivati
- galoil i heksahidroksidifenoil estri i njihovi derivati
Quideauova definicija
urediPrema Stéphaneu Quideauu, termin "polifenol" odnosi se na spojeve izvedene iz šikimat/fenilpropanoid i/ili poliketidnpog puta, koji sadrži više od jedne fenolne jedinice i lišen dušika na bazi funkcije.
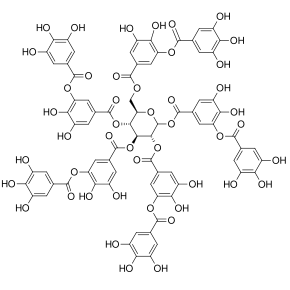
Elagična kiselina, molekula u srži prirodnih fenolnih spojeva različitih veličina, sama po sebi nije polifenol prema WBSSH definiciji, već prema Quideauovoj definiciji. Mlinski elagitanin,[8] s druge strane, sa svojih 14 dijelova galne kiseline (većina u komponentama tipa elaginske kiseline), i više od 40 fenolnih hidroksilnih grupa, zadovoljava kriterije obje definicije polifenola. Ostali primjeri spojeva koji potpadaju pod definicije po WBSSH-u i Quideauu uključuju crni čaj teaflavin-3-galat prikazan ispod, i tanin koji se može hidrolizovati, taninsku kiselinu. [[slika:Theaflavin 3-gallate.svg|thumb|left|upright|Teaflavin-3-galat, polifenol biljnog porijekla, estar galne kiseline i teaflavinsko jezgro. Postoji 9 fenolnih hidroksilnih grupa i dvije fenolne eterske veze.
Hemija
urediPolifenoli su reaktivne vrste prema oksidaciji, otuda njihov opis kao antioksidansa in vitro.[9]
Strukturna hemija
urediPolifenoli su često veće molekule (makromolekule). Njihova gornja granica molekulse težine je oko 800 daltona, što omogućava brze difuzije kroz ćelijske membrane, tako da mogu doći do međućelijskih mjesta djelovanja ili ostati kao pigmenti, nakon što ćelija senescira. Stoga se mnogi veći polifenoli biosintetiziraju "in-situ" od manjih polifenola do nehidrolizirajućih tanina i ostaju neotkriveni u biljnom matriksu. Većina polifenola sadrži ponavljajuće fenolne dijelove pirokatehola, resorcinola, pirogalola i floroglucinola, povezane esterima (tanini koji se mogu hidrolizirati) ili stabilnijim C-C vezama (nehidrolizirani kondenzirani tanini). Proantocijanidini su uglavnom polimerne jedinice katehina i epikatehina. [[Slika:Puerarin.svg|thumb|Podstrukturu C-glukozida polifenola predstavlja konjugat fenol-saharid puerarin, prirodni biljni proizvod srednje molekulske težine. Vezanje fenola za saharid je vezom ugljik-ugljik. Izoflavon i njegov 10-atomski benzopiranski sistem "stopljenog prstena", koji je ovdje također strukturna karakteristika, uobičajen je u polifenolima.]]
Polifenoli često imaju funkcionalne grupe izvan hidroksilnih grupa. Eterne esterske veze su uobičajene, kao i karboksilne kiseline.
Analitička hemija
urediTehnike analize su one iz fitohemije: ekstrakcija, izolacija, strukturno razjašnjavanje,[10] zatim kvantifikacija.
Ekstrakcija
urediEkstrakcija polifenola [11] može se izvesti pomoću rastvarača kao što je voda, vruća voda, metanol, metanol/mravlja kiselina, metanol/voda/sirćetna ili mravlja kiselina. ekstrakcija tekućina–tečnost se također može izvesti ili protustrujna hromatografija. Ekstrakcija čvrste faze se takođe može napraviti na C18 sorbent patronama. Druge tehnike su ultrazvučna ekstrakcija, ekstrakcija refluksa toplote, ekstrakcija uz pomoć mikrotalasne pećnice,[12] kritičnog ugljik-dikoksida,[13][14] pod visokim pritiskom tečnom ekstrakcijom[15] ili korištenjem etanola u uranjajućem ekstraktoru.[16] Uvjeti ekstrakcije (temperatura, vrijeme ekstrakcije, omjer rastvarača i sirovog materijala, veličina čestica uzorka, tip rastvarača i koncentracije rastvarača) za različite sirovine i metode ekstrakcije moraju biti optimizirani.[17][18] Visoki nivoi polifenola koji se uglavnom nalaze u kožici i sjemenkama voća mogu odražavati samo "izmjereni sadržaj ekstrahiravog" polifenola (EPP) u voću, koji također može sadržavati polifenole koje se ne mogu ekstrahirati. Crni čaj sadrži velike količine polifenola i čini 20% njegove težine.[19]
Koncentracija se može postići ultrafiltracijom.[20] Purification can be achieved by preparative chromatography.
Tehnike analize
urediFosfomolibdinska kiselina se koristi kao reagens za bojenje fenola u tankoslojnoj hromatografiji. Polifenoli se mogu proučavati spektroskopski, posebno u ultraljubičastom domenu, frakcioniranjem ili hromatografijom na papiru. Mogu se analizirati i hemijskom karakterizacijom.
Instrumentalnohemijske analize uključuju odvajanje pomoću tečne hromatografije visokih performansi (HPLC), a posebno tečne hromatografije reverzne faze (RPLC), mogu se povezati sa masenom spektrometrijom.[13] Prečišćeni spojevi mogu se identifikovati pomoću nuklearne magnetne rezonance.
Mikroskopska analiza
urediDMACA reagens je histološka boja specifična za polifenole koji se koriste u mikroskopskim analizama. Autofluorescencija polifenola se također može koristiti, posebno za lokalizaciju lignina i suberina. Tamo gdje je fluorescencija samih molekula nedovoljna za vizualizaciju svjetlosnom mikroskopijom, DPBA (2-aminoetil-ester difenilborne kiseline, koji se također naziva Naturstoffov reagens A) tradicijske se koristi, barem u biljnoj znanosti, za poboljšanje fluorescentnih signala.Greška kod citiranja: Nedostaje oznaka za zatvaranje </ref> nakon <ref>
Kvantifikacija
urediSadržaj polifenola in vitro može se kvantificirati volumetrijskom titracijom. Oksidacijsko sredstvo, permanganat, koristi se za oksidaciju poznatih koncentracija standardnog ratvora tanina, stvarajući standardnu krivu. Sadržaj nepoznatog tanina se tada izražava kao ekvivalent odgovarajućeg hidrolizabilnog ili kondenzovanog tanina.[21]
Neki metodi za kvantifikaciju ukupnog sadržaja polifenola in vitro zasnivaju se na kolorimetrijskim mjerenjima. Neki testovi su relativno specifični za polifenole (naprimjer Porterov test). Ukupni fenoli (ili antioksidativni efekt) mogu se izmjeriti pomoću Folin-Ciocalteuove reakcije.[13] Rezultati se obično izražavaju kao ekvivalenti galne kiseline. Polifenoli se rijetko procjenjuju pomoću tehnologija antitijela.[22]
Ostali testovi mjere antioksidativni kapacitet frakcije. Neki koriste ABTS radikalski kation koji je reaktivan prema većini antioksidansa uključujući fenole, tiole i vitamin C.[23] Tokom ove reakcije, plavi ABTS radikal kationa se ponovo pretvara u svoj bezbojni neutralni oblik. Reakcija se može pratiti spektrofotometrijski. Ovaj test se često naziva test troloks ekvivalentnog antioksidativnog kapaciteta (TEAC). Reaktivnost različitih testiranih antioksidansa upoređena je sa onom kod troloksa, koji je analog vitamina E.
Drugi testovi antioksidativnog kapaciteta koji koriste troloks kao standard uključuju difenilpikrilhidrazil (DPPH), kapacitet apsorpcije kisikovih radikala (ORAC),[24] sposobnost plazmtske redukcije gvožđa (FRAP)[25] assays or inhibition of copper-catalyzed in vitro human low-density lipoprotein oxidation.[26]
Novi metodi. uključujući upotrebu biosenzora, mogu pomoći u praćenju sadržaja polifenola u hrani.[27]
Rezultati kvantitacije proizvedeni pomoću detektor sa diodnim nizom-spregnutog HPLC-a su općenito dati kao relativni, a ne kao apsolutna vrijednost kao kad nedostaju komercijalno dostupni standardi za sve polifenolne molekule.
Biohemija
urediSmatra se da polifenoli imaju različite uloge u ekologiji biljaka. Ove funkcije uključuju:[28]
- Oslobađanje i supresija hormona rasta kao što je auksin.
- UV ekrani za zaštitu od ionizujućeg zračenja i za bojenje (biljni pigmenti).[5]
- Odvraćanje biljojeda (senzorna svojstva).
- Prevencija mikrobnih infekcija (fitoaleksini).[5][29]
- Signalne molekule u sazrevanju i drugim procesima rasta.
Polifenoli uključuju manje dijelove i gradivne blokove od jednostavnijih prirodnih fenola, koji potiču iz fenilpropanoidnog puta za fenolne kiseline ili puta šikimske kiseline galotanina i analoga. Flavonoidi i derivati kafeinske kiseline se biosintetiziraju iz fenilalanina i malonil-CoA. Kompleksni galotanini razvijaju se "in-vitro" oksidacijom 1,2,3,4,6-pentagaloilglukoze ili procesi dimerizacije koji rezultiraju hidrolizabilnim taninima. Za antocijanidine, prekursori kondenzirane biosinteze tanina, dihidroflavonol-reduktaza i leukoantocijanidin-reduktaza (LAR) su ključni enzimi s naknadnim dodatkom katehina i epikatehinskih dijelova za veće, nehidrolizirane dijelove.[30]
Glikozilirani oblik se razvija iz aktivnosti glukoziltransferaze i povećava rastvorljivost polifenola.[31] Polifenol-oksidaza (PPO) je enzim koji katalizuje oksidaciju o-difenola za proizvodnju o-kinona. Brza polimerizacija o-kinona za proizvodnju crnih, smeđih ili crvenih polifenolnih pigmenata uzrokuje posmeđenost voća. Kod insekata, PPO je uključen u stvrdnjavanje zanoktice.[32]
Također pogledajte
urediReference
uredi- ^ a b Quideau S, Deffieux D, Douat-Casassus C, Pouységu L (januar 2011). "Plant polyphenols: chemical properties, biological activities, and synthesis". Angewandte Chemie. 50 (3): 586–621. doi:10.1002/anie.201000044. PMID 21226137.
- ^ a b "Flavonoids". Micronutrient Information Center, Linus Pauling Institute, Oregon State University. 1. 2. 2016. Pristupljeno 28. 10. 2020.
- ^ Nonaka G (1989). "Isolation and structure elucidation of tannins" (PDF). Pure Appl. Chem. 61 (3): 357–360. doi:10.1351/pac198961030357. S2CID 84226096.
- ^ "Polyphenol". Merriam-Webster, Inc. 2019. Pristupljeno 23. 2. 2019.
- ^ a b c Manach C, Scalbert A, Morand C, Rémésy C, Jiménez L (maj 2004). "Polyphenols: food sources and bioavailability". The American Journal of Clinical Nutrition. 79 (5): 727–747. doi:10.1093/ajcn/79.5.727. PMID 15113710.
- ^ Haslam E, Cai Y (januar 1994). "Plant polyphenols (vegetable tannins): gallic acid metabolism". Natural Product Reports. 11 (1): 41–66. doi:10.1039/NP9941100041. PMID 15206456.
- ^ Practical Polyphenolics, Edwin Haslam, 1998, ISBN 0-521-46513-3
- ^ "Cardiovascular disease and phytochemicals. Anonymous. C. Hamilton et al". Arhivirano s originala, 4. 3. 2016. Pristupljeno 16. 12. 2022.
- ^ Martín Santos MA, Bonilla Venceslada JL, Martín Martín A, García García I (2005). "Estimating the selectivity of ozone in the removal of polyphenols from vinasse". Journal of Chemical Technology and Biotechnology. 80 (4): 433–438. doi:10.1002/jctb.1222. INIST:16622840.
- ^ Owen RW, Haubner R, Hull WE, Erben G, Spiegelhalder B, Bartsch H, Haber B (decembar 2003). "Isolation and structure elucidation of the major individual polyphenols in carob fibre". Food and Chemical Toxicology. 41 (12): 1727–1738. doi:10.1016/S0278-6915(03)00200-X. PMID 14563398.
- ^ Escribano-Bailon MT, Santos-Buelga C (2003). "Polyphenol Extraction From Foods" (PDF). u Santos-Buelga C, Williamson G (ured.). Methods in Polyphenol Analysis. Royal Society of Chemistry. str. 1–16. ISBN 978-0-85404-580-8. Arhivirano s originala (PDF), 27. 7. 2011. Pristupljeno 16. 12. 2022.
- ^ Pan X (2003). "Microwave-assisted extraction of tea polyphenols and tea caffeine from green tea leaves". Chemical Engineering and Processing. 42 (2): 129–133. doi:10.1016/S0255-2701(02)00037-5.
- ^ a b c Aizpurua-Olaizola O, Ormazabal M, Vallejo A, Olivares M, Navarro P, Etxebarria N, Usobiaga A (januar 2015). "Optimization of supercritical fluid consecutive extractions of fatty acids and polyphenols from Vitis vinifera grape wastes". Journal of Food Science. 80 (1): E101–E107. doi:10.1111/1750-3841.12715. PMID 25471637.
- ^ Palma M, Taylor LT (juli 1999). "Extraction of polyphenolic compounds from grape seeds with near critical carbon dioxide". Journal of Chromatography A. 849 (1): 117–124. doi:10.1016/S0021-9673(99)00569-5. PMID 10444839.
- ^ Alonso-Salces RM, Korta E, Barranco A, Berrueta LA, Gallo B, Vicente F (novembar 2001). "Pressurized liquid extraction for the determination of polyphenols in apple". Journal of Chromatography A. 933 (1–2): 37–43. doi:10.1016/S0021-9673(01)01212-2. PMID 11758745.
- ^ Sineiro J, Domínguez H, Núñez MJ, Lema JM (1996). "Ethanol extraction of polyphenols in an immersion extractor. Effect of pulsing flow". Journal of the American Oil Chemists' Society. 73 (9): 1121–1125. doi:10.1007/BF02523372. S2CID 96009875.
- ^ Papoutsis, Konstantinos; Pristijono, Penta; Golding, John; Stathopoulos, Costas; Bowyer, Michael; Scarlett, Christopher; Vuong, Quan (2018). "Screening the effect of four ultrasound-assisted extraction parameters on hesperidin and phenolic acid content of aqueous citrus pomace extracts". Food Bioscience. 21: 20–26. doi:10.1016/j.fbio.2017.11.001.
- ^ Papoutsis, Konstantinos; Vuong, Quan; Golding, John; Hasperué, Joaquín; Pristijono, Penta; Bowyer, Michael; Scarlett, Christopher; Stathopoulos, Costas (2018). "Pretreatment of citrus by-products affects polyphenol recovery: a review". Food Reviews International. 34: 770–795. doi:10.1080/87559129.2018.1438471.
- ^ Arranz S, Saura-Calixto F, Shaha S, Kroon PA (august 2009). "High contents of nonextractable polyphenols in fruits suggest that polyphenol contents of plant foods have been underestimated". Journal of Agricultural and Food Chemistry. 57 (16): 7298–7303. doi:10.1021/jf9016652. hdl:10261/82508. PMID 19637929.
- ^ Nawaz H, Shi J, Mittal GS, Kakuda Y (2006). "Extraction of polyphenols from grape seeds and concentration by ultrafiltration". Separation and Purification Technology. 48 (2): 176–181. doi:10.1016/j.seppur.2005.07.006.
- ^ Tempel AS (oktobar 1982). "Tannin-measuring techniques : A review". Journal of Chemical Ecology. 8 (10): 1289–1298. doi:10.1007/BF00987762. PMID 24414735. S2CID 39848160.
- ^ Gani M, Mcguinness BJ, Da Vies AP (1998). "Monoclonal antibodies against tea polyphenols: A novel immunoassay to detect polyphenols in biological fluids". Food and Agricultural Immunology. 10: 13–22. doi:10.1080/09540109809354964.
- ^ Walker RB, Everette JD (februar 2009). "Comparative reaction rates of various antioxidants with ABTS radical cation". Journal of Agricultural and Food Chemistry. 57 (4): 1156–1161. doi:10.1021/jf8026765. PMID 19199590.
- ^ Roy MK, Koide M, Rao TP, Okubo T, Ogasawara Y, Juneja LR (mart 2010). "ORAC and DPPH assay comparison to assess antioxidant capacity of tea infusions: relationship between total polyphenol and individual catechin content". International Journal of Food Sciences and Nutrition. 61 (2): 109–124. doi:10.3109/09637480903292601. PMID 20109129. S2CID 1929167.
- ^ Pulido R, Bravo L, Saura-Calixto F (august 2000). "Antioxidant activity of dietary polyphenols as determined by a modified ferric reducing/antioxidant power assay". Journal of Agricultural and Food Chemistry. 48 (8): 3396–3402. doi:10.1021/jf9913458. hdl:10261/112476. PMID 10956123.
- ^ Meyer AS, Yi OS, Pearson DA, Waterhouse AL, Frankel EN (1997). "Inhibition of Human Low-Density Lipoprotein Oxidation in Relation to Composition of Phenolic Antioxidants in Grapes (Vitis vinifera)". Journal of Agricultural and Food Chemistry. 45 (5): 1638–1643. doi:10.1021/jf960721a.
- ^ Mello LD, Sotomayor MD, Kubota LT (2003). "HRP-based amperometric biosensor for the polyphenols determination in vegetables extract". Sensors and Actuators B: Chemical. 96 (3): 636–645. doi:10.1016/j.snb.2003.07.008.
- ^ V. Lattanzio et al. (2006). "Role of phenolics in the resistance mechanisms of plants against fungal pathogens and insects" Arhivirano 17. 5. 2017. na Wayback Machine (and references therein). Phytochemistry: Advances in Research, 23–67. ISBN 81-308-0034-9.
- ^ Huber B, Eberl L, Feucht W, Polster J (2003). "Influence of polyphenols on bacterial biofilm formation and quorum-sensing". Zeitschrift für Naturforschung C. 58 (11–12): 879–884. doi:10.1515/znc-2003-11-1224. PMID 14713169. S2CID 25764128.
- ^ Tanner GJ, Francki KT, Abrahams S, Watson JM, Larkin PJ, Ashton AR (august 2003). "Proanthocyanidin biosynthesis in plants. Purification of legume leucoanthocyanidin reductase and molecular cloning of its cDNA". The Journal of Biological Chemistry. 278 (34): 31647–31656. doi:10.1074/jbc.M302783200. PMID 12788945.
- ^ Krasnow MN, Murphy TM (juni 2004). "Polyphenol glucosylating activity in cell suspensions of grape (Vitis vinifera)". Journal of Agricultural and Food Chemistry. 52 (11): 3467–3472. doi:10.1021/jf035234r. PMID 15161217.
- ^ Malek SR (1961). "Polyphenols and their quinone derivatives in the cuticle of the desert locust, Schistocerca gregaria (Forskål)". Comparative Biochemistry and Physiology. 2: 35–77. doi:10.1016/0010-406X(61)90071-8.
Vanjski linkovi
uredi- Phenol-Explorer, electronic database of polyphenol content in foods
- Rječnik molekulskih formula prirodnih fenola i polifenola