ORT
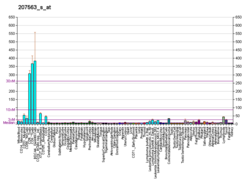
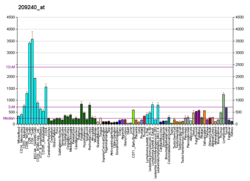
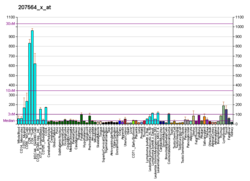
Protein O-GlcNAc transferaza, znana i kao OGT ili O-vezana N-acetilglukozaminiltransferaza je enzim (EC: 2.4.1.255) koji je kod ljudi kodiran genom OGT sa hromosoma X.[5][6] OGT katalizira posttranslacijsko dodavanje O-GlcNAc u proteine.[5][7][8][9][10][11]
Nomenklatura
urediOstali nazivi uključuju:
- O-GlcNAc transferaza
- OGTaza
- O-vezana N-acetilglukozaminiltransferaza
- Uridin difosfo-N-acetilglukozamin:polipeptid β-N-acetilglukozaminiltransferaza
Sistematski naziv: UDP-N-α-acetil-d-glukozamin:[protein]-3-O-N-acetil-β-d-glukozaminil transferaza
Glikoziltransferaza
urediOGT katalizira dodavanje jednog N-acetilglukozamina preko O-glikozidne veze na serin ili treonin i S-glikozidne veze sa cisteinskim[12][13] ostacima nukleocitoplazmatskih proteina. Budući da se i fosforilacija i O-GlcNAcilacija natječu za slične ostatke serina ili treonina, ova dva procesa mogu se nadmetati za mjesta ili mogu promijeniti supstratnu specifičnost obližnjih mjesta sternim ili elektrostatskim efektima. Za ovaj gen su pronađene dvije varijante transkripta koje kodiraju citoplazmatske i mitohondrijske izoforme.[6] OGT glikozilira mnoge proteine uključujući: histon H2B,[14] AKT1,[15] PFKL,[16] KMT2E/MLL5,[16] MAPT/TAU,[17] faktor ćelije domaćina C1,[18] i SIN3A.[19]
O-GlcNAc transferaza je dio niza bioloških funkcija u ljudskom tijelu. OGT je uključen u rezistenciju na insulin u mišićnim ćelijama i adipocit ima, tako što inhibira fosforilaciju treonina 308 AKT1, povećavajući stopu fosforilacija IRS1 (kod serina 307 i serina 632/635), smanjujući insulinsku signalizaciju i glikozilirajuće komponente insulinskih signala.[20] Dodatno, O-GlcNAc transferaza katalizira unutarćelijsku glikozilaciju ostataka serina i treonina uz dodatak N-acetilglukozamina. Studije pokazuju da su OGT aleli vitalni za embriogenezu, te da je OGT neophodan za unutarćelijsku glikozilaciju i vitalnost embrionskih matičnih ćelija.[21] O-GlcNAc transferaza također katalizira posttranslacijsku modifikaciju koja modificira faktore transkripcije i RNK-polimerazu II; međutim specifična funkcija ove modifikacije je uglavnom nepoznata.[22]
OGT cijepa faktor ćelije domaćina C1, u jednoj ili više od 6 ponavljajućih sekvenci od 26 aminokiselina. TPR domen OGT veže se za karboksilni terminalni dio HCF1 proteolitskog ponavljanja tako da je regija cijepanja na aktivnom mjestu glikoziltransferaze iznad uridin-difosfat-GlcNAc [11] Neophodan je veliki dio OGT kompleksa sa HCF1 za cijepanje HCF1, a HCFC1 je potreban za stabilizaciju OGT u jedru. HCF1 reguliše stabilnost OGT, koristeći posttranskripcijski mehanizam, međutim mehanizam interakcije sa HCFC1 je još uvijek nepoznat.[23]
Aminokiselinska sekvenca
urediDužina polipeptidnog lanca je 1.046 aminokiselina, a molekulska težina 116.925 Da.[6]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MASSVGNVAD | STEPTKRMLS | FQGLAELAHR | EYQAGDFEAA | ERHCMQLWRQ | ||||
| EPDNTGVLLL | LSSIHFQCRR | LDRSAHFSTL | AIKQNPLLAE | AYSNLGNVYK | ||||
| ERGQLQEAIE | HYRHALRLKP | DFIDGYINLA | AALVAAGDME | GAVQAYVSAL | ||||
| QYNPDLYCVR | SDLGNLLKAL | GRLEEAKACY | LKAIETQPNF | AVAWSNLGCV | ||||
| FNAQGEIWLA | IHHFEKAVTL | DPNFLDAYIN | LGNVLKEARI | FDRAVAAYLR | ||||
| ALSLSPNHAV | VHGNLACVYY | EQGLIDLAID | TYRRAIELQP | HFPDAYCNLA | ||||
| NALKEKGSVA | EAEDCYNTAL | RLCPTHADSL | NNLANIKREQ | GNIEEAVRLY | ||||
| RKALEVFPEF | AAAHSNLASV | LQQQGKLQEA | LMHYKEAIRI | SPTFADAYSN | ||||
| MGNTLKEMQD | VQGALQCYTR | AIQINPAFAD | AHSNLASIHK | DSGNIPEAIA | ||||
| SYRTALKLKP | DFPDAYCNLA | HCLQIVCDWT | DYDERMKKLV | SIVADQLEKN | ||||
| RLPSVHPHHS | MLYPLSHGFR | KAIAERHGNL | CLDKINVLHK | PPYEHPKDLK | ||||
| LSDGRLRVGY | VSSDFGNHPT | SHLMQSIPGM | HNPDKFEVFC | YALSPDDGTN | ||||
| FRVKVMAEAN | HFIDLSQIPC | NGKAADRIHQ | DGIHILVNMN | GYTKGARNEL | ||||
| FALRPAPIQA | MWLGYPGTSG | ALFMDYIITD | QETSPAEVAE | QYSEKLAYMP | ||||
| HTFFIGDHAN | MFPHLKKKAV | IDFKSNGHIY | DNRIVLNGID | LKAFLDSLPD | ||||
| VKIVKMKCPD | GGDNADSSNT | ALNMPVIPMN | TIAEAVIEMI | NRGQIQITIN | ||||
| GFSISNGLAT | TQINNKAATG | EEVPRTIIVT | TRSQYGLPED | AIVYCNFNQL | ||||
| YKIDPSTLQM | WANILKRVPN | SVLWLLRFPA | VGEPNIQQYA | QNMGLPQNRI | ||||
| IFSPVAPKEE | HVRRGQLADV | CLDTPLCNGH | TTGMDVLWAG | TPMVTMPGET | ||||
| LASRVAASQL | TCLGCLELIA | KNRQEYEDIA | VKLGTDLEYL | KKVRGKVWKQ | ||||
| RISSPLFNTK | QYTMELERLY | LQMWEHYAAG | NKPDHMIKPV | EVTESA |
Struktura
urediLjudski OGT gen ima 1046 aminokiselinskih ostataka i heterotrimer je koji se sastoji od dvije podjedinice i jedne podjedinice od 78 kDa.[9] Podjedinica od 110 kDa sadrži 13 tetratricopeptidna ponavljanja (TPR); 13. ponavljanje je skraćeno. Ove podjedinice su dimerizovane TPR ponavljanjima 6 i 7. OGT je visoko eksprimiran u pankreasu, a također je izražen u srcu, mozgu, skeletnim mišićima i posteljici. Pronađene su količine u tragovima u plućima i jetri.[5] Mjesta vezivanja su određena za podjedinicu od 110 kDa. Ima 3 mjesta vezivanja na aminokiselinskim ostacima 849, 852 i 935. Vjerovatno aktivno mjesto je na ostatku 508.[16]
Kristalna struktura O-GlcNAc transferaze nije dobro proučena, ali struktura binarnog kompleksa sa UDP i ternarnog kompleksa sa UDP i peptidnim supstratom je eksprimiran.[11] OGT-UDP kompleks sadrži tri domena u svom katalitsčkom regionu: amino N-kraj|(''N'')- terminalni domen, karboksi (C)-terminalni domen i intervencioni domen (Int-D). Katalitska regija je povezana sa TPR ponavljanjima translacijskom spiralom (H3), koja se kreće od C-cat domena do N-cat domena, duž gornje površine katalitske regije.[11] OGT-UDP-peptidni kompleks ima veći prostor između TPR domena i katalitske regije OGT-UDP kompleksa. CKII peptid, koji sadrži tri serinska ostatka i jedan treoninski ostatak, vezuje se u ovom prostoru. U 2021., analiza CryoEM od 5Å otkrila je odnos između katalitskih domena [24] i netaknuti TPR regioni koji potvrđuju raspored dimera koji je prvi put viđen u samoj TPR strukturi X-zraka. Ova struktura podržava uređeni sekvencni bi-bi mehanizam koji se poklapa s činjenicom da je „pri zasićenim koncentracijama peptida, konkurentska inhibicija uzoraka dobijenih za UDP u odnosu na UDP-GlcNAc.”[11]
Funkcija
uredi| O-GlcNAc transferaza | |
|---|---|
| Struktura superheliksnog TPR domena O-vezane GlcNAc transferaze (generirane iz PyMOL-a) | |
| Identifikatori | |
| Simbol | O-GlcNac-trans |
Glikoziltransferaza
urediOGT katalizira dodavanje jednog N-acetilglukozamina preko O-glikozidne veze na serin ili treonin i S-glikozidne veze sa cisteinskim[12][13] ostacima nukleocitoplazmatskih proteina. Budući da se i fosforilacija i O-GlcNAcilacija natječu za slične ostatke serina ili treonina, ova dva procesa mogu se nadmetati za mjesta ili mogu promijeniti supstratnu specifičnost obližnjih mjesta sternim ili elektrostatskim efektima. Za ovaj gen su pronađene dvije varijante transkripta koje kodiraju citoplazmatske i mitohondrijske izoforme.[6] OGT glikozilira mnoge proteine uključujući: histon H2B,[14] AKT1,[15] PFKL,[16] KMT2E/MLL5,[16] MAPT/TAU,[17] faktor ćelije domaćina C1,[18] i SIN3A.[19]
O-GlcNAc transferaza je dio niza bioloških funkcija u ljudskom tijelu. OGT je uključen u rezistenciju na insulin u mišićnim ćelijama i adipocit ima, tako što inhibira fosforilaciju treonina 308 AKT1, povećavajući stopu fosforilacija IRS1 (kod serina 307 i serina 632/635), smanjujući insulinsku signalizaciju i glikozilirajuće komponente insulinskih signala.[20] Dodatno, O-GlcNAc transferaza katalizira unutarćelijsku glikozilaciju ostataka serina i treonina uz dodatak N-acetilglukozamina. Studije pokazuju da su OGT aleli vitalni za embriogenezu, te da je OGT neophodan za unutarćelijsku glikozilaciju i vitalnost embrionskih matičnih ćelija.[21] O-GlcNAc transferaza također katalizira posttranslacijsku modifikaciju koja modificira faktore transkripcije i RNK-polimerazu II; međutim specifična funkcija ove modifikacije je uglavnom nepoznata.[22]
OGT cijepa faktor ćelije domaćina C1, u jednoj ili više od 6 ponavljajućih sekvenci od 26 aminokiselina. TPR domen OGT veže se za karboksilni terminalni dio HCF1 proteolitskog ponavljanja tako da je regija cijepanja na aktivnom mjestu glikoziltransferaze iznad uridin-difosfat-GlcNAc [11] Neophodan je veliki dio OGT kompleksa sa HCF1 za cijepanje HCF1, a HCFC1 je potreban za stabilizaciju OGT u jedru. HCF1 reguliše stabilnost OGT, koristeći posttranskripcijski mehanizam, međutim mehanizam interakcije sa HCFC1 je još uvijek nepoznat.[23]
Mehanizam katalize
urediMolekulski mehanizam "O"-vezane "N"-acetilglukozamin transferaze također nije opširno proučavan, jer ne postoji potvrđena kristalna struktura enzima. Mehanizam koji su predložili Lazarus et al. je podržan obrascima inhibicije proizvoda UDP-a u uslovima zasićenja peptida. Ovaj mehanizam se odvija sa polaznim materijalima uridin-difosfat N-acetilglukozaminam i peptidni lancima sa reaktivnom serinskom ili treoninskom hidroksil grupom. Predložena reakcija je uređeni sekvencni bi-bi mehanizam.[11]
Hemijska reakcija se može zapisati kao:
- UDP-N-acetil-D-glukozamin + [protein]-L-treonin → UDP + [protein]-3-O -(N-acetil-D-glukozaminil)-L-treonin
Prvo, hidroksilnu grupu serina deprotonira histidin 498, katalitska baza u ovoj predloženoj reakciji. Lizin 842 je također prisutan da stabilizuje UDP oblast. Kisikov ion tada napada šećer-fosfatnu vezu između glukozamina i UDP-a. Ovo rezultira cijepanjem UDP-N-acetilglukozamina na N-acetilglukozamin – peptid i UDP. Protonski transferi odvijaju se na fosfatu i histidinu 498. Ovaj mehanizam je podstaknut OGT genom koji sadrži O-vezanu N-acetilglukozamin transferazu. Osim prijenosa protona, reakcija se odvija u jednom koraku, kao što je prikazano na slici 2.[11] Slika 2 koristi usamljeni ostatak serina kao predstavnika peptida sa reaktivnom hidroksilnom grupom. Treonin je također mogao biti korišten u mehanizmu.
Inhibitori
urediPrijavljeni su mnogi inhibitori enzimske aktivnosti OGT. Inhibicija OGT dovodi do globalne regulacije O-GlcNAc. Čini se da ćelije pojačavaju OGT i reduciraju OGA kao odgovor na inhibiciju OGT.[26]
5S-GlcNAc
urediAc45S-GlcNAc se unutarćelijsk pretvara u UDP-5S-GlcNAc, analogni inhibitor supstrata OGT-a. UDP-5S-GlcNAc se ne koristi efikasno kao donatorski šećer od strane OGT-a, vjerovatno zbog izobličenja piranoznog prstena, zamjenom kisika sumporom.[26] Kao što se koriste druge glikoziltransferaze UDP-GlcNAc kao donatorski šećer, UDP-5S-GlcNAc ima neke nespecifične efekte na glikozilaciju na površini ćelije.[27]
OSMI
urediOSMI-1 je prvi put identificiran iz visokopropusnog skrininga, korištenjem fluorescentne polarizacije.[27] Dalja optimizacija dovela je do razvoja OSMI-2, OSMI-3 i OSMI-4, koji vezuju OGT sa niskim nanomolarnim afinitetom. Rentgenska kristalografija je pokazala da kinolinon-6-sulfonamidni okvir spoja OSMI djeluje kao uridinov mimetik. OSMI-2, OSMI-3 i OSMI-4 imaju negativno nabijene karboksilatne grupe; esterifikacija čini ove inhibitore propusnim za ćelije.[28]
Regulacija
urediO-GlcNAc transferaza je dio dinamičke konkurencije za serinsku ili treoninsku hidroksilnu funkcionalnu grupu u peptidnoj jedinici. Slika 3 prikazuje primjer recipročne zauzetosti istog i susjednog mjesta. Za zauzetost istog mjesta, OGT se takmiči sa kinazom da katalizira glikozilaciju proteina umjesto fosforilacije. Primjer zauzetosti susjednog mjesta pokazuje da se goli protein kataliziran OGT pretvara u glikoprotein, koji može povećati promet proteina kao što je tumorski represor p53.[29]
Posttranslacijska modifikacija proteina pomoću O-GlcNAc je podstaknuta protokom glukoze kroz biosintetski put heksozamina. OGT katalizira vezivanje O-GlcNAc grupe za serin i treonin, dok O-GlcNAcase podstiče uklanjanje šećera.[30][31] Ova regulacija je važna za višestruke ćelijske procese uključujući transkripciju, transdukciju signala i proteasomsku degradaciju. Također, postoji kompetitivna regulacija između OGT i kinaze da se protein veže na fosfatnu grupu ili O-GlcNAc, koji može promijeniti funkciju proteina u tijelu kroz nizvodne efekte.[16][30] OGT inhibira aktivnost 6-fosofuktosekinaze PFKL posredovanjem u procesu glikozilacija. To onda djeluje kao dio regulacije glikolize. O-GlcNAc je definiran kao negativni regulator transkripcije, kao odgovor na signalizaciju steroidnih hormona.[20]
Studije pokazuju da O-GlcNAc transferaza stupa u direktnu interakciju sa enzimom Ten eleven translokacije 2 (TET2), koji pretvara 5-metilcitozin u 5-hidroksimetilcitozin i reguliše transkripciju gena.[32] Dodatno, povećanje nivoa OGT za O-GlcNacilaciju može imati terapeutske efekte za pacijente sa Alzheimerovom bolešću. Metabolizam glukoze u mozgu je poremećen kod Alzheimerove bolesti, a studija sugeriše da to dovodi do hiperfosforilacije tau i degeneracije tau O-GlcNCAcilacije. Dopuna tau O-GlcNacilacije u mozgu zajedno s protein fosfatazom može spriječiti ovaj proces i poboljšati metabolizam glukoze u mozgu.[17]
Također pogledajte
urediReference
uredi- ^ a b c GRCh38: Ensembl release 89: ENSG00000147162 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000034160 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c Lubas WA, Frank DW, Krause M, Hanover JA (april 1997). "O-Linked GlcNAc transferase is a conserved nucleocytoplasmic protein containing tetratricopeptide repeats". The Journal of Biological Chemistry. 272 (14): 9316–24. doi:10.1074/jbc.272.14.9316. PMID 9083068.
- ^ a b c d "Entrez Gene: OGT O-linked N-acetylglucosamine (GlcNAc) transferase (UDP-N-acetylglucosamine:polypeptide-N-acetylglucosaminyl transferase)".
- ^ Banerjee S, Robbins PW, Samuelson J (april 2009). "Molecular characterization of nucleocytosolic O-GlcNAc transferases of Giardia lamblia and Cryptosporidium parvum". Glycobiology. 19 (4): 331–6. doi:10.1093/glycob/cwn107. PMC 2733775. PMID 18948359.
- ^ Clarke AJ, Hurtado-Guerrero R, Pathak S, Schüttelkopf AW, Borodkin V, Shepherd SM, et al. (oktobar 2008). "Structural insights into mechanism and specificity of O-GlcNAc transferase". The EMBO Journal. 27 (20): 2780–8. doi:10.1038/emboj.2008.186. PMC 2556091. PMID 18818698.
- ^ a b Haltiwanger RS, Blomberg MA, Hart GW (maj 1992). "Glycosylation of nuclear and cytoplasmic proteins. Purification and characterization of a uridine diphospho-N-acetylglucosamine:polypeptide beta-N-acetylglucosaminyltransferase". The Journal of Biological Chemistry. 267 (13): 9005–13. doi:10.1016/S0021-9258(19)50380-5. PMID 1533623.
- ^ Rao FV, Dorfmueller HC, Villa F, Allwood M, Eggleston IM, van Aalten DM (april 2006). "Structural insights into the mechanism and inhibition of eukaryotic O-GlcNAc hydrolysis". The EMBO Journal. 25 (7): 1569–78. doi:10.1038/sj.emboj.7601026. PMC 1440316. PMID 16541109.
- ^ a b c d e f g h i Lazarus MB, Nam Y, Jiang J, Sliz P, Walker S (januar 2011). "Structure of human O-GlcNAc transferase and its complex with a peptide substrate". Nature. 469 (7331): 564–7. Bibcode:2011Natur.469..564L. doi:10.1038/nature09638. PMC 3064491. PMID 21240259.
- ^ a b Maynard JC, Burlingame AL, Medzihradszky KF (novembar 2016). "Cysteine S-linked N-acetylglucosamine (S-GlcNAcylation), A New Post-translational Modification in Mammals". Molecular & Cellular Proteomics. 15 (11): 3405–3411. doi:10.1074/mcp.M116.061549. PMC 5098038. PMID 27558639.
- ^ a b Gorelik A, Bartual SG, Borodkin VS, Varghese J, Ferenbach AT, van Aalten DM (novembar 2019). "Genetic recoding to dissect the roles of site-specific protein O-GlcNAcylation". Nature Structural & Molecular Biology. 26 (11): 1071–1077. doi:10.1038/s41594-019-0325-8. PMC 6858883. PMID 31695185.
- ^ a b Fujiki R, Hashiba W, Sekine H, Yokoyama A, Chikanishi T, Ito S, et al. (novembar 2011). "GlcNAcylation of histone H2B facilitates its monoubiquitination". Nature. 480 (7378): 557–60. Bibcode:2011Natur.480..557F. doi:10.1038/nature10656. PMC 7289526. PMID 22121020.
- ^ a b Whelan SA, Dias WB, Thiruneelakantapillai L, Lane MD, Hart GW (februar 2010). "Regulation of insulin receptor substrate 1 (IRS-1)/AKT kinase-mediated insulin signaling by O-Linked beta-N-acetylglucosamine in 3T3-L1 adipocytes". The Journal of Biological Chemistry. 285 (8): 5204–11. doi:10.1074/jbc.M109.077818. PMC 2820748. PMID 20018868.
- ^ a b c d e f "O15294 (OGT1_HUMAN) Reviewed, UniProtKB/Swiss-Prot". UniProt.
- ^ a b c Liu F, Shi J, Tanimukai H, Gu J, Gu J, Grundke-Iqbal I, et al. (juli 2009). "Reduced O-GlcNAcylation links lower brain glucose metabolism and tau pathology in Alzheimer's disease". Brain. 132 (Pt 7): 1820–32. doi:10.1093/brain/awp099. PMC 2702834. PMID 19451179.
- ^ a b Wysocka J, Myers MP, Laherty CD, Eisenman RN, Herr W (april 2003). "Human Sin3 deacetylase and trithorax-related Set1/Ash2 histone H3-K4 methyltransferase are tethered together selectively by the cell-proliferation factor HCF-1". Genes & Development. 17 (7): 896–911. doi:10.1101/gad.252103. PMC 196026. PMID 12670868.
- ^ a b Yang X, Zhang F, Kudlow JE (juli 2002). "Recruitment of O-GlcNAc transferase to promoters by corepressor mSin3A: coupling protein O-GlcNAcylation to transcriptional repression". Cell. 110 (1): 69–80. doi:10.1016/S0092-8674(02)00810-3. PMID 12150998.
- ^ a b c Yang X, Ongusaha PP, Miles PD, Havstad JC, Zhang F, So WV, et al. (februar 2008). "Phosphoinositide signalling links O-GlcNAc transferase to insulin resistance". Nature. 451 (7181): 964–9. Bibcode:2008Natur.451..964Y. doi:10.1038/nature06668. PMID 18288188. S2CID 18459576.
- ^ a b Shafi R, Iyer SP, Ellies LG, O'Donnell N, Marek KW, Chui D, et al. (maj 2000). "The O-GlcNAc transferase gene resides on the X chromosome and is essential for embryonic stem cell viability and mouse ontogeny". Proceedings of the National Academy of Sciences of the United States of America. 97 (11): 5735–9. Bibcode:2000PNAS...97.5735S. doi:10.1073/pnas.100471497. PMC 18502. PMID 10801981.
- ^ a b Chen Q, Chen Y, Bian C, Fujiki R, Yu X (januar 2013). "TET2 promotes histone O-GlcNAcylation during gene transcription". Nature. 493 (7433): 561–4. Bibcode:2013Natur.493..561C. doi:10.1038/nature11742. PMC 3684361. PMID 23222540.
- ^ a b Daou S, Mashtalir N, Hammond-Martel I, Pak H, Yu H, Sui G, et al. (februar 2011). "Crosstalk between O-GlcNAcylation and proteolytic cleavage regulates the host cell factor-1 maturation pathway". Proceedings of the National Academy of Sciences of the United States of America. 108 (7): 2747–52. Bibcode:2011PNAS..108.2747D. doi:10.1073/pnas.1013822108. PMC 3041071. PMID 21285374.
- ^ Meek, Richard W.; Blaza, James N.; Busmann, Jil A.; Alteen, Matthew G.; Vocadlo, David J.; Davies, Gideon J. (11. 11. 2021). "Cryo-EM structure provides insights into the dimer arrangement of the O-linked β-N-acetylglucosamine transferase OGT". Nature Communications (jezik: engleski). 12 (1): 6508. Bibcode:2021NatCo..12.6508M. doi:10.1038/s41467-021-26796-6. ISSN 2041-1723. PMC 8586251 Provjerite vrijednost parametra
|pmc=(pomoć). PMID 34764280 Provjerite vrijednost parametra|pmid=(pomoć). - ^ Jínek M, Rehwinkel J, Lazarus BD, Izaurralde E, Hanover JA, Conti E (oktobar 2004). "The superhelical TPR-repeat domain of O-linked GlcNAc transferase exhibits structural similarities to importin alpha". Nature Structural & Molecular Biology. 11 (10): 1001–7. doi:10.1038/nsmb833. PMID 15361863.
- ^ a b Gloster TM, Zandberg WF, Heinonen JE, Shen DL, Deng L, Vocadlo DJ (mart 2011). "Hijacking a biosynthetic pathway yields a glycosyltransferase inhibitor within cells". Nature Chemical Biology. 7 (3): 174–81. doi:10.1038/nchembio.520. PMC 3202988. PMID 21258330.
- ^ a b Ortiz-Meoz RF, Jiang J, Lazarus MB, Orman M, Janetzko J, Fan C, et al. (juni 2015). "A small molecule that inhibits OGT activity in cells". ACS Chemical Biology. 10 (6): 1392–7. doi:10.1021/acschembio.5b00004. PMC 4475500. PMID 25751766.
- ^ Martin SE, Tan ZW, Itkonen HM, Duveau DY, Paulo JA, Janetzko J, et al. (oktobar 2018). "Structure-Based Evolution of Low Nanomolar O-GlcNAc Transferase Inhibitors". Journal of the American Chemical Society. 140 (42): 13542–13545. doi:10.1021/jacs.8b07328. PMC 6261342. PMID 30285435.
- ^ a b Hart GW, Housley MP, Slawson C (april 2007). "Cycling of O-linked beta-N-acetylglucosamine on nucleocytoplasmic proteins". Nature. 446 (7139): 1017–22. Bibcode:2007Natur.446.1017H. doi:10.1038/nature05815. PMID 17460662. S2CID 4392021.
- ^ a b Yang X, Su K, Roos MD, Chang Q, Paterson AJ, Kudlow JE (juni 2001). "O-linkage of N-acetylglucosamine to Sp1 activation domain inhibits its transcriptional capability". Proceedings of the National Academy of Sciences of the United States of America. 98 (12): 6611–6. Bibcode:2001PNAS...98.6611Y. doi:10.1073/pnas.111099998. PMC 34401. PMID 11371615.
- ^ Love DC, Hanover JA (novembar 2005). "The hexosamine signaling pathway: deciphering the "O-GlcNAc code"". Science's STKE. 2005 (312): re13. doi:10.1126/stke.3122005re13. PMID 16317114. S2CID 29082840.
- ^ Tahiliani M, Koh KP, Shen Y, Pastor WA, Bandukwala H, Brudno Y, et al. (maj 2009). "Conversion of 5-methylcytosine to 5-hydroxymethylcytosine in mammalian DNA by MLL partner TET1". Science. 324 (5929): 930–5. Bibcode:2009Sci...324..930T. doi:10.1126/science.1170116. PMC 2715015. PMID 19372391.
Vanjski linkovi
urediThe O-GlcNAc Database[1][2] - A curated database for protein O-GlcNAcylation and referencing more than 14 000 protein entries and 10 000 O-GlcNAc sites.
- Protein O-GlcNAc transferase na US National Library of Medicine Medical Subject Headings (MeSH)
- ^ Wulff-Fuentes E, Berendt RR, Massman L, Danner L, Malard F, Vora J, Kahsay R, Olivier-Van Stichelen S (januar 2021). "The human O-GlcNAcome database and meta-analysis". Scientific Data. 8 (1): 25. Bibcode:2021NatSD...8...25W. doi:10.1038/s41597-021-00810-4. PMC 7820439. PMID 33479245.
- ^ Malard F, Wulff-Fuentes E, Berendt RR, Didier G, Olivier-Van Stichelen S (juli 2021). "Automatization and self-maintenance of the O-GlcNAcome catalog: a smart scientific database". Database (Oxford). 2021: 1. doi:10.1093/database/baab039. PMC 8288053 Provjerite vrijednost parametra
|pmc=(pomoć). PMID 34279596 Provjerite vrijednost parametra|pmid=(pomoć).