Lipoprotein lipaza
Lipoprotein-lipaza (LPL) (EC 3.1.1.34) je enzim koji je kod ljudi kodiran genom LPL. Čan je porodice lipaznih gena, koja uključuje gušteračnu, jetrenu i endotelnu lipazu. Topiv je u vodi a hidrolizita trigliceride u lipoproteine, poput onih koji se nalaze u hilomikronima i lipoproteinima vrlo niske gustoće (VLDL), u dvije slobodne masne kiseline i jednu monoacilglicerol molekulu. Također je uključen u podstcanje ćelijske apsorpcije hilomikronskih ostataka, lipoproteina bogatih olesterolom i slobodnih masnih kiselina.[5][6][7] LPL zahtijeva ApoC-II kao kofaktor.[8][9]
| Lipoprotein-lipaza | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifikatori | |||||||||
| EC broj | 3.1.1.34 | ||||||||
| CAS broj | 9004-02-8 | ||||||||
| Baze podataka | |||||||||
| IntEnz | IntEnz pregled | ||||||||
| BRENDA | BRENDA unos | ||||||||
| ExPASy | NiceZyme pregled | ||||||||
| KEGG | KEGG unos | ||||||||
| MetaCyc | metabolički put | ||||||||
| PRIAM | profil | ||||||||
| PDB strukture | RCSB PDB PDBj PDBe PDBsum | ||||||||
| Ontologija gena | AmiGO / QuickGO | ||||||||
| |||||||||
LPL je pričvršćen na lumensku površinu endotelnih ćelija u kapilarima, HDL-vezujućim glikozilfosfatidilinozitol proteinom 1 (GPIHBP1) i heparan-sulfatiranim peptidoglikanima.[10] Najraširenije je u masnom, srčanom i skeletnomišićnom tkivu, kao i u mliječnim žlijezdama u laktaciji.[11][12][13]
Aminokiselinska sekvenca
urediDužina polipeptidnog lanca je 455 aminokiselina, а molekulska težina 53.162 Da.[14]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MESKALLVLT | LAVWLQSLTA | SRGGVAAADQ | RRDFIDIESK | FALRTPEDTA | ||||
| EDTCHLIPGV | AESVATCHFN | HSSKTFMVIH | GWTVTGMYES | WVPKLVAALY | ||||
| KREPDSNVIV | VDWLSRAQEH | YPVSAGYTKL | VGQDVARFIN | WMEEEFNYPL | ||||
| DNVHLLGYSL | GAHAAGIAGS | LTNKKVNRIT | GLDPAGPNFE | YAEAPSRLSP | ||||
| DDADFVDVLH | TFTRGSPGRS | IGIQKPVGHV | DIYPNGGTFQ | PGCNIGEAIR | ||||
| VIAERGLGDV | DQLVKCSHER | SIHLFIDSLL | NEENPSKAYR | CSSKEAFEKG | ||||
| LCLSCRKNRC | NNLGYEINKV | RAKRSSKMYL | KTRSQMPYKV | FHYQVKIHFS | ||||
| GTESETHTNQ | AFEISLYGTV | AESENIPFTL | PEVSTNKTYS | FLIYTEVDIG | ||||
| ELLMLKLKWK | SDSYFSWSDW | WSSPGFAIQK | IRVKAGETQK | KVIFCSREKV | ||||
| SHLQKGKAPA | VFVKCHDKSL | NKKSG |
Struktura
urediPrijavljene su kristalne strukture LPL kompleksa sa GPIHBP1.[15][16] LPL se sastoji od dvije različite regije: većeg N-terminalnog domena koji sadrži lipolizno aktivno mjesto i manji C-terminalni domen. Ove dvije regije povezane su peptidnim linkerom. N-krajnji domen ima α/β hidrolazno savijanje, koje je globulasta struktura sa centralnim β listom okruženim α heliksima. C-terminalni domen je β sendvič, formiran od dva β sloja i podsjeća na izduženi cilindar.
Sinteza
urediUkratko, LPL se luče parenhimske ćelije srca, mišića i masnog tkiva, kao glikozilirani homodimer, nakon čega se translocira kroz vanćelijski matriks i, preko endotelnih ćelija, u lumen kapilara . Nakon translacije, novosintetizirani protein se glikozilira u endoplazmatskom retikulumu. Mjesta glikozilacija LPL-a su Asn-43, Asn-257 i Asn-359.[5] Glukozidaze zatim uklanjaju terminalne ostatke glukoze; nekad se vjerovalo da je ovo podrezivanje glukoze odgovorno za konformacijske promjene potrebne da LPL formira homodimere i postane katalitski aktivan.[5][13][17][18] U Golgijevom aparatu, oligosaharidi se dalje mijenjaju, kako bi rezultirali ili dva složena lanca, ili dva složena i jednim lancem sa visokom manozom.[5][13] In the final protein, carbohydrates account for about 12% of the molecular mass (55-58 kDa).[5][13][19]
Prije nego što se LPL može izlučiti iz ćrlija, potrebna je homodimerizacija.[19][20] Nakon sekrecije, LPL se prenosi kroz endotelne ćelije i uvodi u lumen kapilara, pomoću proteina glikozilfosfatidilinositolskog usidrenog proteina velike gustoće koji veže lipoprotein 1.[21][22]
Mehanizam
urediN-terminalni domeni plave boje, C-terminalni domeni narandžasti.
Područje poklopca koje blokira aktivno mjesto prikazano je tamno plavo.
Triglicerid se veže za C-terminalni domen i područje kapaka, izazivajući promjenu konformacije u LPL-u kako bi aktivno mjesto bilo dostupno.
Aktivno mjesto LPL-a sastoji se od konzervirane trijade Ser-132, Asp-156 i His-241. Ostala važna područja N-terminalnog domena za katalizu uključuju oksijanionsku rupu (Trp-55, Leu-133), područje poklopca (ostaci 216-239), kao i petlju β5 (ostaci 54-64 ).[5][11][18] Mjesto vezivanja ApoC-II još je nepoznato, ali se predviđa da su za nastanak ove interakcije potrebni ostaci i na N- i na C-terminalnim domenama. C-terminalni domen daje specifičnost LPL supstrata; ima veći afinitet za velike lipoproteine bogate triacilgliceridima od lipoproteina bogatih holesterolom.[23] C-terminalni domen je također važan za vezivanje za receptore LDL.[24] I N- i C-terminalni domeni sadrže heparinska mjesta vezivanja, distalno od mjesta vezivanja lipida; LPL stoga služi kao most između ćelijske površine i lipoproteina. Važno je da vezanje LPL-a na ćelijskuu površinu ili receptore ne ovisi o njegovoj katalitskoj aktivnosti.[25]
LPL nekovalentni homodimer ima raspored monomera od glave do repa. Ser /Asp /His trijada je u hidrofobnom utoru koji je poklopcem blokiran od rastvarača. Nakon vezivanja za ApoC-II i lipida u lipoprotein, C-terminalni domen predstavlja lipidni supstrat u području kapaka. Lipid stupa u interakciju i s pokrovom i sa hidrofobnim žlijebom na aktivnom mjestu; ovo uzrokuje pomicanje poklopca, pružajući pristup aktivnom mjestu. Petlja β5 se presavija natrag u jezgo proteina, dovodeći jedan od elektrofila oksijanionske rupe u položaj za lipolizu. Glicerolska okosnica lipida tada može ući aktivno mjesto i hidrolizirati se.
Za svaki LPL dimer mogu se vezati po dvije molekule ApoC-II.[26] Procjenjuje se da na jedan lipoprotein može istovremeno djelovati do četrdeset LPL dimera.[5] Što se tiče kinetike, vjeruje se da je puštanje proizvoda u promet u koraka ograničavanja brzine reakcije.[11]
Funkcija
urediLPL gen kodira lipoprotein-lipazu koja se eksprimira u srcu, mišićima i masnom tkivu.[27][28] LPL funkcionira kao homodimer i ima dvostruke funkcije triglicerid-hidrolaze i ligand/premošćujućeg faktora za receptorski posredovanu apsorpciju lipoproteina. Putem katalize, VLDL se pretvara u IDL, a zatim u LDL. Teške mutacije koje uzrokuju nedostatak LPL rezultiraju hiperlipoproteinemijom tipa I, dok su manje ekstremne mutacije u LPL povezane s mnogim poremećajima metabolizma lipoproteina.[29]
Regulacija
urediLPL se kontrolira transkripcijski i posttranskripcijski.[30] Cirkadijski sat može biti važan u kontroli nivoa Lpl-ove iRNK u perifernim tkivima.[31]
LPL izozimi se različito reguliraju, ovisno o tkivu. Naprimjer, poznato je da insulin aktivira LPL u adipocitima i njegovo postavljanje u endotel kapilara. Nasuprot tome, pokazalo se da insulin smanjuje ekspresiju mišićnih LPL.[32] Umjesto toga, mišićne i miokardne LPL aktiviraju glukagon i adrenalin. Ovo pomaže objašnjnu zašto se tokom posta aktivnost LPL povećava u mišićnom tkivu, a smanjuje u masnom tkivu, dok se nakon obroka događa suprotno.[5][13]
U skladu s tim, makronutrijenti u prehrani različito utiču na aktivnost LPL masti i mišića. Nakon 16 dana na dijeti s visokim udjelom ugljikohidrata ili s visokim udjelom masti, aktivnost LPL značajno se povećala u oba tkiva, šestr sati nakon obroka bilo kojeg sastava, ali došlo je i do značajno većeg porasta LPL u masnom tkivu, kao odgovor na dijetu s visokim udjelom ugljikohidrata u odnosu na ishranu bogatu mastima. Nije bilo razlike između učinaka dviju dijeta na osjetljivost na insulin ili aktivnost LPL natašte u bilo kojem tkivu.[33]
Koncentracija LPL prikazana na površini endotelnih ćelija ne može se regulirati endotelnim ćelijama, jer niti sintetiziraju niti razgrađuju LPL. Umjesto toga, do ove regulacije dolazi upravljanjem protokom LPL-a koji stiže na lipolitsko mjesto i reguliranjem aktivnosti LPL-a prisutnog na endotelu. Ključni protein uključen u kontrolu aktivnosti LPL je ANGPTL4, koji služi kao lokalni inhibitor LPL. Indukcija ANGPTL4 objašnjava inhibiciju aktivnosti LPL -a u bijelom masnom tkivu tokom gladovanja. Sve veći dokazi impliciraju ANGPTL4 u fiziološkoj regulaciji aktivnosti LPL u različitim tkivima.[34]
Za objašnjenje varijacija aktivnosti LPL-a tokom ciklusa brzog hranjenja, predložen je model ANGPTL3-4-8.[35] Konkretno, hranjenje inducira ANGPTL8, aktivirajući put ANGPTL8-ANGPTL3, koji inhibira LPL u srčanim i skeletnim mišićima, čime se cirkulirajući trigliceridi stavljaju na raspolaganje za unos u bijelo masno tkivo, u kojem je aktivnost LPL povećana zbog smanjenja ANGPTL4; obrnuto je za vrijeme posta, koji potiskuje ANGPTL8, ali inducira ANGPTL4, usmjeravajući tako trigliceride u mišiće. Model predlaže opći okvir za reguliranje prometa triglicerida.[35]
Klinički značaj
urediNedostatak lipoprotein lipaze dovodi do hipertrigliceridemije (povišenih nivoa triglicerida u krvotoku).[36] U miševa je pokazano da prekomjerna ekspresija LPL uzrokuje otpornost na insulin,[37][38] i podstiče gojaznost.[31]
Odgovor na visoku razinu LPL masnog tkiva pri dijeti bogatoj ugljikohidratima može predisponirati povećanje masnoće. Jedno istraživanje pokazalo je da su ispitanici dobili više tjelesne masti u sljedeće četiri godine ako su, nakon dijete s visokim udjelom ugljikohidrata i obroka bogatog ugljikohidratima, odgovorili povećanjem aktivnosti LPL masnog tkiva po adipocitu ili smanjenjem koštanog tkiva mišićna LPL aktivnost po gramu tkiva.[39]
Pokazalo se da je ekspresija LPL prognostički prediktor u hroničnu limfocitnu leukemiju.[40] Čini se da u ovom krvnom poremećaju LPL daje masne kiseline, kao izvor energije malignim ćelijama.[41] Stoga se povišeni nivoi LPL-ove iRNK ili proteina smatraju pokazateljima loše prognoze.[42][43][44][45][46][47][48][49][50][51]
Interakcije
urediPokazalo se da lipoprotein-lipaza stupa u interakciju sa LRP1.[52][53][54] Također je ligand za α2M, GP330 i VLDL receptore.[24] Pokazalo se da je LPL ligand za LRP2, iako sa manjim afinitetom nego za druge receptore; međutim, većina degradacije VLDL-a ovisne o LPL-u može se pripisati putu LRP2.[24] U svakom slučaju, LPL služi kao most između receptora i lipoproteina. Dok je LPL aktiviran pomoću ApoC-II, on je inhibiran ApoCIII-om.[11]
U ostalim organizmima
urediLPL gen je visoko konzerviran kod kičmenjaka. Lipoprotein-lipaza je uključena u transport lipida u posteljicu živih guštera (Pseudemoia entrecasteauxii).[55]
Mapa interaktivnog puta
urediReference
uredi- ^ a b c GRCh38: Ensembl release 89: ENSG00000175445 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000015568 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c d e f g h Mead JR, Irvine SA, Ramji DP (decembar 2002). "Lipoprotein lipase: structure, function, regulation, and role in disease". J. Mol. Med. 80 (12): 753–69. doi:10.1007/s00109-002-0384-9. PMID 12483461. S2CID 40089672.
- ^ Rinninger F, Kaiser T, Mann WA, Meyer N, Greten H, Beisiegel U (juli 1998). "Lipoprotein lipase mediates an increase in the selective uptake of high density lipoprotein-associated cholesteryl esters by hepatic cells in culture". J. Lipid Res. 39 (7): 1335–48. doi:10.1016/S0022-2275(20)32514-1. PMID 9684736.
- ^ Ma Y, Henderson HE, Liu MS, Zhang H, Forsythe IJ, Clarke-Lewis I, Hayden MR, Brunzell JD (novembar 1994). "Mutagenesis in four candidate heparin binding regions (residues 279-282, 291-304, 390-393, and 439-448) and identification of residues affecting heparin binding of human lipoprotein lipase". J. Lipid Res. 35 (11): 2049–59. doi:10.1016/S0022-2275(20)39951-X. PMID 7868983.
- ^ Kim SY, Park SM, Lee ST (januar 2006). "Apolipoprotein C-II is a novel substrate for matrix metalloproteinases". Biochem. Biophys. Res. Commun. 339 (1): 47–54. doi:10.1016/j.bbrc.2005.10.182. PMID 16314153.
- ^ Kinnunen PK, Jackson RL, Smith LC, Gotto AM, Sparrow JT (novembar 1977). "Activation of lipoprotein lipase by native and synthetic fragments of human plasma apolipoprotein C-II". Proc. Natl. Acad. Sci. U.S.A. 74 (11): 4848–51. Bibcode:1977PNAS...74.4848K. doi:10.1073/pnas.74.11.4848. PMC 432053. PMID 270715.
- ^ Meneghetti MC, Hughes AJ, Rudd TR, Nader HB, Powell AK, Yates EA, Lima MA (septembar 2015). "Heparan sulfate and heparin interactions with proteins". Journal of the Royal Society, Interface. 12 (110): 0589. doi:10.1098/rsif.2015.0589. PMC 4614469. PMID 26289657.
- ^ a b c d Wang CS, Hartsuck J, McConathy WJ (januar 1992). "Structure and functional properties of lipoprotein lipase" (PDF). Biochimica et Biophysica Acta. 1123 (1): 1–17. doi:10.1016/0005-2728(92)90119-M. PMID 1730040.
- ^ Wong H, Schotz MC (juli 2002). "The lipase gene family". Journal of Lipid Research. 43 (7): 993–9. doi:10.1194/jlr.R200007-JLR200. PMID 12091482.
- ^ a b c d e Braun JE, Severson DL (oktobar 1992). "Regulation of the synthesis, processing and translocation of lipoprotein lipase". The Biochemical Journal. 287 ( Pt 2) (2): 337–47. doi:10.1042/bj2870337. PMC 1133170. PMID 1445192.
- ^ "UniProt, P06858" (jezik: engleski). Pristupljeno 19. 9. 2021.
- ^ PDB 6E7K; Birrane G, Beigneux AP, Dwyer B, Strack-Logue B, Kristensen KK, Francone OL, et al. (januar 2019). "Structure of the lipoprotein lipase-GPIHBP1 complex that mediates plasma triglyceride hydrolysis". Proceedings of the National Academy of Sciences of the United States of America. 116 (5): 1723–1732. doi:10.1073/pnas.1817984116. PMC 6358717. PMID 30559189.
- ^ PDB 6OAU; Arora R, Nimonkar AV, Baird D, Wang C, Chiu CH, Horton PA, et al. (maj 2019). "Structure of lipoprotein lipase in complex with GPIHBP1". Proceedings of the National Academy of Sciences of the United States of America. 116 (21): 10360–10365. doi:10.1073/pnas.1820171116. PMC 6534989. PMID 31072929.
- ^ Semb H, Olivecrona T (mart 1989). "The relation between glycosylation and activity of guinea pig lipoprotein lipase". J. Biol. Chem. 264 (7): 4195–200. doi:10.1016/S0021-9258(19)84982-7. PMID 2521859.
- ^ a b Wong H, Davis RC, Thuren T, Goers JW, Nikazy J, Waite M, Schotz MC (april 1994). "Lipoprotein lipase domain function". J. Biol. Chem. 269 (14): 10319–23. doi:10.1016/S0021-9258(17)34063-2. PMID 8144612.
- ^ a b Vannier C, Ailhaud G (august 1989). "Biosynthesis of lipoprotein lipase in cultured mouse adipocytes. II. Processing, subunit assembly, and intracellular transport". J. Biol. Chem. 264 (22): 13206–16. doi:10.1016/S0021-9258(18)51616-1. PMID 2753912.
- ^ Ong JM, Kern PA (februar 1989). "The role of glucose and glycosylation in the regulation of lipoprotein lipase synthesis and secretion in rat adipocytes". J. Biol. Chem. 264 (6): 3177–82. doi:10.1016/S0021-9258(18)94047-0. PMID 2644281.
- ^ Beigneux AP, Davies BS, Gin P, Weinstein MM, Farber E, Qiao X, Peale F, Bunting S, Walzem RL, Wong JS, Blaner WS, Ding ZM, Melford K, Wongsiriroj N, Shu X, de Sauvage F, Ryan RO, Fong LG, Bensadoun A, Young SG (2007). "Glycosylphosphatidylinositol-anchored high-density lipoprotein-binding protein 1 plays a critical role in the lipolytic processing of chylomicrons". Cell Metabolism. 5 (4): 279–291. doi:10.1016/j.cmet.2007.02.002. PMC 1913910. PMID 17403372.
- ^ Davies BS, Beigneux AP, Barnes RH, Tu Y, Gin P, Weinstein MM, Nobumori C, Nyrén R, Goldberg I, Olivecrona G, Bensadoun A, Young SG, Fong LG (juli 2010). "GPIHBP1 is responsible for the entry of lipoprotein lipase into capillaries". Cell Metabolism. 12 (1): 42–52. doi:10.1016/j.cmet.2010.04.016. PMC 2913606. PMID 20620994.
- ^ Lookene A, Nielsen MS, Gliemann J, Olivecrona G (april 2000). "Contribution of the carboxy-terminal domain of lipoprotein lipase to interaction with heparin and lipoproteins". Biochem. Biophys. Res. Commun. 271 (1): 15–21. doi:10.1006/bbrc.2000.2530. PMID 10777674.
- ^ a b c Medh JD, Bowen SL, Fry GL, Ruben S, Andracki M, Inoue I, Lalouel JM, Strickland DK, Chappell DA (juli 1996). "Lipoprotein lipase binds to low density lipoprotein receptors and induces receptor-mediated catabolism of very low density lipoproteins in vitro". J. Biol. Chem. 271 (29): 17073–80. doi:10.1074/jbc.271.29.17073. PMID 8663292.
- ^ Beisiegel U, Weber W, Bengtsson-Olivecrona G (oktobar 1991). "Lipoprotein lipase enhances the binding of chylomicrons to low density lipoprotein receptor-related protein". Proc. Natl. Acad. Sci. U.S.A. 88 (19): 8342–6. Bibcode:1991PNAS...88.8342B. doi:10.1073/pnas.88.19.8342. PMC 52504. PMID 1656440.
- ^ McIlhargey TL, Yang Y, Wong H, Hill JS (juni 2003). "Identification of a lipoprotein lipase cofactor-binding site by chemical cross-linking and transfer of apolipoprotein C-II-responsive lipolysis from lipoprotein lipase to hepatic lipase". J. Biol. Chem. 278 (25): 23027–35. doi:10.1074/jbc.M300315200. PMID 12682050.
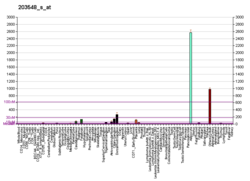
- ^ Protein Atlas, Protein Atlas. "Tissue expression of LPL - Summary - The Human Protein Atlas". www.proteinatlas.org. The Human Protein Atlas. Pristupljeno 25. 7. 2019.
- ^ Gene Cards, Gene Cards. "Human Gene Database". www.genecards.org. GeneCardsSuite. Pristupljeno 25. 7. 2019.
- ^ "Entrez Gene: LPL lipoprotein lipase".
- ^ Wang H, Eckel RH (2009). "Lipoprotein lipase: from gene to obesity". Am J Physiol Endocrinol Metab. 297 (2): E271–88. doi:10.1152/ajpendo.90920.2008. PMID 19318514.
- ^ a b Delezie J, Dumont S, Dardente H, Oudart H, Gréchez-Cassiau A, Klosen P, et al. (2012). "The nuclear receptor REV-ERBα is required for the daily balance of carbohydrate and lipid metabolism". FASEB J. 26 (8): 3321–35. doi:10.1096/fj.12-208751. PMID 22562834. S2CID 31204290.
- ^ Kiens B, Lithell H, Mikines KJ, Richter EA (oktobar 1989). "Effects of insulin and exercise on muscle lipoprotein lipase activity in man and its relation to insulin action". J. Clin. Invest. 84 (4): 1124–9. doi:10.1172/JCI114275. PMC 329768. PMID 2677048.
- ^ Yost TJ, Jensen DR, Haugen BR, Eckel RH (august 1998). "Effect of dietary macronutrient composition on tissue-specific lipoprotein lipase activity and insulin action in normal-weight subjects" (PDF). Am. J. Clin. Nutr. 68 (2): 296–302. doi:10.1093/ajcn/68.2.296. PMID 9701186.
- ^ Dijk W, Kersten S (2014). "Regulation of lipoprotein lipase by Angptl4". Trends Endocrinol. Metab. 25 (3): 146–155. doi:10.1016/j.tem.2013.12.005. PMID 24397894. S2CID 10273285.
- ^ a b Zhang R (april 2016). "The ANGPTL3-4-8 model, a molecular mechanism for triglyceride trafficking". Open Biol. 6 (4): 150272. doi:10.1098/rsob.150272. PMC 4852456. PMID 27053679.
- ^ Okubo M, Horinishi A, Saito M, Ebara T, Endo Y, Kaku K, Murase T, Eto M (novembar 2007). "A novel complex deletion-insertion mutation mediated by Alu repetitive elements leads to lipoprotein lipase deficiency". Mol. Genet. Metab. 92 (3): 229–33. doi:10.1016/j.ymgme.2007.06.018. PMID 17706445.
- ^ Ferreira LD, Pulawa LK, Jensen DR, Eckel RH (2001). "Overexpressing human lipoprotein lipase in mouse skeletal muscle is associated with insulin resistance". Diabetes. 50 (5): 1064–8. doi:10.2337/diabetes.50.5.1064. PMID 11334409.
- ^ Kim JK, Fillmore JJ, Chen Y, Yu C, Moore IK, Pypaert M, et al. (2001). "Tissue-specific overexpression of lipoprotein lipase causes tissue-specific insulin resistance". Proc Natl Acad Sci U S A. 98 (13): 7522–7. Bibcode:2001PNAS...98.7522K. doi:10.1073/pnas.121164498. PMC 34701. PMID 11390966.
- ^ Ferland A, Château-Degat ML, Hernandez TL, Eckel RH (maj 2012). "Tissue-specific responses of lipoprotein lipase to dietary macronutrient composition as a predictor of weight gain over 4 years". Obesity (Silver Spring). 20 (5): 1006–11. doi:10.1038/oby.2011.372. PMID 22262159. S2CID 40167321.
- ^ Prieto D, Oppezzo P (decembar 2017). "Lipoprotein Lipase Expression in Chronic Lymphocytic Leukemia: New Insights into Leukemic Progression". Molecules. 22 (12): 2083. doi:10.3390/molecules22122083. PMC 6149886. PMID 29206143.
- ^ Rozovski U, Hazan-Halevy I, Barzilai M, Keating MJ, Estrov Z (8. 12. 2015). "Metabolism pathways in chronic lymphocytic leukemia". Leukemia & Lymphoma. 57 (4): 758–65. doi:10.3109/10428194.2015.1106533. PMC 4794359. PMID 26643954.
- ^ Oppezzo P, Vasconcelos Y, Settegrana C, Jeannel D, Vuillier F, Legarff-Tavernier M, Kimura EY, Bechet S, Dumas G, Brissard M, Merle-Béral H, Yamamoto M, Dighiero G, Davi F (juli 2005). "The LPL/ADAM29 expression ratio is a novel prognosis indicator in chronic lymphocytic leukemia". Blood. 106 (2): 650–7. doi:10.1182/blood-2004-08-3344. PMID 15802535.
- ^ Heintel D, Kienle D, Shehata M, Kröber A, Kroemer E, Schwarzinger I, Mitteregger D, Le T, Gleiss A, Mannhalter C, Chott A, Schwarzmeier J, Fonatsch C, Gaiger A, Döhner H, Stilgenbauer S, Jäger U (juli 2005). "High expression of lipoprotein lipase in poor risk B-cell chronic lymphocytic leukemia". Leukemia. 19 (7): 1216–23. doi:10.1038/sj.leu.2403748. PMID 15858619.
- ^ van't Veer MB, Brooijmans AM, Langerak AW, Verhaaf B, Goudswaard CS, Graveland WJ, van Lom K, Valk PJ (januar 2006). "The predictive value of lipoprotein lipase for survival in chronic lymphocytic leukemia". Haematologica. 91 (1): 56–63. PMID 16434371.
- ^ Nückel H, Hüttmann A, Klein-Hitpass L, Schroers R, Führer A, Sellmann L, Dührsen U, Dürig J (juni 2006). "Lipoprotein lipase expression is a novel prognostic factor in B-cell chronic lymphocytic leukemia". Leukemia & Lymphoma. 47 (6): 1053–61. doi:10.1080/10428190500464161. PMID 16840197. S2CID 20532204.
- ^ Mansouri M, Sevov M, Fahlgren E, Tobin G, Jondal M, Osorio L, Roos G, Olivecrona G, Rosenquist R (mart 2010). "Lipoprotein lipase is differentially expressed in prognostic subsets of chronic lymphocytic leukemia but displays invariably low catalytical activity". Leukemia Research. 34 (3): 301–6. doi:10.1016/j.leukres.2009.07.032. PMID 19709746.
- ^ Kaderi MA, Kanduri M, Buhl AM, Sevov M, Cahill N, Gunnarsson R, Jansson M, Smedby KE, Hjalgrim H, Jurlander J, Juliusson G, Mansouri L, Rosenquist R (august 2011). "LPL is the strongest prognostic factor in a comparative analysis of RNA-based markers in early chronic lymphocytic leukemia". Haematologica. 96 (8): 1153–60. doi:10.3324/haematol.2010.039396. PMC 3148909. PMID 21508119.
- ^ Porpaczy E, Tauber S, Bilban M, Kostner G, Gruber M, Eder S, Heintel D, Le T, Fleiss K, Skrabs C, Shehata M, Jäger U, Vanura K (juni 2013). "Lipoprotein lipase in chronic lymphocytic leukaemia - strong biomarker with lack of functional significance". Leukemia Research. 37 (6): 631–6. doi:10.1016/j.leukres.2013.02.008. PMID 23478142.
- ^ Mátrai Z, Andrikovics H, Szilvási A, Bors A, Kozma A, Ádám E, Halm G, Karászi É, Tordai A, Masszi T (januar 2017). "Lipoprotein Lipase as a Prognostic Marker in Chronic Lymphocytic Leukemia". Pathology Oncology Research. 23 (1): 165–171. doi:10.1007/s12253-016-0132-z. PMID 27757836. S2CID 22647616.
- ^ Prieto D, Seija N, Uriepero A, Souto-Padron T, Oliver C, Irigoin V, Guillermo C, Navarrete MA, Inés Landoni A, Dighiero G, Gabus R, Giordano M, Oppezzo P (august 2018). "LPL protein in Chronic Lymphocytic Leukaemia have different origins in Mutated and Unmutated patients. Advances for a new prognostic marker in CLL". British Journal of Haematology. 182 (4): 521–525. doi:10.1111/bjh.15427. PMID 29953583.
- ^ Rombout A, Verhasselt B, Philippé J (novembar 2016). "Lipoprotein lipase in chronic lymphocytic leukemia: function and prognostic implications". European Journal of Haematology. 97 (5): 409–415. doi:10.1111/ejh.12789. PMID 27504855.
- ^ Williams SE, Inoue I, Tran H, Fry GL, Pladet MW, Iverius PH, Lalouel JM, Chappell DA, Strickland DK (mart 1994). "The carboxyl-terminal domain of lipoprotein lipase binds to the low density lipoprotein receptor-related protein/alpha 2-macroglobulin receptor (LRP) and mediates binding of normal very low density lipoproteins to LRP". J. Biol. Chem. 269 (12): 8653–8. doi:10.1016/S0021-9258(17)37017-5. PMID 7510694.
- ^ Nykjaer A, Nielsen M, Lookene A, Meyer N, Røigaard H, Etzerodt M, Beisiegel U, Olivecrona G, Gliemann J (decembar 1994). "A carboxyl-terminal fragment of lipoprotein lipase binds to the low density lipoprotein receptor-related protein and inhibits lipase-mediated uptake of lipoprotein in cells". J. Biol. Chem. 269 (50): 31747–55. doi:10.1016/S0021-9258(18)31759-9. PMID 7989348.
- ^ Chappell DA, Fry GL, Waknitz MA, Iverius PH, Williams SE, Strickland DK (decembar 1992). "The low density lipoprotein receptor-related protein/alpha 2-macroglobulin receptor binds and mediates catabolism of bovine milk lipoprotein lipase". J. Biol. Chem. 267 (36): 25764–7. doi:10.1016/S0021-9258(18)35675-8. PMID 1281473.
- ^ Griffith OW, Ujvari B, Belov K, Thompson MB (novembar 2013). "Placental lipoprotein lipase (LPL) gene expression in a placentotrophic lizard, Pseudemoia entrecasteauxii". Journal of Experimental Zoology Part B: Molecular and Developmental Evolution. 320 (7): 465–70. doi:10.1002/jez.b.22526. PMID 23939756.
Dopunska literatura
uredi- Zechner R (1997). "The tissue-specific expression of lipoprotein lipase: implications for energy and lipoprotein metabolism". Curr. Opin. Lipidol. 8 (2): 77–88. doi:10.1097/00041433-199704000-00005. PMID 9183545.
- Fisher RM, Humphries SE, Talmud PJ (1998). "Common variation in the lipoprotein lipase gene: effects on plasma lipids and risk of atherosclerosis". Atherosclerosis. 135 (2): 145–59. doi:10.1016/S0021-9150(97)00199-8. PMID 9430364.
- Beisiegel U (1998). "Lipoprotein metabolism". Eur. Heart J. 19 Suppl A: A20–3. doi:10.1093/eurheartj/19.Abstract_Supplement.1. PMID 9519338.
- Pentikäinen MO, Oksjoki R, Oörni K, Kovanen PT (2002). "Lipoprotein lipase in the arterial wall: linking LDL to the arterial extracellular matrix and much more". Arterioscler. Thromb. Vasc. Biol. 22 (2): 211–7. doi:10.1161/hq0102.101551. PMID 11834518.
- Lichtenstein L, Berbée JF, van Dijk SJ, van Dijk KW, Bensadoun A, Kema IP, Voshol PJ, Müller M, Rensen PC, Kersten S (novembar 2007). "Angptl4 upregulates cholesterol synthesis in liver via inhibition of LPL- and HL-dependent hepatic cholesterol uptake". Arterioscler. Thromb. Vasc. Biol. 27 (11): 2420–7. doi:10.1161/ATVBAHA.107.151894. PMID 17761937.
- Lichtenstein L, Mattijssen F, de Wit NJ, Georgiadi A, Hooiveld GJ, van der Meer R, He Y, Qi L, Köster A, Tamsma JT, Tan NS, Müller M, Kersten S (decembar 2010). "Angptl4 protects against severe proinflammatory effects of saturated fat by inhibiting fatty acid uptake into mesenteric lymph node macrophages". Cell Metab. 12 (6): 580–92. doi:10.1016/j.cmet.2010.11.002. PMC 3387545. PMID 21109191.
Vanjski linkovi
uredi- GeneReviews/NCBI/NIH/UW entry on Familial Lipoprotein Lipase Deficiency
- Gene therapy for lipoprotein lipase deficiency
- Lipoprotein lipase na US National Library of Medicine Medical Subject Headings (MeSH)