Savijanje proteina
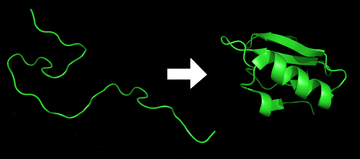
Sklapanje proteina, savijanje proteina ili presavijanje proteina, je fizički proces kojim proteinski lanac stiče svoju prirodnu trodimenzijsku strukturu, konformaciju koja je obično biološki djelotvorna, na brz i ponovljiv način. To je fizički proces kojim se polipeptid preklapa u svoju karakterističnu i funkcijsku trodimenzionzijsku strukturu iz slučajne zavojnice.[1] Svaki protein postoji kao rasklopljeni lančani polipeptid ili slučajna zavojnica kada se translatira iz sekvence iRNK do linearnog lanca aminokiselina. Ovom polipeptidu nedostaje stabilna (dugotrajna) trodimenzijska struktura (lijeva strana prve slike). Kako se polipeptidni lanac sintetizira u ribosomu, linearni lanac počinje se savijati u svoju trodimenzijsku strukturu. Preklapanje počinje čak i za vrijeme translacije polipeptidnog lanca. Aminokiseline međusobno djeluju da bi stvorile dobro definiranu trodimenzijsku strukturu, u presavijeni protein (desna strana slike), poznat kao izvorno stanje. Rezultirajuća prostorna (3D) struktura određena je aminokiselinskom sekvencom ili primarnom strukturom (Anfinsenova dogma).[2]

Ispravna trodimenzionzijska struktura bitna je za funkcioniranje, iako neki dijelovi funkcijskih proteina mogu ostati nesavijeni,[3] tako da je važna i dinamika proteina. Ako se ne preklope u nativnu strukturu, općenito se stvaraju neaktivni proteini, ali u nekim slučajevima pogrešno savijeni proteini imaju modificiranu ili toksičnu funkcionalnost. Smatra se da nekoliko neurodegenerativnih i drugih bolesti nastaje akumulacijom amiloidnih fibrila, formiranih od pogrešno sklopljenih proteina.[4] Mnoge alergije izazvane su nepravilnim savijanjem nekih proteina, jer imunski sistem ne stvara antitijela na izvjesne proteinske strukture.[5]
Denaturacija proteina je proces prelaska iz presavijenog u rasklopljeno stanje. To se događa pri kuhanju, u opekotinama, u slučaju proteinopatije i u drugim kontekstima.
Trajanje procesa savijanja dramatično varira ovisno o posmatranom proteinu. Kada se proučavaju izvan ćelije, najsporije presavijajućim proteinima treba mnogo minuta ili sati da se preklope prvenstveno zbog izomerizacije prolina, i moraju proći kroz niz srednjih stanja, poput kontrolnih tačaka, prije nego što se postupak kompletira.[6] S druge strane, vrlo mali pojedinačni – domenski proteini, dužine do stotinu aminokiselina, obično se presavijaju u jednom koraku.[7] Vremenske skale milisekundi su norma, a najbrže poznate reakcije presavijanja proteina završavaju se u roku od nekoliko mikrosekundi.[8]
Proces presavijanja proteina
urediPrimarna struktura
urediPrimarna struktura proteina i njena linearna aminokiselinska sekvenca, određuje njegovu prirodnu konformaciju.[9] Specifični aminokiselinski ostaci i njihov položaj u polipeptidnom lancu su odlučujući faktori kojima se dijelovi proteina usko preklapaju i čine njegovu trodimenzijsku konformaciju. Sastav aminokiselina nije toliko važan kao njihov redoslijed.[10] Suštinska činjenica presavijanja, međutim, ostaje da aminokiselinska sekvenca svakog proteina sadrži informacije koje specificiraju i nativnu strukturu i put za postizanje tog stanja. To ne znači da se gotovo identične aminokiselinske sekvence uvijek slično preklapaju.[11] Konformacije se razlikuju i na osnovu faktora okoline; slični proteini različito se savijaju ovisno o tome gdje se nalaze.
Sekundarna struktura
urediFormiranje sekundarne strukture prvi je korak u procesu presavijanja koji protein treba da bi preuzeo svoju prirodnu strukturu. Karakteristike sekundarne strukture su poznate kao alfa-heliksi i beta-listovi, koje se brzo savijaju jer su stabilizirani unutarmolekulskim vodikovim vezama, što je prvi okarakterizirao Linus Pauling. Stvaranje intramolekulskih vodikovih veza pruža još jedan važan doprinos stabilnosti proteina.[12] α–heliksi nastaju stvaranjem vodikovih veza okosnice, kako bi oblikovale spiralni oblik (slika desno).[10] P–naborani sloj je struktura koja se formira sa okosnicom, savijenom unazad, da bi stvorile vodikove veze (kao što je prikazano na slici lijevo). Vodikove veze su peptidne veze između amidnog vodika i karbonilnog kisika. Postoje antiparalelni β-nabrani i paralelni β-spirali listovi, gdje je stabilnost vodikovih veza jača u paralelnom β –listu, jer se vodikove veze pod idealnim uglom od 180 stepeni u usporedbi s kosim vodikovim vezama nastalim paralelnim u listovima.[10]
Tercijarna struktura
urediAlfa-heliksi i beta savijeni listovi mogu biti amfipatski po prirodi ili sadržavati hidrofilni i hidrofobni dio. Ovo svojstvo sekundarnih struktura pomaže u tercijarnoj strukturi proteina, kada dolazi do presavijanja, tako da su hidrofilne strane okrenute ka vodenoj okolini koja okružuje protein, a hidrofobne strane prema hidrofobnom jezgru proteina.[13] Sekundarna struktura hijerarhijski ustupa mjesto formiranju tercijarne strukture. Kada se tercijarna struktura proteina formira i stabilizira hidrofobnim interakcijama, može nastati kovalentna veza u obliku disulfidnih mostova formiranih između dva cisteinska ostatka. Tercijarna struktura proteina uključuje jedan polipeptidni lanac, ali dodatne interakcije presavijenih polipeptidnih lanaca dovode do stvaranja kvaternarne strukture.[14]
Kvaternarna struktura
urediTercijarna struktura, u nekim proteinima, može se nastaviti formiranjem kvaternarne strukture, što obično uključuje "ansamle" ili "koansamble" podjedinica koje su se već presavile; drugim riječima, višestruki polipeptidni lanci mogli bi međusobno stvarati potpuno funkcionalni kvarternarni protein.[10]
Pokretačke sile savijanja proteina
urediPreklapanje je spontani proces, koji se uglavnom vodi hidrofobnim interakcijama, stvaranjem unutarmolekulskih vodikovih veza, van der Waalsove sile, a suprotstavljajoj se konformacijska entropija.[15] Proces savijanja često započinje kotranslacijski, tako da se N-kraj proteina počinje presavijati dok se C-krajevi proteina još uvijek sintetiziraju u ribosomima. Međutim, molekula proteina može se spontano saviti tokom ili nakon biosinteze.[16] Iako se ove makromolekule mogu smatrati "presavijenim", postupak također zavisi i od rastvarača (voda ili lipidni dvosloj),[17] koncentracije soli, pH, temperature, mogućeg prisustva kofaktora i molekulskih šaperona.
Proteini će imati ograničenja sposobnosti presavijanja zbog ograničenih uglova savijanja ili konformacija koje su moguće. Ovi dozvoljeni uglovi presavijanja proteina opisani su dvodimenzijskom grafičkom pločom poznatom kao Ramachandranov plot, prikazan sa psi i fi uglovima dozvoljene rotacije.[18]
Hidrofobni efekti
urediPreklapanje proteina mora biti termodinamički povoljno za ćeliju, da bi moglo biti spontana reakcija. Budući da je poznato da je savijanje proteina spontano, mora poprimiti negativnu vrijednost Gibbsove slobodne energije. Gibbsova slobodna energija u presavijanju proteina direktno je povezana sa entalpijom i entropijom.[10] Da bi nastala negativna delta G i da bi savijanje proteina postalo termodinamički povoljno, entalpija, entropija ili obje moraju biti povoljne.
Važna pokretačka sila procesa presavijanja je minimiziranje broja hidrofobnih bočnih lanaca izloženih vodi.[19] Hidrofobni učinak je pojava u kojoj se hidrofobni lanci proteina ulaze u jezgro proteina (daleko od hidrofilnog okruženja).[10] U vodenom okruženju, molekule vode su sklone da se agregiraju oko hidrofobnih područja ili bočnih lanaca proteina, stvarajući vodene ljuske uređenih molekula vode.[20] Raspored molekula vode oko hidrofobne regije povećava red u sistemu i stoga doprinosi negativnoj promjeni entropije (manje entropije u sistemu). Molekule vode su fiksirane u tim vodenim kavezima koji pokreću hidrofobni kolaps ili savijanje hidrofobnih grupa prema unutra. Hidrofobni kolaps uvodi entropiju u sistem, razbijanjem vodenih kaveza čime se oslobađaju uređene vodene molekule.[10] Mnoštvo hidrofobnih grupa koje međusobno djeluju u jezgri globulasto presavijenog proteina doprinosi značajno stabilnosti proteina nakon presavijanja, zbog izuzetno akumuliranih van der Waalsovih sila (konkretno Londonske disperzijske sile).[10] Kao pokretač sila u termodinamici hidrofobni efekt postoji samo ako postoji vodeni medij sa amfifilnom molekulom sa velikim hidrofobnim područjem.[21] Snaga vodikovih veza ovisi o njihovoj okolini; prema tome, H-veze obavijene hidrofobnom jezgrom doprinose stabilnosti matičnog stanja više od H-veza izloženih vodenom.[22]
U proteinima sa globulastim naborima, hidrofobne aminokiseline imaju sklonost za prošaranost duž primarne sekvence, a ne nasumično raspoređene ili skupljene zajedno.[23][24] Međutim, proteini koji su nedavno nastali de novo, koji imaju tendenciju da budu suštinski poremećeni,[25][26] ispoljavaju suprotan obrazac hidrofobnog grupiranja aminokiselina duž primarne sekvence.[27]
Šaperoni
urediMolekule šaperona su klasa proteina koji pomažu u pravilnom savijanju ostalih proteina in vivo. Postoje u svim ćelijskim odjeljcima i u interakciji su s polipeptidnim lancima, kako bi omogućili stvaranje prirodne trodimenzijske konformacije proteina; međutim, sami šaperoni nisu uključeni u konačnu strukturu proteina kojem pomažu.[28] Šaperoni mogu pomoći u presavijanju čak i kada ribosom sintetizira novonastajući polipeptid.[29] Molekulski šaperoni djeluju vezanjem, tako da stabiliziraju inače nestabilnu strukturu proteina u procesu presavijanja, ali šaperoni ne sadrže potrebne informacije da bi se znala tačna prirodna struktura proteina kojem pomažu. Oni su prije pratitelji koji djeluju sprečavanjem netačnih konformacija presavijanja.[29] Na taj način, oni zapravo ne povećavaju brzinu pojedinačnih koraka uključenih u preklopni put prema prirodnoj strukturi; umjesto toga, oni djeluju smanjenjem mogućih neželjenih nakupina polipeptidnog lanca koji bi inače mogli usporiti potragu za odgovarajućim međuproduktom i pružaju efikasniji put da polipeptidni lanac oblikuje ispravne konformacije.[28] Šaperone ne treba zamijeniti sa sklopivim katalizatorima, koji zapravo kataliziraju inače spore korake na preklopnom putu. Primjeri sklopivih katalizatora su izomeraze protein-disulfida i peptidil-prolil-izomeraza, koje mogu biti uključene u stvaranje disulfidnih veza ili međusobnu konverziju između cis– i trans-stereoizomera.[29] Šaperoni su pokazali kritičnost u procesu presavijanja proteina in vivo, jer im pružaju pomoć potrebnu za postizanje odgovarajućih poravnanja i konformacija dovoljno efikasno da postanu "biološki relevantni".[30] To znači da bi se polipeptidni lanac teorijski mogao presaviti u svoju prirodnu strukturu i bez pomoći šaperona, kao što su pokazali eksperimenti presavijanja proteina provedeni in vitro;[30] ali ovaj postupak je previše neučinkovit ili prespor da bi postojao u biološkim sistemima. Zato su šaperoni neophodni za savijanje proteina in vivo. Zajedno sa njihovom ulogom u pomaganju formiranju prirodne strukture, sudjeluju i u različitim ulogama kao što su transport proteina, razgradnja i čak dopuštaju denaturiranim proteinima izloženim određenim vanjskim faktorima denaturacije priliku da se ponovo ugrade u ispravne nativne.[31]
Potpuno denaturiranom proteinu nedostaje i tercijarna i sekundarna struktura, a postoji kao takozvana slučajna zavojnica. Pod određenim uvjetima, neki se proteini mogu ponovo presaviti; međutim, u mnogim slučajevima denaturacija je nepovratna.[32] Ćelije ponekad štite svoje proteine od denaturacijskog uticaja toplote, pomoću enzima, poznatih kao proteini toplotnog šoka (tip šaperona), koji pomažu ostalim proteinima i u presavijanju i u zaoslalom presavijanju. Proteini toplotnog šoka pronađeni su u šaperonskim proteinomima svih ispitivanih vrsta, od bakterija do ljudi, što sugerira da su se razvili vrlo rano i imaju važnu funkciju. Neki proteini se nikad ne presavijaju u ćelijama, osim uz pomoć šaperona, koji ili izoliraju pojedinačne proteine, tako da njihovo savijanje ne prekida interakcija s drugim proteinima, ili pomažu u odmotavanju pogrešno sklopljenih proteina, omogućavajući im da se presaviju u ispravnu prirodnu strukturu.[33] Ova funkcija je presudna za sprečavanje rizika od precipitacije u netopive amorfne agregate. Vanjski faktori koji su uključeni u denaturaciju proteina ili poremećaj izvornog stanja uključuju temperaturu, vanjska polja (električna, magnetna),[34] molekularno gomilanje,[35] pa čak i ograničenje prostora (tj. zatvorenost), što može imati veliki uticaj na presavijanje proteina.[36] Denaturaciji proteina također oogu doprinositi i visoke koncentracije rastvorene supstance, ekstremi pH, mehaničke sile i prisustvo hemijskih denaturanata. Ovi pojedinačni faktori kategorizirani su zajedno kao stresni. Pokazalo se da tokom ćelijskog stresa šaperoni javljaju u sve većim koncentracijama i pomažu pravilnom presavijanju novih proteina, kao i denaturiranih ili pogrešno savijenih.[28]
Pod nekim uslovima, proteini se neće saviti u svoje biohemijski djelotvorne forme. Temperature iznad ili ispod opsega u kojem ćelije mogu da žive uzrokovaće da nastaju termički nestabilni proteini ili denaturiraju (zbog toga ključalo bjelance postaje neprozirno). Termička stabilnost proteina, međutim, nije daleko od konstantne; naprimjer, pronađene su hipertermofilne bakterije koje rastu na temperaturama visokim oko 122 °C,[37] što naravno zahtijeva da njihov puni komplement vitalnih proteina i proteinskih sklopova bude stabilan na toj ili višoj temperaturi.
Bakterija E. coli je domaćin za bakteriofag T4, a i gp31 protein kodiran s fagom funkcijski homologan sa šaperon (protein)|šaperonskim proteinom]] GroES E. coli i sposoban jeda ga nadomesti u sastavu čestica bakteriofaga T4 virusa tokom infekcije.[38] Poput GroES, gp31 tvori stabilni kompleks s GroEL šaperoninom koji je prijeko potreban za presavijanje i in vivo savijanje glavnog kapsidnog proteina bakteriofaga T4 gp23.[38]
Nepravilno savijanje proteina i neurodegenerativne bolesti
urediSmatra se da je protein pogrešno savijen ako ne može postići normalno prirodno stanje. To može biti posljedica mutacija gena za aminokiselinske sekvence ili poremećaja normalnog procesa presavijanja, djelovanjem vanjskih faktora.[39] Pogrešno sklopljeni protein obično sadrži β-listove koji su organizirani u supramolekulskom rasporedu poznatom kao kros-β struktura. Ovi sklopovi bogati β-listovima vrlo su stabilni, netopivi i uglavnom su otporni na proteolizu (razlaganje).[40] Strukturna stabilnost ovih nitasatih sklopova prouzrokovana je intenzivnim interakcijama između proteinskih monomera, formiranih okosničnim vodikovim vezama između njihovih β-lanaca.[40] Pogrešno savijanje proteina može podstaknuti daljnje pogrešno savijanje i nakupljanje drugih proteini u agregate ili oligomere. Povećani nivoi agregiranih proteina u ćeliji dovode do stvaranja amiloida, sličnih struktura koje mogu prouzrokovati degenerativne poremećaje i ćelijsku smrt.[39] Amiloidi su nitaste strukture koje sadrže međumolekulske vodikove veze, visoko netopive i izrađene od konvertiranih proteinskih agregata.[39] Stoga, proteosomski put možda neće biti dovoljno efikasan da razgradi pogrešno savijene proteine prije agregacije. Pogrešno sklopljeni proteini mogu međusobno komunicirati i stvarati strukturirane agregate i u međumolekulskm interakcijama sticati toksičnost.[39]
Agregirani proteini povezani su sa prionima srodnim bolestima kao što su Creutzfeldt – Jakobova bolest, goveđa spongiformna encefalopatija (bolest ludih krava), a amiloidima povezane bolesti kao što je Alzheimerova bolest i porodična amiloidna kardiomiopatija ili polineuropatija,[41] kao i bolesti unutarćelijske agregacije kao što su Hungtingtonova i Parkinsonova bolest.[4][42] Ove degenerativne bolesti koje se javljaju u starosti povezane su s agregacijom pogrešno sklopljenih proteina u netopive, vanćelijske agregate i / ili unutarćelijske inkluzije, uključujući unakrsne β amiloidne fibrile. Nije potpuno jasno jesu li agregati uzrok ili samo odraz gubitka homeostaze proteina, ravnoteže između sinteze, presavijanja, agregacije i prometa proteina. Nedavno je Evropska agencija za lijekove odobrila upotrebu Tafamidis ili Vyndaqel-a (kinetičkog stabilizatora tetramernog transtiretina) za liječenje transtiretinskih amiloidnih bolesti. To sugerira da proces stvaranja amiloidnih fibrila (a ne samih fibrila) uzrokuje degeneraciju postmitotskog tkiva kod ljudskih amiloidnih bolesti..[43] Pogrešno savijanje i prekomjerna degradacija umjesto savijanja i funkcije dovodi do brojnih proteopatija i bolesti kao što su antitripsinski–povezani emfizem, cistična fibroza i lizosomska bolest skladištenja, gdje je gubitak funkcije posljedica poremećaja. Iako se proteinska nadomjesna terapija u prošlosti koristila za ispravljanje potonjih poremećaja, novi pristup je upotreba farmaceutski pratiteljfarmaceutskih pratitelja za preklapanje mutiranih proteina kako bi postali dječotvorni.
Eksperimentalne tehnike za proučavanje presavijanja proteina
urediIako se zaključci o presavijanju proteina mogu donijeti putem studije mutacija, obično se eksperimentalne tehnike za proučavanje presavijanja proteina oslanjaju na odvijanje ili savijanje proteina i posmatranje konformacijskih promjena, koristeći standard nekristalografskih.
RTG kristalografija
urediRendgenska kristalografija jedna je od efikasnijih i važnijih metoda za pokušaj dešifriranja trodimenzijske konfiguracije presavijenog proteina.[44] Da bi se mogla provesti rendgenska kristalografija, protein koji se ispituje mora biti smješten unutar kristalne rešetke. Da bi se smjestio unutar kristalne rešetke, mora se imati prikladni rastvarač za kristalizaciju, dobiti čisti protein na prezasićenom nivou u otopini i taložiti kristale u rastvoru.[45] Kada se protein kristalizira, rendgenske zrake mogu se koncentrirati kroz kristalnu rešetku, koja bi difraktirala zrake ili ih uputila prema van u različitim smjerovima. Ovi izlazni snopovi povezani su sa specifičnom trodimenzijskom konfiguracijom proteina koji je zatvoren u njima. X-zrake specifično komuniciraju s elektronskim oblacima koji okružuju pojedine atome unutar rešetkaste kristalne strukture i stvaraju uočljivi obrazac difrakcije.[13] Ovaj obrazac može se pročitati i dovesti do pretpostavki o uključenim fazama ili faznim uglovima (koji kompliciraju ovaj metod), samo povezivanjem oblaka elektronske gustine sa amplitudom rendgenskih zraka.[46] Bez relacije uspostavljene putem matematičke osnove poznate kao Fourierova transformacija, "fazni problem" učinio bi predviđanje difrakcionih obrazaca vrlo teškim. Nove metode, kao što je višestruka izomorfna zamjena, za difrakciju rendgenskih zraka na predvidljiviji način, koriste prisustvo iona teškog metala, smanjujući broj uključenih varijabli i rješavajući fazni problem.
Fluorescentna spektroskopija
urediFluorescentna spektroskopija je visoko osjetljiv metod za proučavanje stanja savijanja proteina. Tri aminokiseline, fenilalanin (Phe), tirozin (Tyr) i triptofan (Trp), imaju svojstvena fluorescentna obilježja, ali eksperimentalno se koriste samo Tyr i Trp, jer su njihovi kvantni prinosi dovoljno visoki da daju dobre fluorescentne signale. I Trp i Tyr pobuđuju se talasnom dužinom od 280 nm, dok se samo Trp pobuđuje talasnom dužinom od 295 nm. Zbog svog aromatskog karaktera, ostaci Trp i Tyr često se nalaze u potpunosti ili djelomično zaklonjeni u hidrofobnom jezgru proteina, na površini između dva proteinska domena ili na granici između podjedinica oligomernih proteina. U ovom apolarnom okruženju imaju visoke kvantne prinose, a samim tim i velike intenzitete fluorescencije. Po prestanku tercijarne ili kvartarne strukture proteina, ovi bočni lanci postaju izloženiji hidrofilnom okruženju rastvarača, a njihovi kvantni prinosi se smanjuju, što dovodi do niskih intenziteta fluorescencije. Za ostatke Trp, talasna dužina njihove maksimalne emisije fluorescencije također ovisi o njihovoj okolini.
Fluorescentna spektroskopija može se koristiti za karakterizaciju ravnoteže nesavijanja proteina, mjerenjem varijacije u intenzitetu emisije fluorescencije ili u talasnoj dužini maksimalne emisije u funkciji vrijednosti.[47][48] Denaturant može biti hemijska molekula (urea, gvanidinij-hidroklorid), temperatura, pH, pritisak itd. Ravnoteža između različitih, ali diskretnih proteinskih stanja, tj. prirodno stanje, intrmedijarna stanja, stanje nesavijenosti, ovise o vrijednosti denaturanta; stoga i globalni signal fluorescencije ravnotežne njihove smjese također ovise o ovoj vrijednosti. Tako se dobija profil vezan za globalni signal proteina za vrijednost denaturanta. Profil ravnotežnog odvijanja može omogućiti otkrivanje i identificiranje neodvijajućih međuprodukata.[49][50] Hugues Bedouelle razvio je opće jednadžbe da iz takvih profila dobije termodinamičke parametre koji karakteriziraju odvijajuće ravnoteže homomernih ili heteromernih proteina, do trimera i potencijalno tetramera. Fluorescentna spektroskopija u kombinaciji s uređajima za brzo miješanje, kao što je zaustavljeni protok, za mjerenje kinetike savijanja proteina[51] generiran je ševronski plot i izvedena Phi vrijednost analize.
Kružni dihroizam
urediKružni dihroizam jedan je od najopćijih i osnovnih alata za proučavanje presavijanja proteina. Njegova spektroskopija mjeri apsorpciju kružno polarizirane svetlosti. U proteinima su strukture, kao što su alfa-heliksi i beta-listovi hiralne, te tako apsorbiraju takvu svjetlost. Apsorpcija ove svjetlosti djeluje kao marker stepena nabranosti proteinskog ansambla. Ova tehnika koristi se za mjerenje ravnoteže neodvijanja proteina, mjerenjem promjene u ovoj apsorpciji, u ovisnosti o koncentraciji denaturanta ili temperatura. Rastopljena masa za denaturaciju mjeri oslobođenu energiju odvijanja, kao i vrijednost m proteina ili ovisnost o denaturantu. Tališna temperatura mjeri temperaturu denaturacije (Tm) proteina. Što se tiče fluorescentne spektroskopije, spektroskopija kružnog dihroizma može se kombinirati s brzim uređajima za mješanje, kao što je zaustavljeni protok za merenje kinetike presavijanja proteina i za generiranje ševron plotova.
Vibracijski kružni dihroizam proteina
urediNoviji razvoj tehnika vibracijskog kružnog dihroizma (VCD) za proteine, koji sada uključuju instrumente Fourierove transformacije (FT), pružaju moćna sredstva za određivanje konformacija proteina u rastvoru, čak i za njihove vrlo velike molekule. Takve VCD studije proteina često se kombiniraju s difrakcijom rendgenskih zraka proteinskih kristala, FT-IR podacima za proteinske rastvore u teškoj vodi (D2O) ili ab initio kvantna izračunavanja za pružanje nedvosmislenih strukturnih zadataka koji su nedostupni prema CD.
Spektroskopija nuklearne magnetske rezonancije proteina
urediSavijaanje proteina rutinski se proučava pomoću NMR spektroskopije, naprimjer praćenjem protona izmjene vodik-deuterijskih amidnih protona proteina u njihovom izvornom stanju, što osigurava stabilnost specifičnu za ostatke i ukupnu stabilnost proteina.[52]
Dvopolarizacijska interferometrija
urediDvopolarizacijska interferometrija je površinska tehnika za mjerenje optičkih svojstava molekulskih slojeva. Kada se koristi za karakteriziranje nabora proteina, mjeri njihovu konformaciju određivanjem ukupne veličine jednoslojnog proteina i njegove gustoće u stvarnom vremenu pri subangstremskoj razlučivosti,[53] iako su mjerenja kinetike savijanja proteina u stvarnom vremenu ograničena na procese koji se odvijaju sporije od ~ 10 Hz. Slično kružnom dihroizmu, podsticaj za presavijanje može pokrenuti denaturant ili temperatura.
Studije presavijanja s velikom vremenskom rezolucijom
urediStudije presavijanja proteina uveliko su napredovale posljednjih godina, razvojem brzih tehnika s vremenskim rješavanjem. Eksperimentatori brzo pokreću presavijanje uzorka nesavijenog proteina i promatraju rezultirajuću dinamiku. Brze tehnike koje se koriste uključuju raspršivanje neutrona,[54] ultrabrzo miješanje rastvora, fotohemijske metode i spektroskopiju laserskog skoka temperature. Među mnogim naučnicima koji su pridonijeli razvoju ovih tehnika su Jeremy Cook, Heinrich Roder, Harry Gray, Martin Gruebele, Brian Dyer, William Eaton, Sheena Radford, Chris Dobson, Alan Fersht, Bengt Nölting i Lars Konermann.
Proteoliza
urediProteoliza je rutinski postupak koju se koristi za ispitivanje frakcije koja se odvijala u širokom rasponu uvjeta rastvora (npr. brza paralelna proteoliza (FASTpp.[55][56]
Jednomolekulska spektroskopija sile
urediTehnike pojedinačnih molekula poput optičke pincete i AFM, korištene su za razumijevanje mehanizama presavijanja izoliranih proteina kao i proteina s šaperonima.[57] Optička pinceta korištena je za istezanje pojedinačnih proteinskih molekula sa njihovih nesavijenih C– i N-krajeva, kako bi se omogućilo proučavanje naknadnog resavijanja.[58] Tehnika omogućuje mjerenje brzine savijanja na razini jedne molekule; naprimjer, optička pinceta nedavno je primijenjena za proučavanje presavijanja i odvijanja proteina koji sudjeluju u koagulaciji krvi. Ključnu ulogu u procesu stvaranja krvnih ugrušaka ima protein zvani von Willebrandov faktor. Otkrilo se – pomoću mjerenja optičkom pincetom s jednom molekulom – da vWF vezan za kalcij djeluje kao senzor smicajuće sile u krvi. Sila smicanja dovodi do odvijanja A2 domena vWF, čija se brzina ponovnog savijanja dramatično povećava u prisutnosti kalcija.[59] Nedavno je također pokazano da jednostavni src SH3 domen pristupa sa multiplim putevima odvijanja pod silom.[60]
Slikanje biotina
urediSlikanje biotinom omogućuje ćelijske snimke (ne)presavijenih proteina. 'Slika' biotina pokazuje pristranost prema predviđenim suštinski poremećenim proteinima .[61]
Računarske studije presavijanja proteina
urediRačunarske studije presavijanja proteina uključuju tri glavna aspekta koja se odnose na predviđanje stabilnosti proteina, kinetiku i strukturu. Nedavni pregled sažima dostupne računarske metode za savijanje proteina.[62]
Levinthalov paradoks
urediU 1969., Cyrus Levinthal primijetio je da, zbog vrlo velikog broja stepeni slobode u nesavijenom polipeptidnom lancu, molekula ima astronomski broj mogućih konformacija. U jednom od njegovih radova, to je procijenjeno na 3300 ili 10143.[63] Levinthalov paradoks je eksperiment zasnovan na zapažanju da bi, ako bi se protein savio uzastopnim uzimanjem uzoraka svih mogućih konformacija, za to bilo potrebno astronomsko vrijeme, čak i ako bi se konformacije prikupljale najvećom brzinom. (na skali nanosekundi ili piksosekundi.[64] Na temelju zapažanja da se proteini savijaju mnogo brže od ovoga, Levinthal je tada predložio da se ne događa nasumično konformacijsko pretraživanje, te se protein, prema tome, mora presaviti u nizu metastabilnih intermedijarnih stanja.
Energetsko okruženje presavijanja proteina
urediKonfiguracijski prostor proteina tokom presavijanja može se vizualizirati kao energetski pejzaž. Prema Josephu Bryngelsonu i Peteru Wolynesu, proteini slijede "princip minimalne frustracije", što znači da su prirodno evoluirani proteini optimizirali svoj energetsko okruženje,[65] i da je priroda odabrala aminokiselinske sekvence tako da je njihovo savijeno stanje dovoljno stabilno. Pored toga, sticanje presavijenog stanja moralo je postati dovoljno brz proces. Iako je priroda smanjila nivo frustracije u proteinima, određeni stepen ostao je i do danas, što se može primijetiti u prisustvu lokalnih minimuma u energetskom okruženju proteina.
Posljedica ovih evolucijski odabranih sekvenci je da se općenito smatra da proteini imaju globalno "usmjereni energetski pejzaž" (skovao José Onuchic)[66] koji su u velikoj mjeri usmjereni prema matičnom stanju. Ovaj krajolik "lijevak za preklapanje" omogućava proteinu da se savije u prirodno stanje, bilo kojim od velikog broja puteva i intermedijara, umjesto da bude ograničen na jedan mehanizam. Teoriju podržavaju i računarske simulacije modelnih proteina i eksperimentalne studije,[65], a korištena je za poboljšanje metoda za predviđanje strukture proteina i dizajn proteina.[65] Opis presavijanja proteina izravnavanjem okruženja slobodne energije također je u skladu sa 2. zakonom termodinamike.[67] Fizički gledano, razmišljanje o timokruženjima u smislu vizueliziranog potencijala ili ukupnih energetskih površina jednostavno s maksimumima, sedlastim tačkama, minimumima i lijevcima, češće poput geografskih pejzaža, možda je malo zavaravajuće. Relevantni opis zaista je visokodimenziijski fazni prostor u kojem bi mnogostrukosti mogle poprimiti razne složenije topološke oblike.[68]
Nesavijeni polipeptidni lanac započinje na vrhu lijevka, gdje e može pretpostaviti najveći broj nerasvijećenih varijacija i u svom je najvišem energetskom stanju. Ovakvi energetski pejzaži ukazuju na to da postoji veliki broj početnih mogućnosti, ali da je moguća samo jedno matično stanje; međutim, ne otkriva brojne moguće puteve savijanja. Različite molekule istog tačnog proteina mogu biti u mogućnosti da prate marginalno različite puteve savijanja, tražeći različite međuprodukte niže energije, sve dok se postigne ista prirodna struktura.[69] Različiti putevi mogu imati različite frekvencije upotrebe, ovisno o termodinamičkoj povoljnosti svakog puta. To znači da ako se utvrdi da je jedan put termodinamički povoljniji od drugog, vjerovatno će se češće koristiti u potrazi za prirodnom strukturom.[69] Kako se protein počinje savijati i skupljati u različitin konformacijama, uvijek traži termodinamički povoljniju strukturu nego prije i tako nastavlja kroz energetski lijevak. Stvaranje sekundarnih struktura snažan je pokazatelj povećane stabilnosti unutar proteina, a samo će jedna kombinacija sekundarnih struktura koje pretpostavlja okosnica polipeptida imati najmanje energije i stoga će biti prisutna u izvornom stanju proteina.[69] Među prvim strukturama koje se formiraju nakon što se polipeptid počne savijati su alfa-helikse i beta-listove, pri čemu alfa-heliksi mogu nastati za samo 100 nanosekundi, a beta-listovi za jednu mikrosekundu.[28]
U okruženju energetskog lijevka postoji sedlo u kojem se nalazi prijelazno stanje za određeni protein.[28] Prijelazno stanje u dijagrami lijevka energije je konformacija koju mora pretpostaviti svaka molekula tog protein ako će konačno uspostaviti prirodnu strukturu. Nijedan protein ne može poprimiti takvu strukturu bez prethodnog prolaska kroz prijelazno stanje.[28] Prijelazno stanje može se nazvati varijantom ili preuranjenim oblikom prirodnog stanja, a ne samo još jednim posredničkim korakom.[70] Pokazalo se da je savijanje prijelaznog stanja presudno za određivanje brzine, a iako postoji u višem energetskom stanju od izvornog nabora, u velikoj mjeri nalikuje prirodnoj strukturi. Unutar prijelaznog stanja postoji jezgro oko kojeg se protein može saviti, nastalo na načim koji se naziva "kondenzacija nukleacije", gdje struktura počinje kolabirati na jezgro.[70]
Modeliranje savijanja proteina
urediDe novo ili ab initio tehnike za računanje predviđanja strukture proteina povezane su, ali se strogo razlikuju od eksperimentalnih studija presavijanja proteina. Molekulska dinamika (MD) važan je alat za proučavanje presavijanja i dinamike proteina in silico.[71] Prve simulacije savijanja ravnoteže rađene su pomoću implicitnog modela rastvarača i kišobranastog uzimanja uzoraka.[72] Zbog računarskih troškova, simulacije presavijanja sa eksplicitnom vodom ab initio MD, ograničene su na peptide i vrlo male proteine.[73][74] MD-simulacije većih proteina i dalje su ograničene na dinamiku eksperimentalne strukture ili njen razvoj na visokim temperaturama. Dugotrajnim procesima presavijanja (preko oko 1 milisekunde), poput savijanja proteina male veličine (oko 50 ostataka) ili većim, može se pristupiti pomoću grubozrnastih modela.[75][76][77]
Projekt 100 petaFLOP distribuiranog računarstva Folding@home koji je kreirala grupa Vijaya Pande na Stanford University simulira presavijanje proteina koristeći vreijme mirovanja CPU i GPU volonterskih personalnih računara. Cilj projekta je razumijevanje pogrešnog stvaranja proteina i ubrzanje dizajniranja lijekova za istraživanje bolesti.
Duge simulacije kontinuirane putanje izvedene su na Antonu, masivnom paralelnom superračunaru koji je dizajnirao i izgradio D. E. Shaw Research, oko prilagođenih ASIC-a i međusobnih veza. Najduži objavljeni rezultat simulacije izvedene pomoću Antona je simulacija NTL9 od 2,936 milisekundi pri 355 K.[78]
Također pogledajte
urediReference
uredi- ^ Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walters, Peter (2002). "The Shape and Structure of Proteins". Molecular Biology of the Cell; Fourth Edition. New York and London: Garland Science. ISBN 978-0-8153-3218-3. Upotreblja se zastarjeli parametar
|chapterurl=(pomoć) - ^ Anfinsen CB (juli 1972). "The formation and stabilization of protein structure". The Biochemical Journal. 128 (4): 737–49. doi:10.1042/bj1280737. PMC 1173893. PMID 4565129.
- ^ Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002). "3. Protein Structure and Function". Biochemistry. San Francisco: W. H. Freeman. ISBN 978-0-7167-4684-3. Upotreblja se zastarjeli parametar
|chapterurl=(pomoć) - ^ a b Selkoe DJ (decembar 2003). "Folding proteins in fatal ways". Nature. 426 (6968): 900–4. Bibcode:2003Natur.426..900S. doi:10.1038/nature02264. PMID 14685251.
- ^ Alberts, Bruce; Bray, Dennis; Hopkin, Karen; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2010). "Protein Structure and Function". Essential cell biology (Third izd.). New York, NY: Garland Science. str. 120–70. ISBN 978-0-8153-4454-4.
- ^ Kim PS, Baldwin RL (1990). "Intermediates in the folding reactions of small proteins". Annual Review of Biochemistry. 59: 631–60. doi:10.1146/annurev.bi.59.070190.003215. PMID 2197986.
- ^ Jackson SE (1998). "How do small single-domain proteins fold?". Folding & Design. 3 (4): R81-91. doi:10.1016/S1359-0278(98)00033-9. PMID 9710577.
- ^ Kubelka J, Hofrichter J, Eaton WA (februar 2004). "The protein folding 'speed limit'". Current Opinion in Structural Biology. 14 (1): 76–88. doi:10.1016/j.sbi.2004.01.013. PMID 15102453.
- ^ Anfinsen CB (juli 1973). "Principles that govern the folding of protein chains". Science. 181 (4096): 223–30. Bibcode:1973Sci...181..223A. doi:10.1126/science.181.4096.223. PMID 4124164.
- ^ a b c d e f g h Voet, Donald; Voet, Judith G.; Pratt, Charlotte W. (2016). Principles of Biochemistry (Fifth izd.). Wiley. ISBN 978-1-118-91840-1.
- ^ Alexander PA, He Y, Chen Y, Orban J, Bryan PN (juli 2007). "The design and characterization of two proteins with 88% sequence identity but different structure and function". Proceedings of the National Academy of Sciences of the United States of America. 104 (29): 11963–8. Bibcode:2007PNAS..10411963A. doi:10.1073/pnas.0700922104. PMC 1906725. PMID 17609385.
- ^ Rose GD, Fleming PJ, Banavar JR, Maritan A (novembar 2006). "A backbone-based theory of protein folding". Proceedings of the National Academy of Sciences of the United States of America. 103 (45): 16623–33. Bibcode:2006PNAS..10316623R. doi:10.1073/pnas.0606843103. PMC 1636505. PMID 17075053.
- ^ a b Fersht, Alan (1999). Structure and Mechanism in Protein Science: A Guide to Enzyme Catalysis and Protein Folding. Macmillan. ISBN 978-0-7167-3268-6.
- ^ "Protein Structure". Scitable. Nature Education. Pristupljeno 26. 11. 2016.
- ^ Pratt, Charlotte; Cornely, Kathleen (2004). "Thermodynamics". Essential Biochemistry. Wiley. ISBN 978-0-471-39387-0. Pristupljeno 26. 11. 2016.
- ^ Zhang, Gong; Ignatova, Zoya (1. 2. 2011). "Folding at the birth of the nascent chain: coordinating translation with co-translational folding". Current Opinion in Structural Biology. 21 (1): 25–31. doi:10.1016/j.sbi.2010.10.008. ISSN 0959-440X. PMID 21111607.
- ^ van den Berg B, Wain R, Dobson CM, Ellis RJ (august 2000). "Macromolecular crowding perturbs protein refolding kinetics: implications for folding inside the cell". The EMBO Journal. 19 (15): 3870–5. doi:10.1093/emboj/19.15.3870. PMC 306593. PMID 10921869.
- ^ Al-Karadaghi, Salam. "Torsion Angles and the Ramachnadran Plot in Protein Structures". www.proteinstructures.com. Pristupljeno 26. 11. 2016.
- ^ Pace CN, Shirley BA, McNutt M, Gajiwala K (januar 1996). "Forces contributing to the conformational stability of proteins". FASEB Journal. 10 (1): 75–83. doi:10.1096/fasebj.10.1.8566551. PMID 8566551.
- ^ Cui D, Ou S, Patel S (decembar 2014). "Protein-spanning water networks and implications for prediction of protein-protein interactions mediated through hydrophobic effects". Proteins. 82 (12): 3312–26. doi:10.1002/prot.24683. PMID 25204743.
- ^ Tanford C (juni 1978). "The hydrophobic effect and the organization of living matter". Science. 200 (4345): 1012–8. Bibcode:1978Sci...200.1012T. doi:10.1126/science.653353. PMID 653353.
- ^ Deechongkit S, Nguyen H, Powers ET, Dawson PE, Gruebele M, Kelly JW (juli 2004). "Context-dependent contributions of backbone hydrogen bonding to beta-sheet folding energetics". Nature. 430 (6995): 101–5. Bibcode:2004Natur.430..101D. doi:10.1038/nature02611. PMID 15229605.
- ^ Irbäck, Anders; Sandelin, Erik (novembar 2000). "On Hydrophobicity Correlations in Protein Chains". Biophysical Journal. 79 (5): 2252–2258. arXiv:cond-mat/0010390. Bibcode:2000BpJ....79.2252I. doi:10.1016/S0006-3495(00)76472-1. PMC 1301114. PMID 11053106.
- ^ Irbäck, A.; Peterson, C.; Potthast, F. (3. 9. 1996). "Evidence for nonrandom hydrophobicity structures in protein chains". Proceedings of the National Academy of Sciences. 93 (18): 9533–9538. arXiv:chem-ph/9512004. Bibcode:1996PNAS...93.9533I. doi:10.1073/pnas.93.18.9533. PMC 38463. PMID 8790365.
- ^ Wilson, Benjamin A.; Foy, Scott G.; Neme, Rafik; Masel, Joanna (24. 4. 2017). "Young genes are highly disordered as predicted by the preadaptation hypothesis of de novo gene birth". Nature Ecology & Evolution. 1 (6): 0146–146. doi:10.1038/s41559-017-0146. PMC 5476217. PMID 28642936.
- ^ Willis, Sara; Masel, Joanna (septembar 2018). "Gene Birth Contributes to Structural Disorder Encoded by Overlapping Genes". Genetics. 210 (1): 303–313. doi:10.1534/genetics.118.301249. PMC 6116962. PMID 30026186.
- ^ Foy, Scott G.; Wilson, Benjamin A.; Bertram, Jason; Cordes, Matthew H. J.; Masel, Joanna (april 2019). "A Shift in Aggregation Avoidance Strategy Marks a Long-Term Direction to Protein Evolution". Genetics. 211 (4): 1345–1355. doi:10.1534/genetics.118.301719. PMC 6456324. PMID 30692195.
- ^ a b c d e f Dobson CM (decembar 2003). "Protein folding and misfolding". Nature. 426 (6968): 884–90. Bibcode:2003Natur.426..884D. doi:10.1038/nature02261. PMID 14685248.
- ^ a b c Hartl FU (juni 1996). "Molecular chaperones in cellular protein folding". Nature. 381 (6583): 571–9. Bibcode:1996Natur.381..571H. doi:10.1038/381571a0. PMID 8637592.
- ^ a b Hartl FU, Bracher A, Hayer-Hartl M (juli 2011). "Molecular chaperones in protein folding and proteostasis". Nature. 475 (7356): 324–32. doi:10.1038/nature10317. PMID 21776078.
- ^ Kim YE, Hipp MS, Bracher A, Hayer-Hartl M, Hartl FU (2013). "Molecular chaperone functions in protein folding and proteostasis". Annual Review of Biochemistry. 82: 323–55. doi:10.1146/annurev-biochem-060208-092442. PMID 23746257.
- ^ Shortle D (januar 1996). "The denatured state (the other half of the folding equation) and its role in protein stability". FASEB Journal. 10 (1): 27–34. doi:10.1096/fasebj.10.1.8566543. PMID 8566543.
- ^ Lee S, Tsai FT (2005). "Molecular chaperones in protein quality control". Journal of Biochemistry and Molecular Biology. 38 (3): 259–65. doi:10.5483/BMBRep.2005.38.3.259. PMID 15943899.
- ^ Ojeda-May P, Garcia ME (juli 2010). "Electric field-driven disruption of a native beta-sheet protein conformation and generation of a helix-structure". Biophysical Journal. 99 (2): 595–9. Bibcode:2010BpJ....99..595O. doi:10.1016/j.bpj.2010.04.040. PMC 2905109. PMID 20643079.
- ^ van den Berg B, Ellis RJ, Dobson CM (decembar 1999). "Effects of macromolecular crowding on protein folding and aggregation". The EMBO Journal. 18 (24): 6927–33. doi:10.1093/emboj/18.24.6927. PMC 1171756. PMID 10601015.
- ^ Ellis RJ (juli 2006). "Molecular chaperones: assisting assembly in addition to folding". Trends in Biochemical Sciences. 31 (7): 395–401. doi:10.1016/j.tibs.2006.05.001. PMID 16716593.
- ^ Takai K, Nakamura K, Toki T, Tsunogai U, Miyazaki M, Miyazaki J, Hirayama H, Nakagawa S, Nunoura T, Horikoshi K (august 2008). "Cell proliferation at 122 degrees C and isotopically heavy CH4 production by a hyperthermophilic methanogen under high-pressure cultivation". Proceedings of the National Academy of Sciences of the United States of America. 105 (31): 10949–54. Bibcode:2008PNAS..10510949T. doi:10.1073/pnas.0712334105. PMC 2490668. PMID 18664583.
- ^ a b Marusich EI, Kurochkina LP, Mesyanzhinov VV. Chaperones in bacteriophage T4 assembly. Biochemistry (Mosc). 1998;63(4):399-406
- ^ a b c d Chaudhuri TK, Paul S (april 2006). "Protein-misfolding diseases and chaperone-based therapeutic approaches". The FEBS Journal. 273 (7): 1331–49. doi:10.1111/j.1742-4658.2006.05181.x. PMID 16689923.
- ^ a b Soto C, Estrada L, Castilla J (mart 2006). "Amyloids, prions and the inherent infectious nature of misfolded protein aggregates". Trends in Biochemical Sciences. 31 (3): 150–5. doi:10.1016/j.tibs.2006.01.002. PMID 16473510.
- ^ Hammarström P, Wiseman RL, Powers ET, Kelly JW (januar 2003). "Prevention of transthyretin amyloid disease by changing protein misfolding energetics". Science. 299 (5607): 713–6. Bibcode:2003Sci...299..713H. doi:10.1126/science.1079589. PMID 12560553.
- ^ Chiti F, Dobson CM (2006). "Protein misfolding, functional amyloid, and human disease". Annual Review of Biochemistry. 75: 333–66. doi:10.1146/annurev.biochem.75.101304.123901. PMID 16756495.
- ^ Johnson SM, Wiseman RL, Sekijima Y, Green NS, Adamski-Werner SL, Kelly JW (decembar 2005). "Native state kinetic stabilization as a strategy to ameliorate protein misfolding diseases: a focus on the transthyretin amyloidoses". Accounts of Chemical Research. 38 (12): 911–21. doi:10.1021/ar020073i. PMID 16359163.
- ^ Cowtan, Kevin (2001). "Phase Problem in X-ray Crystallography, and Its Solution" (PDF). Encyclopedia of Life Sciences. Macmillan Publishers Ltd, Nature Publishing Group. Pristupljeno 3. 11. 2016.
- ^ Drenth, Jan (5. 4. 2007). Principles of Protein X-Ray Crystallography. Springer Science & Business Media. ISBN 978-0-387-33746-3.
- ^ Taylor, Garry (2003). "The phase problem". Acta Crystallographica Section D. 59 (11): 1881–90. doi:10.1107/S0907444903017815. PMID 14573942.
- ^ Bedouelle H (februar 2016). "Principles and equations for measuring and interpreting protein stability: From monomer to tetramer". Biochimie. 121: 29–37. doi:10.1016/j.biochi.2015.11.013. PMID 26607240.
- ^ Monsellier E, Bedouelle H (septembar 2005). "Quantitative measurement of protein stability from unfolding equilibria monitored with the fluorescence maximum wavelength". Protein Engineering, Design & Selection. 18 (9): 445–56. doi:10.1093/protein/gzi046. PMID 16087653.
- ^ Park YC, Bedouelle H (juli 1998). "Dimeric tyrosyl-tRNA synthetase from Bacillus stearothermophilus unfolds through a monomeric intermediate. A quantitative analysis under equilibrium conditions". The Journal of Biological Chemistry. 273 (29): 18052–9. doi:10.1074/jbc.273.29.18052. PMID 9660761.
- ^ Ould-Abeih MB, Petit-Topin I, Zidane N, Baron B, Bedouelle H (juni 2012). "Multiple folding states and disorder of ribosomal protein SA, a membrane receptor for laminin, anticarcinogens, and pathogens". Biochemistry. 51 (24): 4807–21. doi:10.1021/bi300335r. PMID 22640394.
- ^ Royer CA (maj 2006). "Probing protein folding and conformational transitions with fluorescence". Chemical Reviews. 106 (5): 1769–84. doi:10.1021/cr0404390. PMID 16683754.
- ^ Beatrice M.P. Huyghues-Despointes, C. Nick Pace, S. Walter Englander, and J. Martin Scholtz. "Measuring the Conformational Stability of a Protein by Hydrogen Exchange." Methods in Molecular Biology. Kenneth P. Murphy Ed. Humana Press, Totowa, New Jersey, 2001. pp. 69–92
- ^ Cross, Graham H.; Freeman, Neville J.; Swann, Marcus J. (2008). "Dual Polarization Interferometry: A Real-Time Optical Technique for Measuring (Bio)molecular Orientation, Structure and Function at the Solid/Liquid Interface". Handbook of Biosensors and Biochips. doi:10.1002/9780470061565.hbb055. ISBN 978-0-470-01905-4.
- ^ Bu Z, Cook J, Callaway DJ (septembar 2001). "Dynamic regimes and correlated structural dynamics in native and denatured alpha-lactalbumin". Journal of Molecular Biology. 312 (4): 865–73. doi:10.1006/jmbi.2001.5006. PMID 11575938.
- ^ Minde DP, Maurice MM, Rüdiger SG (2012). "Determining biophysical protein stability in lysates by a fast proteolysis assay, FASTpp". PLOS ONE. 7 (10): e46147. Bibcode:2012PLoSO...746147M. doi:10.1371/journal.pone.0046147. PMC 3463568. PMID 23056252.
- ^ Park C, Marqusee S (mart 2005). "Pulse proteolysis: a simple method for quantitative determination of protein stability and ligand binding". Nature Methods. 2 (3): 207–12. doi:10.1038/nmeth740. PMID 15782190.
- ^ Mashaghi A, Kramer G, Lamb DC, Mayer MP, Tans SJ (januar 2014). "Chaperone action at the single-molecule level". Chemical Reviews. 114 (1): 660–76. doi:10.1021/cr400326k. PMID 24001118.
- ^ Jagannathan B, Marqusee S (novembar 2013). "Protein folding and unfolding under force". Biopolymers. 99 (11): 860–9. doi:10.1002/bip.22321. PMC 4065244. PMID 23784721.
- ^ Jakobi AJ, Mashaghi A, Tans SJ, Huizinga EG (juli 2011). "Calcium modulates force sensing by the von Willebrand factor A2 domain". Nature Communications. 2: 385. Bibcode:2011NatCo...2..385J. doi:10.1038/ncomms1385. PMC 3144584. PMID 21750539.
- ^ Jagannathan B, Elms PJ, Bustamante C, Marqusee S (oktobar 2012). "Direct observation of a force-induced switch in the anisotropic mechanical unfolding pathway of a protein". Proceedings of the National Academy of Sciences of the United States of America. 109 (44): 17820–5. Bibcode:2012PNAS..10917820J. doi:10.1073/pnas.1201800109. PMC 3497811. PMID 22949695.
- ^ Minde DP, Ramakrishna M, Lilley KS (2018). "Biotinylation by proximity labelling favours unfolded proteins". bioRxiv. doi:10.1101/274761.
- ^ Compiani M, Capriotti E (decembar 2013). "Computational and theoretical methods for protein folding". Biochemistry. 52 (48): 8601–24. doi:10.1021/bi4001529. PMID 24187909.
- ^ "Structural Biochemistry/Proteins/Protein Folding - Wikibooks, open books for an open world". en.wikibooks.org. Pristupljeno 5. 11. 2016.
- ^ Levinthal, Cyrus (1968). "Are there pathways for protein folding?" (PDF). Journal de Chimie Physique et de Physico-Chimie Biologique. 65: 44–45. Bibcode:1968JCP....65...44L. doi:10.1051/jcp/1968650044. Arhivirano s originala (PDF), 2. 9. 2009.
- ^ a b c Bryngelson JD, Onuchic JN, Socci ND, Wolynes PG (mart 1995). "Funnels, pathways, and the energy landscape of protein folding: a synthesis". Proteins. 21 (3): 167–95. arXiv:chem-ph/9411008. doi:10.1002/prot.340210302. PMID 7784423.
- ^ Leopold PE; Montal M; Onuchic JN (septembar 1992). "Protein folding funnels: a kinetic approach to the sequence-structure relationship". Proceedings of the National Academy of Sciences of the United States of America. 89 (18): 8721–5. Bibcode:1992PNAS...89.8721L. doi:10.1073/pnas.89.18.8721. PMC 49992. PMID 1528885.
- ^ Sharma, Vivek; Kaila, Ville R.I.; Annila, Arto (2009). "Protein folding as an evolutionary process". Physica A: Statistical Mechanics and Its Applications. 388 (6): 851–62. Bibcode:2009PhyA..388..851S. doi:10.1016/j.physa.2008.12.004.
- ^ Robson, Barry; Vaithilingam, Andy (2008). "Protein Folding Revisited". Molecular Biology of Protein Folding, Part B. Progress in Molecular Biology and Translational Science. 84. str. 161–202. doi:10.1016/S0079-6603(08)00405-4. ISBN 978-0-12-374595-8. PMID 19121702.
- ^ a b c Dill KA, MacCallum JL (novembar 2012). "The protein-folding problem, 50 years on". Science. 338 (6110): 1042–6. Bibcode:2012Sci...338.1042D. doi:10.1126/science.1219021. PMID 23180855.
- ^ a b Fersht AR (februar 2000). "Transition-state structure as a unifying basis in protein-folding mechanisms: contact order, chain topology, stability, and the extended nucleus mechanism". Proceedings of the National Academy of Sciences of the United States of America. 97 (4): 1525–9. Bibcode:2000PNAS...97.1525F. doi:10.1073/pnas.97.4.1525. PMC 26468. PMID 10677494.
- ^ Rizzuti B, Daggett V (mart 2013). "Using simulations to provide the framework for experimental protein folding studies". Archives of Biochemistry and Biophysics. 531 (1–2): 128–35. doi:10.1016/j.abb.2012.12.015. PMC 4084838. PMID 23266569.
- ^ Schaefer M, Bartels C, Karplus M (decembar 1998). "Solution conformations and thermodynamics of structured peptides: molecular dynamics simulation with an implicit solvation model". Journal of Molecular Biology. 284 (3): 835–48. doi:10.1006/jmbi.1998.2172. PMID 9826519.
- ^ Jones, David. "Fragment-based Protein Folding Simulations". University College London.
- ^ "Protein folding" (by Molecular Dynamics).
- ^ Kmiecik S, Gront D, Kolinski M, Wieteska L, Dawid AE, Kolinski A (juli 2016). "Coarse-Grained Protein Models and Their Applications". Chemical Reviews. 116 (14): 7898–936. doi:10.1021/acs.chemrev.6b00163. PMID 27333362.
- ^ Kmiecik S, Kolinski A (juli 2007). "Characterization of protein-folding pathways by reduced-space modeling". Proceedings of the National Academy of Sciences of the United States of America. 104 (30): 12330–5. Bibcode:2007PNAS..10412330K. doi:10.1073/pnas.0702265104. PMC 1941469. PMID 17636132.
- ^ Adhikari AN, Freed KF, Sosnick TR (oktobar 2012). "De novo prediction of protein folding pathways and structure using the principle of sequential stabilization". Proceedings of the National Academy of Sciences of the United States of America. 109 (43): 17442–7. Bibcode:2012PNAS..10917442A. doi:10.1073/pnas.1209000109. PMC 3491489. PMID 23045636.
- ^ Lindorff-Larsen K, Piana S, Dror RO, Shaw DE (oktobar 2011). "How fast-folding proteins fold". Science. 334 (6055): 517–20. Bibcode:2011Sci...334..517L. doi:10.1126/science.1208351. PMID 22034434.