Popravak ekscizijom nukleotida
Nukleotidni ekscizijski popravak je mehanizam popravka DNK.[2] Oštećenje DNK nastaje konstantno zbog hemikalija (npr. interkalacijski agensi), zračenje i drugi mutageni. Postoje tri puta ekscizijskog popravka za popravku jednolančanog oštećenja DNK: popravak ekscizijom nukleotida (NER), bazni ekscizijski popravak (BER) i popravak neslaganja DNK (MMR). Dok BER put može prepoznati specifične neglomazne lezije u DNK, može ispraviti samo oštećene baze koje su uklonjene specifične glikozilaze . Slično tome, MMR put cilja samo neusklađene Watson-Crickovr bazne parove.
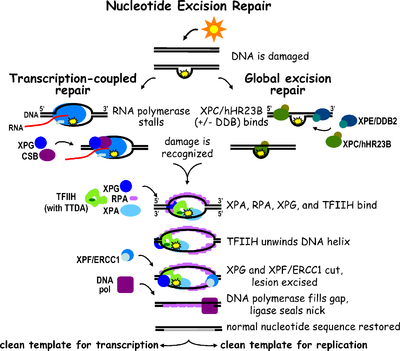
Nukleotidna eksciziona popravka (NER) je posebno važan mehanizam ekscizije koji uklanja oštećenje DNK izazvano ultraljibičastim svjetlom (UV). UV DNK oštećenje rezultira glomaznim DNK-aduktom – ovi adukti su uglavnom timinski dimeri i 6,4-fotoproizvodi. Prepoznavanje oštećenja dovodi do uklanjanja kratkog jednolančanog segmenta DNK koji sadrži leziju. Neoštećena jednolančana DNK ostaje i DNK-polimeraza je koristi kao šablon za sintetiziranje kratke komplementarnih sekvenci. Konačna ligacija za kompletiranje NER-a i formiranje dvolančane DNK izvodi se pomoću DNK-ligaze. NER se može podijeliti na dva potputa: globalni genomski NER (GG-NER ili GGR) i NER povezan s transkripcijom (TC-NER ili TCR). Dva potputa se razlikuju po tome kako prepoznaju oštećenje DNK, ali dijele isti proces za inciziju, popravak i ligaciju lezija.
O važnosti NER-a svjedoče teške ljudske bolesti koje su rezultat urođenih genetičkih mutacija NER proteina. Xeroderma pigmentosum i Cockayneov sindrom su dva primjera bolesti povezanih s NER-om.
Povezani geni s NER-om
uredi| Ljudski gen (protein) | Mišji ortolog | Kvaščev ortolog | Potput | Funkcija u NER-u | GeneCards unos |
|---|---|---|---|---|---|
| CCNH (Ciklin H) | Ccnh | CCL1 | Oba | CDK Aktivator kinaza podjedinica (CAK) | CCNH |
| CDK7 (Ciklin-zavisna kinaza (CDK) 7)) | Cdk7 | KIN28 | Oba | CAK podjedinica | CDK7 |
| CETN2 (Centrin-2) | Cetn2 | Nepoznato | GGR | Prepoznavanje štete; formira kompleks sa XPC | CETN2 |
| DDB1 (DDB1) | Ddb1 | Nepoznato | GGR | Prepoznavanje štete; formira kompleks sa DDB2 | DDB1 |
| DDB2 (DDB2) | Ddb2/Xpe | Nepoznato | GGR | Prepoznavanje štete; regrutuje XPC | DDB2 |
| ERCC1 (ERCC1) | Ercc1 | RAD10 | Oba | Zahvaćen u urezu na 3' strani oštećenja; formira kompleks sa XPF | ERCC1 |
| ERCC2 (XPD) | Ercc2 | RAD3 | Oba | Aktivnost Atpaze i helikaze; transkripcijski faktor podjedinica II H (TFIIH) | ERCC2 |
| ERCC3 (XPB) | Ercc3 | RAD25 | Oba | aktivnost ATPaze i helikaze; transkripcijski faktor podjedinica II H (TFIIH) | ERCC3 |
| ERCC4 (XPF) | Ercc4 | RAD1 | Oba | Zahvaćen u urezu na 3' strani oštećenja; strukturno specifična endonukleaza | ERCC4 |
| ERCC5 (XPG) | Ercc5 | RAD2 | Oba | Zahvaćen u urezu na 5' strani oštećenja; stabilizira TFIIH; strukturno specifična endonukleaza | ERCC5 |
| ERCC6 (CSB) | Ercc6 | RAD26 | TC-NER | Faktor elongacije transkripcije; uključeni u spajanje transkripcije i remodeliranje hromatina | ERCC6 |
| ERCC8 (CSA) | Ercc8 | RAD28 | TC-NER | Kompleks ubikvitin-ligaze; komunicira sa CSB-om i p44 TFIIH-a | ERCC8 |
| LIG1 (DNK ligaza I) | Lig1 | CDC9 | Oba | Finalna ligacija | LIG1 |
| MNAT1 (MNAT1) | Mnat1 | TFB3 | Oba | Stabilizira CAK kompleks | MNAT1 |
| MMS19 (MMS19) | Mms19 | MET18 | Oba | Interagira sa XPD i XPB podjedinicama TFIIH helikaza | MMS19 |
| RAD23A (RAD23A) | Rad23a | RAD23 | GGR | Prepoznavanje štete; formira kompleks sa XPC | RAD23A |
| RAD23B (RAD23B) | Rad23b | RAD23 | GGR | Prepoznavanje oštećenja, formira kompleks sa XPC | RAD23B |
| RPA1 (RPA1) | Rpa1 | RFA1 | Oba | Podjedinica kompleksa RFA | RPA1 |
| RPA2 (RPA2) | Rpa2 | RFA2 | Oba | Podjedinica kompleksa RFA | RPA2 |
| TFIIH (Faktor transkripcije II H]]) | Gtf2h1-3 | Tfb1 Ssl1 Tfb4 | Oba | Uključen u rez, formira kompleks oko lezija | GTF2H1 GTF2H2 [https ://www.genecards.org/cgi-bin/carddisp.pl?gene=GTF2H3 GTF2H3] |
| XAB2 (XAB2) | Xab2 | SYF1 | TC-NER | Prepoznavanje štete; komunicira sa XPA, CSA i CSB | XAB2 |
| XPA (XPA) | Xpa | RAD14 | Oba | Prepoznavanje štete | XPA |
| XPC (XPC) | Xpc | RAD4 | GGR | Prepoznavanje štete | XPC |
Također pogledajte
uredi- Popravak ekscizije baze (BER)
- Popravak neusklađenosti (MMR)
Reference
uredi- ^ Fuss JO, Cooper PK (juni 2006). "DNA repair: dynamic defenders against cancer and aging". PLOS Biology. 4 (6): e203. doi:10.1371/journal.pbio.0040203. PMC 1475692. PMID 16752948.
- ^ Carroll SB; Wessler SR; Griffiths AJFl; Lewontin RC (2008). Introduction to genetic analysis. New York: W.H. Freeman and Co. str. 534. ISBN 978-0-7167-6887-6.
Dopunska literatura
uredi- Ellenberger T, Friedberg EC, Walker GS, Wolfram S, Wood RJ, Schultz R (2006). DNA repair and mutagenesis. Washington, D.C: ASM Press. ISBN 978-1-55581-319-2.
- Satoh MS, Hanawalt PC (septembar 1996). "TFIIH-mediated nucleotide excision repair and initiation of mRNA transcription in an optimized cell-free DNA repair and RNA transcription assay". Nucleic Acids Research. 24 (18): 3576–3582. doi:10.1093/nar/24.18.3576. PMC 146147. PMID 8836185. Article on the relation between TFIIH and NER
- Frit P, Kwon K, Coin F, Auriol J, Dubaele S, Salles B, Egly JM (decembar 2002). "Transcriptional activators stimulate DNA repair". Mol. Cell. 10 (6): 1391–1401. doi:10.1016/S1097-2765(02)00732-3. PMID 12504014.
- Mellon I (septembar 2005). "Transcription-coupled repair: a complex affair". Mutat. Res. 577 (1–2): 155–161. doi:10.1016/j.mrfmmm.2005.03.016. PMID 15913669.