Androstendion
Androstenedion ili 4-androstenedion (skraćeno A4 ili Δ4-dion), poznat i kao androst-4-en-3,17-dion, je endogeni slabi androgeni steroidni hormon i intermedijar u biosintezi estrona i testosterona iz dehidroepiandrosterona (DHEA). Usko je povezan sa androstenediolom (androst-5-en-3β, 17β-diol).
| Androstendion | ||
|---|---|---|
| Naziv lijeka | Androstendion | |
| Druga imena | A4; Δ4-dion; Androstendion; Androst-4-en-3,17-dion; 4-Androsten-3,17-dion; 17-Ketotestosteron; 17-Oksotestosteron | |
| Grupa | Hormonski lijekovi | |
| ||
| CAS registarski broj | 63-05-8 | |
| ||
| Stručne informacije | ||
| ||
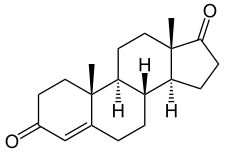  Ime po IUPAC (8R,9S,10R,13S,14S)-10,13-dimetil-2,6,7,8,9,11,12,14,15,16-dekahidro-1H-ciklopenta[a]fenantren-3,17-dion | ||
| Sumarna formula | C19H26O2 | |
| Tačka ključanja | 173-174[1] | |
| ||
| Metabolizam | Jetreni | |
| Izlučivanje | Bubrežno PubChem: 6128 | |
Biološka funkcija
urediAndrostenedion je u tijelu preteča testosterona i drugih androgena, kao i estrogena poput estrona. Osim što funkcionira kao endogeni prohormon, ima i slabu androgenu aktivnost.
Utvrđeno je da androstenedion ima određenu estrogenu aktivnost, slično ostalim metabolitima DHEA.[2] Međutim, za razliku od androstenediola, njegov afinitet za receptor estrogena je vrlo nizak, sa manje od 0,01% afiniteta estradiola za i ERα i ERβ.[3]
Biosinteza
urediAndrostenedion je uobičajeni preteča androgena i estrogena, spolnih hormona.[5]
Androstendion se može biosintetizirati na jedan od dva načina. Primarni put uključuje konverziju 17α-hidroksipregnenolona u DHEA, putem 17,20-liaze, uz naknadnu konverziju DHEA u androstenedion putem enzima 3β-hidroksisteroidne dehidrogenaze. Sekundarni put uključuje konverziju 17α-hidroksiprogesterona, najčešće preteče kortizola u androstenedion, direktno putem 17,20-liaze. Dakle, 17,20-liaza je potrebna za sintezu androstenediona, bez obzira da li se uklanja odmah ili u jednom koraku.
Androstenedion se proizvodi u nadbubrežnim žlijezdama i gonadama. Proizvodnjom androstenediona nadbubrežne žlijezde upravlja adrenokortikotropni hormon (ACTH), dok proizvodnju gonadnog androstenediona kontroliraju gonadotropin. Kod žena u premenopauzi nadbubrežne žlijezde i jajnici proizvode oko polovine ukupnog androstenediona (oko 3 mg/dan). Nakon menopauze proizvodnja androstenediona prepolovljena je, prvenstveno zbog smanjenja steroida koji luči jajnik. Ipak, androstenedion je glavni steroid koji proizvodi postmenopauzni jajnik.
Dio androstenediona se takođe izlučuje u plazmu i može se pretvoriti u perifernim tkivima u testosteron i estrogene.
| Spol | Spolni hormon | Reproduktivna faza |
Krvna stopa proizvodnje |
Gonadna stopa sekrecije |
Stopa metaboličkog klirensa |
Referentni raspon (serumski nivo) | |
|---|---|---|---|---|---|---|---|
| SI jedinice | Ne-SI jedinice | ||||||
| Muškarci | Androstenedion | –
|
2,8 mg/dan | 1,6 mg/dan | 2.200 L/dan | 2,8–7,3 nmol/L | 80–210 ng/dL |
| Testosteron | –
|
6,5 mg/dan | 6,2 mg/dan | 950 L/dan | 6,9–34,7 nmol/L | 200–1000 ng/dL | |
| Estron | –
|
150 μg/dan | 110 μg/dan | 2.050 L/dan | 37–250 pmol/L | 10–70 pg/mL | |
| Estradiol | –
|
60 μg/dan | 50 μg/dan | 1.600 L/dan | <37–210 pmol/L | 10–57 pg/mL | |
| Estron-sulfat | –
|
80 μg/dan | Neznačajno | 167 L/dan | 600–2.500 pmol/L | 200–900 pg/mL | |
| Žene | Androstenedion | –
|
3,2 mg/dan | 2,8 mg/dan | 2.000 L/dan | 3,1–12,2 nmol/L | 89–350 ng/dL |
| Testosteron | –
|
190 μg/dan | 60 μg/dan | 500 L/dan | 0,7–2,8 nmol/L | 20–81 ng/dL | |
| Estron | Folikulska faza | 110 μg/dan | 80 μg/dan | 2.200 L/dan | 110–400 pmol/L | 30–110 pg/mL | |
| Luteusna faza | 260 μg/dan | 150 μg/dan | 2.200 L/dan | 310–660 pmol/L | 80–180 pg/mL | ||
| Postmenopauza | 40 μg/dan | Neznačajno | 1.610 L/dan | 22–230 pmol/L | 6–60 pg/mL | ||
| Estradiol | Folikulska faza | 90 μg/dan | 80 μg/dan | 1200 L/dan | <37–360 pmol/L | 10–98 pg/mL | |
| Luteusna faza | 250 μg/dan | 240 μg/dan | 1.200 L/dan | 699–1250 pmol/L | 190–341 pg/mL | ||
| Postmenopauza | 6 μg/dan | Neznačajno | 910 L/dan | <37–140 pmol/L | 10–38 pg/mL | ||
| Estron-sulfat | Folikulska faza | 100 μg/dan | Neznačajno | 146 L/dan | 700–3.600 pmol/L | 250–1.300 pg/mL | |
| Luteusna faza | 180 μg/dan | 146 L/dan | 1.100–7.300 pmol/L | 400–2.600 pg/mL | |||
| Progesteron | Folikulska faza | 2 mg/dan | 1,7 mg/dan | 2.100 L/dan | 0,3–3 nmol/L | 0,1–0,9 ng/mL | |
| Luteusna faza | 25 mg/dan | 24 mg/dan | 2.100 L/dan | 19–45 nmol/L | 6–14 ng/mL | ||
Napomene:
Koncentracija steroida u cirkulaciji određuje se brzinom kojom se on luči iz žlijezda, brzinom metabolizma prekursora ili prehormona u steroid i brzinom kojom ga tkiva izlučuju i metaboliziraju.
Stopa sekrecije steroida odnosi se na ukupno lučenje spoja iz žlijezde po jedinici vremena. Stope sekrecije procjenjivane su uzorkovanjem venskog izliva iz žlijezde tokom vremena i oduzimanjem arterijskog i perifernog venskog hormona.
Metabolički klirens steroida definira se kao količina krvi koja je u potpunosti očišćena od hormona u jedinici vremena.
Stopa proizvodnje steroidnog hormona odnosi se na ulazak u krv spoj iz svih mogućih izvora, uključujući sekreciju iz žlijezda i pretvorbu prohormona u steroid koji nas zanima. U stabilnom stanju količina hormona koja ulazi u krv iz svih izvora bit će jednaka brzini kojom se uklanja (stopa metaboličkog klirensa) pomnožena sa koncentracijom u krvi (stopa proizvodnje = stopa metaboličkog klirensa × koncentracija). Ako je mali doprinos metabolizma prohormona cirkulacijskom bazenu steroida, tada će se stopa proizvodnje približiti brzini sekrecije.
Izvori: [6][7]
Metabolizam
urediAndrostenedion se pretvara u testosteron ili estron. Za konverziju androstenediona u testosteron potreban je enzim 17β-hidroksisteroidna dehidrogenaza. Androstenedion se oslobađa u krv iz tekinih ćelija. Za konverziju androstenediona u estron potreban je enzim aromataza. Androstenedion je supstrat za proizvodnju estrogena, u ćelijama granuloze koje proizvode aromatazu. Dakle, ćelije teke i ćelije granuloze rade zajedno, kako bi stvorile estrogene.[8]
Androstandion je 5α-reducirani metabolit 4-androstenediona, koji služi kao intermedijar u biosintezi androgena i neurosteroida androsterona.[9]
Reference
uredi- ^ "Androstenedione Compound Summary". PubChem. National Center for Biotechnology Information. U.S. National Library of Medicine.
- ^ Miller KK, Al-Rayyan N, Ivanova MM, Mattingly KA, Ripp SL, Klinge CM, Prough RA (January 2013). "DHEA metabolites activate estrogen receptors alpha and beta". Steroids. 78 (1): 15–25. doi:10.1016/j.steroids.2012.10.002. PMC 3529809. PMID 23123738.
- ^ Kuiper GG, Carlsson B, Grandien K, Enmark E, Häggblad J, Nilsson S, Gustafsson JA (March 1997). "Comparison of the ligand binding specificity and transcript tissue distribution of estrogen receptors alpha and beta". Endocrinology. 138 (3): 863–70. doi:10.1210/endo.138.3.4979. PMID 9048584.
- ^ Häggström, Mikael; Richfield, David (2014). "Diagram of the pathways of human steroidogenesis". WikiJournal of Medicine. 1 (1). doi:10.15347/wjm/2014.005. ISSN 2002-4436.
- ^ Devlin, Thomas M. (2010). Textbook of Biochemistry: with Clinical Correlations (7th izd.). Hoboken, NJ: John Wiley & Sons. str. 432. ISBN 978-0-470-28173-4.
- ^ Strauss, Jerome F. (2013). "The Synthesis and Metabolism of Steroid Hormones". u Jerome F. Strauss; Robert L. Barbieri (ured.). Yen & Jaffe's Reproductive Endocrinology: Physiology, Pathophysiology, and Clinical Management (7 izd.). Elsevier Health Sciences. str. 66–92. doi:10.1016/B978-1-4557-2758-2.00004-4. ISBN 978-1-4557-2758-2.
- ^ Strauss, Jerome F.; FitzGerald, Garret A. (2019). "Steroid Hormones and Other Lipid Molecules Involved in Human Reproduction". u Jerome F. Strauss; Robert L. Barbieri (ured.). Yen & Jaffe's Reproductive Endocrinology: Physiology, Pathophysiology, and Clinical Management (8 izd.). Elsevier Health Sciences. str. 75–114. doi:10.1016/B978-0-323-47912-7.00004-4. ISBN 978-0-323-58232-2.
- ^ Boulpaep, Emile L.; Boron, Walter F. (2005). Medical Physiology: A Cellular and Molecular Approach (Updated izd.). Philadelphia, Pa.: Elsevier Saunders. str. 1155. ISBN 978-1-4160-2328-9.
- ^ Paba S, Frau R, Godar SC, Devoto P, Marrosu F, Bortolato M (2011). "Steroid 5α-reductase as a novel therapeutic target for schizophrenia and other neuropsychiatric disorders". Current Pharmaceutical Design. 17 (2): 151–67. doi:10.2174/138161211795049589. PMID 21361868.
Vanjski linkovi
urediŠablon:Steroidi Šablon:Modulatori androgenih receptora Šablon:Modulatori estrogenih receptora