Limfom pločastih ćelija
Limfom plaštanih ćelija (MCL) je tip ne-Hodgkinovog limfoma (NHL), koji obuhvata oko 6% NHL slučajeva.[1][2] U Sjedinjenim Državama 2015. bilo je samo oko 15.000 ovakvih pacijenata Ime je dobio po zoni plašta limfnih čvorova.
| Limfom plaštanih ćelija | |
|---|---|
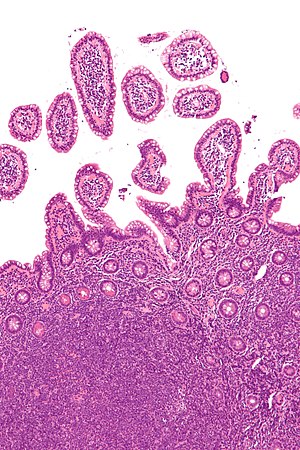 | |
| Mikrografija limfoma plaštanih ćelija (donji deo slike) u biopsiji terminalnog ileuma (boja H&E) | |
| Specijalnost | Hematologija i onkologija |
MCL je podtip B-ćelijskog limfoma, zbog CD5 pozitivnih na antigen nevinih pregerminalnih B-ćelija unutar zone plašta koja okružuje normalne folikule germ-centra. MCL ćelije općenito pretjerano eksprimiraju ciklin D1 zbog translokacije t(11:14)[3], hromosomska translokacija u DNK. Konkretno, translokacija je na t(11;14)(q13;q32).[4][5]

Znakovi i simptomi
urediPri postavljanju dijagnoze, pacijenti su obično u 60-im godinama i javljaju se svom ljekaru s uznapredovalom bolešću. Otprilike polovina ima B-simptome kao što su groznica, noćno znojenje ili neobjašnjivi gubitak težine (preko 10% tjelesne težine). Uvećani limfni čvorovi (naprimjer, "izbočina" na vratu, pazuhu ili preponama) ili povećanje slezine su obično prisutni. Zahvaćenost koštane srži, jetre i gastrointestinalnog trakta javlja se relativno rano u toku bolesti.[6] Prijavljeno je da je limfom ćelija plašta u rijetkim slučajevima povezan s teške alergijske reakcije na ujede komaraca. Ove reakcije uključuju opsežne alergijske reakcije na ubode komaraca, koje se kreću od jako uvećanih mjesta uboda koja mogu biti bolna i uključivati nekrozu do sistemskih simptoma (npr. groznica, otečeni limfni čvorovi, bol u trbuhu i dijareja), ili, u izuzetno rijetkim slučajevima, životno prijeteća anafilaksa. U nekoliko od ovih slučajeva, alergijske reakcije na ujed komaraca (MBA) dogodila se prije dijagnoze MCL-a, što sugerira da MBA može biti manifestacija limfoma plaštanih ćelija u ranom razvoju.[7][8]
Patogeneza
urediMCL, kao i većina karcinoma, posljedica je sticanja kombinacije (nenaslijeđenih) genetičkih mutacija u somatskim ćelijama. Ovo dovodi do klonske ekspanzije malignih B-limfocita. Faktori koji iniciraju genetičke promjene obično se ne mogu identificirati i obično se javljaju kod ljudi bez posebnih faktora rizika za razvoj limfoma. Budući da se radi o stečenom genetičkom poremećaju, MCL nije ni zarazan.
Obilježavajuća karakteristika MCL-a je mutacija i prekomjerna ekspresija ciklina D1, gena ćelijskog ciklusa, koji doprinosi abnormalnoj proliferaciji malignih ćelija. MCL ćelije također mogu biti otporne na lijekom izazvane apoptoze, otežava liječenje hemoterapijom ili zračenjem. Ćelije zahvaćene MCL proliferiraju u "čvorićima" ili "difuzno", s dvije glavne citološke varijante, "tipskm" ili "blastnom". Tipski slučajevi su sa malim do srednje velikim ćelijama, sa nepravilnim jedrima. Blastne (blastoidne) varijante imaju ćelije srednje velike do onih sa fino dispergovanim hromatinom i agresivnije su po prirodi.[9]
Dijagnoza
urediDijagnoza općenito zahtijeva obojene prteparate hirurški uklonjenog dijela limfnog čvora na stakalcu. Uobičajeno se koriste i drugi metodi, uključujući citogenetičke i fluorescentne in situ hibridizacije (FISH). Lančana reakcija polimeraze (PCR) i CER3 klonotipski prajmeri su dodatni metodi, ali se rjeđe koriste.
Profil imunofenotipa sastoji se od CD5+ (u oko 80% slučajeva.[10] CD10 –/+, a obično je CD5+ i CD10–.[11] CD20+, CD23–/+ (iako plus u rijetkim slučajevima). Općenito, ciklin D1 je izražen. Cyclin D1-negativni limfom ćelija plašta može se dijagnosticirati otkrivanjem SOX11-markera. Obrada limfoma plaštanih ćelija slična je obradi mnogih indolentnih limfoma i određenih agresivnih limfoma.
Limfom plaštanih ćelija je sistemska bolest sa čestim zahvatanjem koštane srži i gastrointestinalnog trakta (općenito ima polipoza u sluznici). Postoji i neuobičajena leukemijska faza, obilježena prisustvom u krvi. Budući da limfom plaštnih ćelija može predstavljati limfomatoznu polipozu coli i da je zahvaćenost debelog crijeva uobičajena, kolonoskopija se smatra rutinskim dijelom evaluacije. Gornja endoskopija i CT skeniranje vrata mogu biti od pomoći u odabranim slučajevima. Kod nekih pacijenata sa blastnom varijantom, radi se slabinska punkcija kako bi se procijenila zahvaćenost kičmene tečnosti.
Tretmani
urediNe postoje dokazani standardi liječenja MCL-a, a među stručnjacima ne postoji konsenzus o tome kako ga optimalno liječiti.[12] Dostupni su mnogi režimi i često imaju dobre stope odgovora, ali pacijenti gotovo uvijek imaju progresiju bolesti nakon hemoterapije. Svaki relaps je obično teže liječiti, a relaps je općenito brži. Dostupni su režimi koji liječe relapse, a novi pristupi se testiraju. Zbog gore navedenih faktora, mnogi pacijenti s MCL-om se upisuju u klinička ispitivanja kako bi dobili najnovije tretmane,
U općoj upotrebi su četiri klase tretmana: hemoterapija, imunoterapija, radioimunoterapija i biološki agensi. Faze liječenja su općenito: prva linija, nakon dijagnoze, konsolidacija, nakon prve linije odgovora (da bi se produžile remisije) i recidiv.
Prognoza
urediKlinički napredak u poznavanju limfoma plaštanih ćelija (MCL) doveo je do transformacije standardnih algoritama liječenja. Prva linija kombinovana terapijama rituksimabom, indukcija na bazi citarabina u visokim dozama kod mlađih pacijenata i inhibitori mruton tirozin-kinaza (BTK) u okruženju relapsa, svi su pokazali prednost u preživljavanju u kliničkim ispitivanjima (Wang et al, 2013; Eskelund et al, 2016; Rule et al, 2016). Ove prakse su postepeno postale ugrađene u kliničku praksu i podaci iz stvarnog svijeta su zabilježili odgovarajuća poboljšanja u preživljavanju pacijenata (Abrahamsson et al, 2014; Leux et al, 2014).[13]
Svekupna 5-godišnja stopa preživljavanja za MCL je općenito 50%[14] (advanced stage MCL) to 70%[15] (za ograničene stadije MCL).
Međunarodni prognostički indeks limfoma plaštanih ćelija (MIPI) izveden je iz skupa podataka od 455 pacijenata sa MCL u uznapredovalom stadiju liječenih u nizu kliničkih ispitivanja u Njemačkoj/Evropi. Od populacije koja se može procijeniti, približno 18% je liječeno terapijom visokih doza i transplantacijom matičnih ćelija u prvoj remisiji. MIPI može klasificirati pacijente u tri rizične grupe: nizak rizik (medijana preživljavanja nije postignuta nakon praćenja od 32 mjeseca i 5-godišnja stopa OS od 60%), srednji rizik (medijana preživljavanja 51 mjesec) i visok rizik (medijana preživljavanje 29 mjeseci). Pored četiri nezavisna prognostička faktora uključena u model, indeks proliferacije ćelija (Ki-67) takođe ima dodatnu prognostičku važnost. Kada je Ki67 dostupan, može se izračunati biološki MIPI.[16]
Ki-67 je pokazatelj koliko brzo ćelije sazrevaju i izražen je u rasponu od oko 10% do 90%. Što je procenat manji, to je manja brzina zrelosti, a bolest je indolentnija. Katzenberger et al. prikazuju grafiku preživljavanja u odnosu na vrijeme za podgrupe pacijenata s različitim Ki-67 indeksima. Pokazuju srednje vrijeme preživljavanja od oko godinu dana za 61–90% Ki-67 i skoro četiri godine za 5–20% Ki-67 indeks.
MCL tipovi ćelija mogu pomoći u prognozi na subjektivan način. Blastni tip uključuje veće ćelije. Difuzno se šire kroz limfni čvor. Čvorićne su male grupe sakupljenih ćelija koje se šire kroz čvor. Difuzni i čvorićnii su slični u ponašanju. Blastni brže raste i teže je postići duge remisije. Neki su mislili da se nakon dužeg vremena izvjesni neblastni MCL pretvara u blastni. Iako je preživljavanje većine blastnih pacijenata kraće, neki podaci pokazuju da 25% pacijenata sa blastnom MCL preživi do pet godina. To je duže od difuznog tipa i skoro jednako dugo kao kod čvorićnog (skoro sedam godina). Beta-2 mikroglobulin je još jedan faktor rizika za MCL koji se prvenstveno koristi za pacijente sa transplantacijom. Vrijednosti manje od tri dale su 95% ukupnog preživljavanja do šest godina za auto SCT, gdje više od tri daje medijanu od 44 najdužeg ukupnog preživljavanja za auto SCT (Khouri 03). Testiranje na visoke nivoe laktat-dehidrogenaze (LDH) kod NHL pacijenata je korisno jer se LDH oslobađa kada se tkiva razgrađuju iz „bilo kojeg“ razloga. Iako se ne može koristiti kao jedini način dijagnosticiranja NHL-a, to je surogat za praćenje tumorskog opterećenja kod onih koji su dijagnosticirani drugim sredstvima. Normalni raspon je otprilike 100–190.
Epidemiologija
urediOko 6% slučajeva neHodkinovog limfoma su limfomi plaštanih ćelija.[2] Omjer oboljelih muškaraca i žena je oko 4:1.[2]
Također pogledajte
urediReference
uredi- ^ "Mantle Cell Lymphoma Facts" (PDF). lls.org. Arhivirano s originala (PDF), 9. 2. 2015. Pristupljeno 10. 4. 2018.
- ^ a b c Skarbnik AP, Goy AH (januar 2015). "Mantle cell lymphoma: state of the art". Clin Adv Hematol Oncol. 13 (1): 44–55. PMID 25679973.
- ^ "t(11;14)(q13;q32) IGH/CCND1". atlasgeneticsoncology.org. Pristupljeno 10. 4. 2018.
- ^ Li JY, Gaillard F, Moreau A, et al. (maj 1999). "Detection of translocation t(11;14)(q13;q32) in mantle cell lymphoma by fluorescence in situ hybridization". Am. J. Pathol. 154 (5): 1449–52. doi:10.1016/S0002-9440(10)65399-0. PMC 1866594. PMID 10329598.
- ^ Barouk-Simonet E, Andrieux J, Copin MC, et al. (2002). "TPA stimulation culture for improved detection of t(11;14)(q13;q32) in mantle cell lymphoma". Ann. Genet. 45 (3): 165–8. doi:10.1016/S0003-3995(02)01122-X. PMID 12381451.
- ^ Leukemia&Lymphoma Society (2014). "Mantle Cell Lymphoma Facts" (PDF). www.LLS.org. Arhivirano s originala (PDF), 9. 2. 2015. Pristupljeno 27. 1. 2022.
- ^ Tatsuno K, Fujiyama T, Matsuoka H, Shimauchi T, Ito T, Tokura Y (juni 2016). "Clinical categories of exaggerated skin reactions to mosquito bites and their pathophysiology". Journal of Dermatological Science. 82 (3): 145–52. doi:10.1016/j.jdermsci.2016.04.010. PMID 27177994.
- ^ Kyriakidis I, Vasileiou E, Karastrati S, Tragiannidis A, Gompakis N, Hatzistilianou M (decembar 2016). "Primary EBV infection and hypersensitivity to mosquito bites: a case report". Virologica Sinica. 31 (6): 517–520. doi:10.1007/s12250-016-3868-4. PMC 8193400 Provjerite vrijednost parametra
|pmc=(pomoć). PMID 27900557. S2CID 7996104. - ^ Goy, Andre. "Mantle Cell Lymphoma: An Update for Clinicians". Medscape. Pristupljeno 18. 10. 2007.
- ^ Stanford School of Medicine: "Mantle Cell Lymphoma, Differential Diagnosis" [1] Arhivirano 2. 12. 2020. na Wayback Machine
- ^ Barekman CL, Aguilera NS, Abbondanzo SL (juli 2001). "Low-grade B-cell lymphoma with coexpression of both CD5 and CD10. A report of 3 cases". Arch. Pathol. Lab. Med. 125 (7): 951–3. doi:10.5858/2001-125-0951-LGBCLW. PMID 11419985.
- ^ Rajabi B, Sweetenham JW (2015). "Mantle cell lymphoma: observation to transplantation". Ther Adv Hematol. 6 (1): 37–48. doi:10.1177/2040620714561579. PMC 4298490. PMID 25642314.
- ^ British Journal of Haematology 20 November 2018
- ^ Most recent values in:Herrmann A, Hoster E, Zwingers T, et al. (februar 2009). "Improvement of overall survival in advanced stage mantle cell lymphoma". J. Clin. Oncol. 27 (4): 511–8. doi:10.1200/JCO.2008.16.8435. PMID 19075279.
- ^ Leitch HA, Gascoyne RD, Chhanabhai M, Voss NJ, Klasa R, Connors JM (oktobar 2003). "Limited-stage mantle-cell lymphoma". Ann. Oncol. 14 (10): 1555–61. doi:10.1093/annonc/mdg414. PMID 14504058.
- ^ Hoster E, Dreyling M, Klapper W, et al. (januar 2008). "A new prognostic index (MIPI) for patients with advanced-stage mantle cell lymphoma". Blood. 111 (2): 558–65. doi:10.1182/blood-2007-06-095331. PMID 17962512.
Dopunska literatura
uredi- Cohen JB, Zain JM, Kahl BS (2017). "Current Approaches to Mantle Cell Lymphoma: Diagnosis, Prognosis, and Therapies". Am Soc Clin Oncol Educ Book. 37 (37): 512–25. doi:10.1200/EDBK_175448. PMID 28561694.
- Dreyling M, Ferrero S, Hermine O (novembar 2014). "How to manage mantle cell lymphoma". Leukemia. 28 (11): 2117–30. doi:10.1038/leu.2014.171. PMID 24854989. S2CID 22105743.
- Schieber M, Gordon LI, Karmali R (2018). "Current overview and treatment of mantle cell lymphoma". F1000Res. 7: 1136. doi:10.12688/f1000research.14122.1. PMC 6069726. PMID 30109020.