Mitomicin
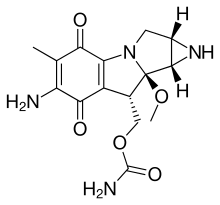
Mitomicini su porodica prirodnih proizvoda koji sadrže aziridin, izolovani iz Streptomyces caespitosus ili Streptomyces lavendulae.[1][2] Uključuju mitomicin A, mitomicin B i mitomicin C. Kada se naziv mitomicin pojavljuje sam, obično se odnosi na mitomicin C, njegov međunarodni nevlasnički naziv. Mitomicin C koristi se kao lijek za različite poremećaje povezane s rastom i širenjem ćelija.
Biosinteza
urediOpćenito, biosinteza svih mitomicina odvija se kombinacijom 3-amino-5-hidroksibenzojeve kiseline (AHBA), D-glukozamina i karbamoil-fosfata , da se formira jezgro mitozana, nakon čega slijede specifični koraci sklapanja.[3] Ključni intermedijer, AHBA, uobičajen je prekursor drugim lijekovima protiv raka, kao što su rifamicin i ansamicin.
Konkretno, biosinteza počinje dodatkom fosfoenolpiruvata (PEP) u eritroza-4-fosfat (E4P) s još neotkrivenim enzimom, koji se zatim amonira da bi se dobio 4-amino-3-deoksi-D-arabino-heptulozonska kiselina-7-fosfat (aminoDHAP). Zatim, DHQ sintaza katalizira zatvaranje prstena, da bi se dobio 4-amino3-dehidrokinat (aminoDHQ), koji se zatim podvrgava dvostrukoj oksidaciji preko aminoDHQ dehidrataze da bi nastao 4-amino-dehidroshikimat (aminoDHS). Ključni intermedijer, 3-amino-5-hidroksibenzojeva kiselina (AHBA), nastaje aromatizacijom pomoću AHBA sintaze.
Sinteza ključnog intermedijera, 3-amino-5-hidroksi-benzojeve kiseline.
Mitozansko jezgro se sintetiše kao što je prikazano u nastavku kondenzacijom AHBA i D-glukozamin, iako nije okarakterisan nijedan specifičan enzim koji posreduje u ovoj transformaciji. Kada dođe do ove kondenzacije, mitozansko jezgro se prilagođava različitim enzimima. I redoslijed i identitet ovih koraka tek treba da se utvrdi.
- Potpuna redukcija C-6 – Vjerovatno preko F420 zavisne tetrahidrometanopterin (H4MPT) reduktaze i H4MPT:CoM metiltransferaze
- Hidroksilacija C-5, C-7 (poslije toga transaminacija) i C-9a. – Vjerovatno putem citokrom P450 monooksigenaze ili benzoat hidroksilaze
- O-metilacija na C-9a – Vjerovatno preko metiltransferaze zavisne od SAM
- Oksidacija na C-5 i C8 – nepoznato
- Intramolekularna aminacija u aziridin – nepoznato
- Karbamoilacija na C-10 – karbamoil transferaza, pri čemu je karbamoil-fosfat (C4P) izveden iz L-citrulina ili L-arginina
Biološki učinci
urediU bakteriji Legionella pneumophila, mitomicin C indukuje kompetentnost za transformaciju.[4] Prirodna transformacija je proces prijenosa DNK između ćelija i smatra se oblikom bakterijske seksualne interakcije. U voćnoj mušici Drosophila melanogaster, izloženost mitomicinu C povećava rekombinaciju tokom mejoze, ključnog stadija seksualnog ciklusa.[5] U biljci Arabidopsis thaliana, mutantni sojevi defektni u genima neophodnim za rekombinaciju tokom mejoze i mitoze su preosjetljivi na ubijanje mitomicinom C.[6]
Tipovi
urediOd 17 prirodnih mitomicina poznatih 2009. godine, 16 je biološki aktivnih, pokazujući ili antibiotska ili citostatička svojstva.[7]
Medicinska upotreba i istraživanje
urediPokazalo se da mitomicin C ima aktivnost protiv stacionarnih faza perzistiranja uzrokovanog putem Borrelia burgdorferi, faktorom lajmske bolesti.[8][9] Mitomicin C se koristi za liječenje raka pankreasa i želuca,[10] i pod kliničkim istraživanjem zbog svog potencijala za liječenje gastrointestinalne strikture,[11] zacjeljivanje rana od glaukomske operacije,[12] ekscimerne laserske operacije rožnjača[13] i endoskopskih dakriocistorhinostomija.[14]
Reference
uredi- ^ Clokie, Martha R. J.; Kropinski, Andrew M. (Andrew Maitland Boleslaw) (2009). Bacteriophages : methods and protocols. Humana Press. ISBN 9781603271646. OCLC 297169927.
- ^ Danshiitsoodol N, de Pinho CA, Matoba Y, Kumagai T, Sugiyama M (2006). "The mitomycin C (MMC)-binding protein from MMC-producing microorganisms protects from the lethal effect of bleomycin: crystallographic analysis to elucidate the binding mode of the antibiotic to the protein". J Mol Biol. 360 (2): 398–408. doi:10.1016/j.jmb.2006.05.017. PMID 16756991.
- ^ Mao Y.; Varoglu M.; Sherman D.H. (april 1999). "Molecular characterization and analysis of the biosynthetic gene cluster for the antitumor antibiotic mitomycin C from Streptomyces Iavendulae NRRL 2564". Chemistry and Biology. 6 (4): 251–263. doi:10.1016/S1074-5521(99)80040-4. PMID 10099135.
- ^ Charpentier X, Kay E, Schneider D, Shuman HA (mart 2011). "Antibiotics and UV radiation induce competence for natural transformation in Legionella pneumophila". J. Bacteriol. 193 (5): 1114–21. doi:10.1128/JB.01146-10. PMC 3067580. PMID 21169481.
- ^ Schewe MJ, Suzuki DT, Erasmus U (juli 1971). "The genetic effects of mitomycin C in Drosophila melanogaster. II. Induced meiotic recombination". Mutat. Res. 12 (3): 269–79. doi:10.1016/0027-5107(71)90015-7. PMID 5563942.
- ^ Bleuyard JY, Gallego ME, Savigny F, White CI (februar 2005). "Differing requirements for the Arabidopsis Rad51 paralogs in meiosis and DNA repair". Plant J. 41 (4): 533–45. doi:10.1111/j.1365-313X.2004.02318.x. PMID 15686518.
- ^ Rockford Coscia: Šablon:Webarchiv Columbia University Chemistry, (PDF).
- ^ Feng, Jie; Shi, Wanliang; Zhang, Shuo; Zhang, Ying (3. 6. 2015). "Identification of new compounds with high activity against stationary phase Borrelia burgdorferi from the NCI compound collection". Emerging Microbes & Infections. 4 (5): e31. doi:10.1038/emi.2015.31. PMC 5176177. PMID 26954881.
- ^ Sharma, Bijaya; Brown, Autumn V.; Matluck, Nicole E.; Hu, Linden T.; Lewis, Kim (26. 5. 2015). "Borrelia burgdorferi, the Causative Agent of Lyme Disease, Forms Drug-Tolerant Persister Cells". Antimicrobial Agents and Chemotherapy. 59 (8): AAC.00864–15. doi:10.1128/AAC.00864-15. PMC 4505243. PMID 26014929.
- ^ "Mitomycin". Drugs.com. 2017. Pristupljeno 11. 11. 2017.
- ^ Rustagi, T; Aslanian, H. R; Laine, L (2015). "Treatment of Refractory Gastrointestinal Strictures with Mitomycin C: A Systematic Review". Journal of Clinical Gastroenterology. 49 (10): 837–47. doi:10.1097/MCG.0000000000000295. PMID 25626632. S2CID 5867992.
- ^ Cabourne, E; Clarke, J. C; Schlottmann, P. G; Evans, J. R (2015). "Mitomycin C versus 5-fluorouracil for wound healing in glaucoma surgery" (PDF). The Cochrane Database of Systematic Reviews (11): CD006259. doi:10.1002/14651858.CD006259.pub2. PMID 26545176.
- ^ Majmudar, Parag A; Forstot, S.Lance; Dennis, Richard F; Nirankari, Verinder S; Damiano, Richard E; Brenart, Robert; Epstein, Randy J (januar 2000). "Topical Mitomycin-C for subepithelial fibrosis after refractive corneal surgery". Ophthalmology. 107 (1): 89–94. doi:10.1016/s0161-6420(99)00019-6. ISSN 0161-6420. PMID 10647725.
- ^ Cheng, S. M; Feng, Y. F; Xu, L; Li, Y; Huang, J. H (2013). "Efficacy of Mitomycin C in Endoscopic Dacryocystorhinostomy: A Systematic Review and Meta-Analysis". PLOS ONE. 8 (5): e62737. Bibcode:2013PLoSO...862737C. doi:10.1371/journal.pone.0062737. PMC 3652813. PMID 23675423.