Energetski nivo
Energijski nivoi su bliske diskretne razine energije u nekom izoliranom sistemu (atoma, molekula) ili u nekome sistemu čestica. U fizici čvrstoga stanja (Fermijev plinski model slobodnih elektrona, teorija elektronskih vrpci u kristalima), gustoća atoma i gustoća energijskih razina golema je, oko 1026 atoma/kg ili oko 1028 atoma/m³. Kada se atomi počinju približavati i stvarati kristalnu rešetku, energijske razine pojedinačnih atoma cijepaju se i spajaju u vrpce ili pojaseve dopuštenih energija. Nivoi energije u metalu ili poluvodiču,opisani su glavnim kvantnim brojem n i dvjema orijentacijama spina ("spin-gore" i "spin-dolje"), pri čemu je svaka orijentacija zasebno stanje zbog Paulijevog pravila. Prema tome, N elektrona u metalu (N je paran) rasporedit će se na:
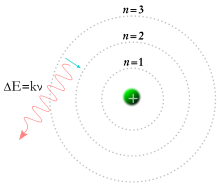

Nakon apsorpcije energije, elektron može "skočiti" iz osnovnog stanja u pobuđeije energentsko stanje.
energijskih nivoa, jer će u svakom od njih biti po dva elektrona. Dakle, broj stanja (elektrona) N dvostruko je veći od broja razina n:
Čestice se u sistemu naseljavaju (razmještaju) po razinama kao razlučive klasičoma Maxwell-Boltzmannovom statistikom ili kao nerazlučive čestice u skladu s pravilima kvantnih statistika: Fermi-Diracovoj i Bose-Einsteinovoj.
Kvantna mehanika – Osnovni pojmovi
urediKvantnomehanički sistem ili čestica koji je vezan – odnosno prostorno ograničen – može poprimiti samo određene diskretne vrijednosti energije, zvane nivoi energije. To je u suprotnosti sa klasičnim česticama, koje mogu imati bilo koju količinu energije. Izraz se obično koristi za nivoe energije elektrona u atomima, ionima ili molekulama, koji su povezani električnim poljem jezgra, ali se također može odnositi na energetske nivoe jezgara ili vibracijske ili rotacijske nivoe energije u molekulama. Kaže se da je energetski spektar sistema s takvim diskretnim nivoima energije kvantiziran. (Nivoi energije ne moraju biti jednaki)
U hemiji i atomskoj fizici, elektronska ljuska ili glavni nivo energije mogu se smatrati orbitom jednog ili više elektrona oko atomskog jezgra. Jezgru najbliža ljuska naziva se 1. ljuska (ili K-ljuska), nakon čega slijedi 2. ljuska (ili L-ljuska), a zatim 3. ljuska (ili M-ljuska), i tako dalje i dalje od jezgra. Ljuske odgovaraju glavnim kvantnim brojevima (n = 1, 2, 3, 4 ...) ili su abecedno označene slovima koja se koriste u rendgenskom zapisu (K, L, M, N…).
Svaka ljuska može sadržavati samo fiksni broj elektrona: prva ljuska do dva elektrona, druga ljuska može ih sadržavati do osam (2 + 6) elektrona, treća ljuska može imati do 18 (2 + 6 + 10 ) i tako dalje. Općenita formula je da n-ta ljuska može u principu imati do 2 (n2) elektrona (n2).[1] Budući da se elektroni električno privlače u jezgro, elektroni atoma će uglavnom zauzimati vanjske ljuske, samo ako je više unutrašnjih ljuski već u potpunosti popunili drugi elektroni. Međutim, ovo nije strog zahtjev: atomi mogu imati dvije ili čak tri nepotpune vanjske ljuske. (Pogledajte Madelungovo pravilo za više detalja.) Za objašnjenje zašto elektroni postoje u ovim ljuskama pogledajte konfiguracija elektrona.[2]
Ako je potencijalna energija postavljena na nulu na beskonačnu udaljenost od atomskog jezgra ili molekule, prema uobičajenoj konvenciji, tada vezana elektronska stanja imaju negativnu potencijalnu energiju.
Ako je atom, ion ili molekula na najnižem mogućem nivou energije, kaže se da su on i njegovi elektroni u osnovnom stanju. Ako je na višem energetskom nivou, kaže se da je pobuđeno, ili su svi elektroni koji imaju veću energiju od osnovnog stanja pobuđeni. Ako je više kvantno mehaničkih stanja u istoj energiji, nivoi energije su degenerirani. Tada se nazivaju degenerirani nivoi energije.
Objašnjenje
urediKvantizirani nivoi energije proizlaze iz odnosa između energije čestice i njene talasne dužine. Za ograničenu česticu poput elektrona u atoma, talasna funkcija ima oblik stojnii talas.[3] Mogu postojati samo stacionarna stanja s energijama koje odgovaraju integralnom broju talasnih dužina; za ostala stanja talasi se razaraju, rezultirajući nultom gustinom vjerovatnoće. Osnovni primjeri koji matematički pokazuju kako dolazi do nivoa energije su čestica u kutiji i kvantni harmonijski oscilator.
Hstorija
urediPrvi dokaz kvantizacije u atomima bilo je posmatranje spektarskih linija u sunčevoj svjetlosti, početkom 1800-ih, što su pokušali Joseph von Fraunhofer i William Hyde Wollaston. Pojam nivoa energije predložio je danski fizičar Niels Bohr, 1913., u Bohrovoj teoriji atoma. Modernu kvantno-mehaničku teoriju koja daje objašnjenje ovih energetskih nivoa u smislu Schrödingerove jednadžbe unaprijedili su Erwin Schrödinger i Werner Heisenberg 1926.
Atomi
urediSopstveni nivoi energije
urediU formulama za energiju elektrona na različitim nivoima datim u atomu ispod, nulta tačka za energiju se postavlja kada je dotični elektron u potpunosti napustio atom, tj. kada je elektronov glavni kvantni broj n = ∞. Kada je elektron vezan za atom u bilo kojoj bližoj vrijednosti n, energija elektrona je niža i smatra se negativnom.
Nivo energije u orbitalnom stanju: atom / ion sa jezgrom + jedan elektron
urediPretpostavimo da postoji jedan elektron u datoj atomskoj orbitali u vodikovom atomu (ionu). Energija njegovog stanja uglavnom se određuje elektrostatskom interakcijom (negativnog) elektrona sa (pozitivnom) jezgrom. Razine energije elektrona oko jezgra daju se kao:
(tipski, između 1 eV i 103 eV), gdje R∞ = Rydbergova konstanta, Z = atomski broj, n = glavni kvantni broj, h = Planckova konstanta, a c = brzina svjetlosti. Samo za atome (ione) slične vodiku, Rydbergovi nivoi ovise samo o glavnom kvantnom broju n.
Ova jednadžba dobija se kombiniranjem Rydbergove formule za bilo koji element sličan vodiku (prikazano dolje) sa E = h ν = h c / λ pod pretpostavkom da je glavni kvantni broj n gore = n1 u Rydbergovoj formuli i n2 = ∞) (glavni kvantni broj nivoa energije s kojeg elektron silazi, kada emitira foton). Rydbergova formula izvedena je iz empirijskih spektroskopske emisije podataka.
Ekvivalentna formula može se izvesti kvantnomehanički, iz vremenski neovisne Schrödingerove jednadžbe sa kinetičkom energijom Hamiltonovog operatora, koristeći talasnu funkciju kao sopstvenu funkciju za dobi,anje nivoa energije lastite vrijednosti, ali Rydbergova konstanta bi bila zamijenjena drugim temeljnim konstantama fizike.
Fino razdvajanje strukture
urediFina struktura proizlazi iz relativističkih korekcija kinetičke energije, sprega spin-orbita (elektrodinamička interakcija između elektrona spina i kretanja i električnog polja jezgra) i Darwinovog pojma (interakcija termina kontakta s ljuske elektrona unutar jezgra). Oni utiču na nivoe tipskim redom veličine 10−3 eV.
Hiperfina struktura
urediOva, još finija struktura je posljedica spin-spin interakcija elektronskog jezgra, što će rezultirati tipskom promjenom nivoa energije za tipski red veličine od 10 −4 eV.
Nivoi energije uslijed vanjskih polja
urediZeemanov efekt
urediPostoji energija interakcije povezana sa magnetnim dipolnim momentom, μL, koja proizlazi iz elektronskog orbitalnog ugaonog momenta, L, dati po:
sa
- .
Pored toga, uzima se u obzir magnetni moment koji proizlazi iz spina elektrona.
Zbog relativističkih efekata (Diracove jednadžbe), postoji magnetni moment , μS, koji proizilazi iz elekstronskog spina:
- ,
with gS elektrospinski g-faktor (oko 2), rezuiltirajući u ukupni magnetni moment, μ,
- .
Energija interakcije stoga postaje: .
Stark efekt
urediMolekule
urediHemijska veza između atoma je u obliku molekula jer oni čine situaciju stabilnijom za uključene atome, što obično znači da je zbir nivoa energije za uključene atome u molekuli niži nego da atomi nisu tako povezani. Kako se odvojeni atomi međusobno približavaju kovalentnom vezom, njihove orbitale međusobno utiču na energetske nivoe, da bi stvorile vezu i protuvezujuću molekulsku orbitalu. Nivo energije vezanja orbitala je niži, a nivo energije orbitale za vezanje je veći. Da bi veza u molekuli bila stabilna, kovalentno-vezujući elektroni zauzimaju nižu energetsku vezujuću orbitalu, što može biti označeno simbolima kao što su σ ili π, ovisno o situaciji. Odgovarajuće anti-vezujuće orbitale mogu se označiti dodavanjem zvjezdice da se dobiju σ* ili π* orbitale. Nevezujuća orbitala u molekuli je orbitala s elektronima u vanjskoj ljusci koji ne sudjeluju u vezanju i njihov energetski nivo je jednak onome koji ima sastavni atom. Takve orbitale možemo označiti kao n orbitale. Elektroni u n orbitali su obično usamljeni parovi.[4]
U polikatomskim molekulama uključeni su i različiti nivoi vibracija i rotacije.
Grubo rečeno, molekulsko energetsko stanje, tj. svojstveno stanje Hamiltonove molekule, zbir je elektronskih, vibracijskih, rotacijskih, nuklearnih i translacijskih komponenata, kao što su:
gdje Eelectronic = vlastita vrijednost elektronske hamiltonovske molekule jednost potencijalne energije površine) na ravnotežnoj geometriji molekule.
Nivoi molekulske energije označeni su kao molekulski izraz. Specifične energije ovih komponenata variraju, u zavisnosti od specifičnog energetskog stanja i supstance.
Dijagrami nivoa energije
urediPostoje različiti tipovi dijagrama nivoa energije za veze između atoma u molekuli. Primjeri
Tranzicijski nivoi energije
urediElektroni u atomima i molekulama mogu mijenjati (praviti prelazeu) nivoe, emitirajući ili upijajući foton (elektromagnetnog zračenja), čija energija mora biti tačno jednaka energetskoj razlici između dva nivoa.
Elektroni se također mogu potpuno ukloniti iz hemijskih vrsta, kao što su atom, molekula ili ion. Potpuno uklanjanje elektrona iz atoma može biti oblik ionizacije, koji efektivno premiješta elektron u orbitalu sa beskonačnim glavnim kvantnim brojem, u stvari tako daleko da praktično više nema efekta na preostali atom (ion). Za razne vrste atoma postoje 1., 2., 3. itd. energije jonizacije, za uklanjanje 1., zatim 2., pa 3., itd. elektrona najviše energije iz atoma, izvorno u osnovnom stanju. Također energija se može osloboditi u odgovarajućim suprotnim količinama, ponekad u obliku energije fotona, kada se elektroni dodaju pozitivno nabijenim ionima ili ponekad atomima. Molekule također mogu proći tranzicije u njihovom vibracijskim ili rotacijskim nivoima energije. Prijelazi energetskog nivoa također mogu biti neradijacijski, što znači da emisija ili apsorpcija fotona nisu uključeni.
Ako je atom, ion ili molekula na najnižem mogućem nivou energije, kaže se da su on i njegovi elektroni u osnovnom stanju. Ako je na višem energetskom nivou, kaže se da je pobuđeno, ili su svi elektroni koji imaju veću energiju od osnovnog stanja pobuđeni. Takva vrsta može se pobuditi na viši nivo energije, pomoću apsorpcije fotona čija je energija jednaka energetskoj razlici između nivoa. Suprotno tome, pobuđena vrsta može preći na niži nivo energije spontanim emitiranjem fotona jednakog energetskoj razlici. Energija fotona jednaka je Planckovoj konstanti (h) puta njegove frekvencija ( f) i stoga je proporcionalna njegovoj frekvenciji, ili obrnuto od njegove talasne dužine (λ):
- ΔE = h f = h c / λ,
budući da je c, brzina svjetlosti jednaka f λ.
Shodno tome, mnogi tipovi spektroskopije temelje se na otkrivanju frekvencije ili talasne dužine emitovanih ili apsorbovanih fotona, kako bi pružile informacije o analiziranom materijalu, uključujući informacije o nivoima energije i elektronskoj strukturi materijala, dobijene analizom spektra.
Za dizajniranje pobuđenog stanja, obično se koristi zvezdica. Prijelaz elektrona u vezi molekule iz osnovnog stanja u pobuđeno stanje može imati oznaku kao što je σ → 6nbsp;σ*, π* ili → π* što znači pobuđivanje elektrona iz a σnbsp; vezivanje za σnbsp; antibonding orbitalu, od πnbsp; vezivanje za πnbsp; orbitalu za vezivanje, ili od n nevezivanja za πnbsp; orbitalu za vezivanje.[4][5] Obrnuti prijelaz elektrona za sve ove vrste pobuđenih molekula također se može vratiti u osnovno stanje, koje se može označiti kao σ* → σ, π* → π ili π* → n.
Tranzicija u nivou energije elektrona u molekuli može se kombinirati sa vibracijskim prijelazom i nazvati vibronski prijelaz. Vibracijski i rotacijski prijelaz mogu se kombinirati pomoću rotacijskog spajanja. U rovibronic sprezanje, prijelazi elektrona se istovremeno kombiniraju i sa vibracijskim i rotacijskim prijelazima. Fotoni koji učestvuju u prelazima mogu imati energiju različitih raspona u elektromagnetnom spektru, kao što su rendgen, ultraljubičasto, vidljivo svetlo, infracrveno ili mikrotalasna zračenje, ovisno o vrsti prijelaza. Na vrlo općenit način, razlike u nivou energije između elektroničkih stanja su veće, razlike između nivoa vibracija su srednje, a razlike između nivoa rotacije su manje, iako se može preklapati. Translacijski nivoi energije su praktično kontinuirani i mogu se izračunati kao kinetička energija korištenjem klasična mehanika.
Viša temperatura dovodi do bržeg kretanja atoma i molekula fluida povećavajući njihovu translacijsku energiju i termički pobuđuje molekule do viših prosječnih amplituda vibracijskog i rotacijskog načina (pobuđuje molekule do viših internih nivoa energije). To znači da s porastom temperature translacijski, vibracijski i rotacijski doprinosi molekularnom toplotnom kapacitetu dopuštaju molekulima da apsorbiraju toplinu i zadržavaju više unutarnje energije. Kondukcija toplote obično se javlja dok se molekuli ili atomi sudaraju prenos toplote međusobno. Na čak i višim temperaturama, elektroni se mogu termički pobuditi na više energetske orbitale u atomima ili molekulima. Kasniji pad elektrona na niži nivo energije može osloboditi foton, uzrokujući moguće obojeni sjaj.
Elektron dalje od jezgre ima veću potencijalnu energiju od elektrona bliže jezgri, pa postaje manje vezan za jezgru, budući da je njegova potencijalna energija negativna i obrnuto ovisi o udaljenosti od jezgra. Obrnuti prijelazi elektrona za sve ove vrste pobuđenih molekula također se mogu vratiti u osnovno stanje, što se može označiti kao σ* → σ, π* → π, or π* → n. Tranzicija u nivou energije elektrona u molekuli može se kombinirati s vibracijskim prijelazom i nazvati vibronska tranzicija. Vibracijska i rotacijska tranzicija mogu se kombinirati pomoću rotacijskog spajanja. U rovinbronskoj sprezi, tranzicija elektrona kombinira se istovremeno i sa vibracijskomm i rotacijskom tranzicijom. Fotoni koji učestvuju u tranzicijama mogu imati energiju različitih raspona u elektromagnetnom spektru, kao što su rendgen, ultraljubičasto, vidljivo svjetlo, infracrveno ili mikrotalasn zračenje, ovisno o tipu tranzicije. Veoma općenito, razlike u nivou energije između elektronskih stanja su veće, razlike između nivoa vibracija su srednje, a razlike između nivoa rotacije su manje, iako se mogu preklapati. Translacijski nivoi energije su praktično kontinuirani i mogu se izračunati kao kinetička energija korištenjem formula klasične mehanike.
Viša temperatura dovodi do bržeg kretanja atoma i molekula fluida, povećavajući svoju translacijsku energiju i termički pobuđuje molekule na veće prosječne amplitude vibracijskog i rotacijskog načina (pobuđuje molekule na viši nivo unutrašnje energije). To znači da s porastom temperature translacijski, vibracijski i rotacijski doprinosi molekulskom toplotnom kapacitetu dopuštaju molekulama da apsorbiraju toplotu i zadržavaju više unutrašnje energije. Kondukcija toplote obično se javlja dok se molekule ili atomi sudaraju, prenoseći toplotu međusobno. Čak i na višim temperaturama, elektroni se mogu termički pobuditi na više energetske orbitale u atomima ili molekulama. Kasniji pad elektrona na niži nivo energije može osloboditi foton, uzrokujući moguće obojeni sjaj.
Elektron dalje od jezgra ima veću potencijalnu energiju od elektrona bliže jezgru, pa postaje manje vezan za njega, budući da je njegova potencijalna energija negativna i obrnuto ovisi o udaljenosti od jezgra.[6]
Kristalni materijali
urediUtvrđeno je da kristalni čvrsti materijal ima energetske opsege, umjesto ili pored energetskih nivoa. Elektroni mogu preuzeti bilo koju energiju unutar nepopunjenog pojasa. U početku se čini da je ovo izuzetak od zahtjeva za nivoe energije. Međutim, kao što je prikazano u teoriji volumena, energetski pojasevi zapravo se sastoje od mnogih diskretnih energetskih nivoa, koji su preblizu da bi se razriješili. Unutar opsega, broj nivoa je reda broja atoma u kristalu, pa, iako su elektroni zapravo ograničeni na te energije, mogu poprimiti kontinuum vrijednosti. Važni nivoi energije u kristalu su pik valencijskog opsega, dno provodnog opsega, Fermijev nivo, nivo vakuuma i nivoi energije bilo kojeg defektnog stanja u kristalu.
Također pogledajte
urediReference
uredi- ^ Re: Why do electron shells have set limits ? madsci.org, 17 March 1999, Dan Berger, Faculty Chemistry/Science, Bluffton College
- ^ Electron Subshells. Corrosion Source. Retrieved on 1 December 2011.
- ^ Tipler, Paul A.; Mosca, Gene (2004). Physics for Scientists and Engineers, 5th Ed. 2. W. H. Freeman and Co. str. 1129. ISBN 0716708108.
- ^ Vrati se na: a b UV-Visible Absorption Spectra
- ^ Theory of Ultraviolet-Visible (UV-Vis) Spectroscopy
- ^ "Archived copy". Arhivirano s originala, 18. 7. 2010. Pristupljeno 7. 10. 2010.CS1 održavanje: arhivirana kopija u naslovu (link)

