Morska voda
Šablon:Salinitet Morska voda ili slana vodamje voda iz mora ili okeana. U prosjeku, morska voda u svjetskim okeanima ima salinitet od oko 3,5% (35 g/L, 599 mM). To znači da svaki kilogram (otprilike jedan litar zapremine) morske vode ima oko 35 grams (1.2 oz) rastvorene soli (pretežno ioni natrij (Na+) i hlor (Cl–). Prosječna gustina na površini je 1,025 kg/L. Morska voda je gušća i od slatke vode i od čiste vode (gustoća 1,0 kg/L, na 4oC , jer rastvorene soli povećavaju masu za veći udio zapremine. Tačka ledišta morske vode smanjuje se kako se povećava koncentracija soli. Pri tipsknom salinitetu, smrzava se na približno –2oC.[1] Najhladnija morska voda koja je ikad zabilježena u tečnom stanju pronađena je 2010. u potoku ispod antarktičkog ledenjaka: izmjerena temperatura bila je –2,6 oC.


Kiselost (pH) morske vode obično je ograničena na raspon između 7,5 i 8,4.[2] Međutim, ne postoji univerzalno prihvaćena referentna pH-skala za morsku vodu i razlika između mjerenja na osnovu različitih referentnih ljestvica može biti i do 0,14 jedinica.[3]
Geohemija
urediSlanost (salinitet)
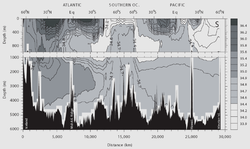
urediIako velika većina morske vode ima salinitet između 31 g/kg i 38 g/kg, odnosno 3,1–3,8%, nije ravnomjerno slana u cijelom svijetu. Tamo gdje se događa miješanje sa otjecanjem slatke vode iz ušća rijeka, u blizini topljenja ledenjaka ili velike količine padavina (npr. monsuni), morska voda može biti znatno slanija. Najslanije otvoreno more je Crveno more, gdje visoke stope isparavanja, niske padavine i malo oticanje rijeke, te ograničena cirkulacija, rezultiraju neobično slanom vodom . Slanost u izoliranim vodenim tijelima može biti znatno veća – oko deset puta veća u slučaju Mrtvog mora. Povijesno gledano, za približavanje apsolutne slanosti morske vode korišteno je nekoliko skala. Popularna bila je "Praktična skala saliniteta", gdje se slanost mjerila u "praktičnim jedinicama saliniteta (psu)". Sadašnji standard za slanost je skala zvana "Referentni salinitet",[5] sa salinitetom izraženim u jedinicama g/kg.
Termofizička svojstva
urediGustoća površinske morske vode kreće se od oko 1.020 do 1.029 kg/m3, ovisno o temperaturi i slanosti. Na temperaturi od 25 °C, slanosti od 35 g/kg i pritisku od 1 atm, gustoća morske vode je 1023,6 kg/m3.[6][7] Duboko u okeanu, pod visokim pritiskom, morska voda može doseći gustoću od 1.050 kg/m3 ili više. Gustoća morske vode također se mijenja sa slanošću. Slane vode koje generiraju postrojenja za desalinizaciju, mogu imati slanost do 120 g/kg. Gustoća tipske salamure morske vode od 120 g/kg slanosti pri 25 °C i normalnom atmosferskom pritisku iznosi 1.088 kg/m3[6][7] Za morsku vodu, pH ograničen je na raspon od 7,5 do 8,4. Brzina zvuka u morskoj vodi je oko 1.500 m/s (dok je brzina zvuka u zraku obično oko 330 m/s, pri pritisku od oko 101,3 kPa (1 atmosfera) i varira s temperaturom vode i slanošću. Toplotna provodljivost morske vode iznosi 0,6 W/mK na 25 °C i salinitetu od 35 g /kg.[8] Toplotna provodljivost opada sa povećanjem slanosti i povećava se s porastom temperature.[9]
Hemijski sastav
urediMorska voda sadrži više rastvorenih iona nego svi bilo koji tip slatke.[10] Međutim, odnosi otopljenih supstanci dramatično se razlikuju. Naprimjer, iako morska voda sadrži oko 2,8 puta više bikarbonata od riječne vode, u njoj je postotak bikarbonata kao omjer „svih“ otopljenih iona daleko niži nego u riječnim vodama. Ioni bikarbonata čine 48% rastvorenih sastojaka riječne vode, ali samo 0,14% morske.[10][11] Razlike poput ovih nastaju zbog različitih vremena zadržavanja otopljenih sastojaka morske vode; natrij i hlorid imaju vrlo dugo vrijeme zadržavanja, dok kalcij (vitalni za formiranje karbonata) ima tendenciju da se mnogo brže taloži.[11] Najzastupljeniji otopljeni ioni u morskoj vodi su natrij, hlor, magnezij, sulfati i kalcij.[12] Njegova osmolarnost je oko 1000 mOsm/L.[13]
Pronađene su male količine drugih supstanci, uključujući aminokiseline, u koncentracijama do dva mikrograma atoma dušika po litru,[14] za koje se smatra da su imale ključnu ulogu u porijeklu života.
| Element | Postotak po masi |
|---|---|
| Kisik | 85,84 |
| Vodik | 10,82 |
| Hlor | 1,94 |
| Natrij | 1,08 |
| Magnezij | 0,1292 |
| Sumpor | 0,091 |
| Kalcij | 0,04 |
| Kalij | 0,04 |
| Brom | 0,0067 |
| Ugljik | 0,0028 |
| Komponenta | Koncentracija (mol/kg) |
|---|---|
| H2O | 53,6 |
| Cl– | 0,546 |
| Na+ | 0,469 |
| Mg2+ | 0,0528 |
| SO2–4 | 0,0282 |
| Ca2+ | 0,0103 |
| K+ | 0,0102 |
| CT (ukupni neorganski ugljik) | 0,0206 |
| Br– | 0,000844 |
| BT (ukupni bor) | 0,000416 |
| Sr2+) | 0,000091 |
| F– | 0,000068 |
Također pogledajte
urediReference
uredi- ^ "U.S. Office of Naval Research Ocean, Water: Temperature". Arhivirano s originala, 12. 12. 2007.
- ^ Chester, Jickells, Roy, Tim (2012). Marine Geochemistry. Blackwell Publishing. ISBN 978-1-118-34907-6.
- ^ Stumm, W, Morgan, J. J. (1981) Aquatic Chemistry, An Introduction Emphasizing Chemical Equilibria in Natural Waters. John Wiley & Sons. pp. 414–416. ISBN 0471048313.
- ^ "World Ocean Atlas 2009". NOAA. Pristupljeno 5. 12. 2012.
- ^ Millero, Frank J.; Feistel, Rainer; Wright, Daniel G.; McDougall, Trevor J. (januar 2008). "The composition of Standard Seawater and the definition of the Reference-Composition Salinity Scale". Deep Sea Research Part I: Oceanographic Research Papers. 55 (1): 50–72. doi:10.1016/j.dsr.2007.10.001.
- ^ a b Nayar, Kishor G.; Sharqawy, Mostafa H.; Banchik, Leonardo D.; Lienhard V, John H. (juli 2016). "Thermophysical properties of seawater: A review and new correlations that include pressure dependence". Desalination. 390: 1–24. doi:10.1016/j.desal.2016.02.024.
- ^ a b "Thermophysical properties of seawater" (jezik: engleski). Department of Mechanical Engineering, Massachusetts Institute of Technology. Pristupljeno 24. 2. 2017.
- ^ Sharqawy, Mostafa H.; Lienhard V, John H.; Zubair, Syed M. (april 2010). "The thermophysical properties of seawater: A review of existing correlations and data" (PDF). Desalination and Water Treatment. 16: 354–380. doi:10.5004/dwt.2010.1 (neaktivno 14. 1. 2021).CS1 održavanje: DOI nije aktivan od 2021 (link)
- ^ "Thermal conductivity of seawater and its concentrates". Pristupljeno 17. 10. 2010.
- ^ a b Gale, Thomson. "Ocean Chemical Processes". Pristupljeno 2. 12. 2006.
- ^ a b Pinet, Paul R. (1996). Invitation to Oceanography. St. Paul: West Publishing Company. str. 126, 134–135. ISBN 978-0-314-06339-7.
- ^ Hogan, C. Michael (2010). "Calcium", eds. A. Jorgensen, C. Cleveland. Encyclopedia of Earth. National Council for Science and the Environment.
- ^ "Osmolarity of sea water".
- ^ Tada, K.; Tada, M.; Maita, Y. (1998). "Dissolved free amino acids in coastal seawater using a modified fluorometric method" (PDF). Journal of Oceanography. 54 (4): 313–321. doi:10.1007/BF02742615. Arhivirano s originala (PDF), 21. 1. 2021. Pristupljeno 15. 1. 2021.
- ^ DOE (1994). "5" (PDF). u A. G. Dickson; C. Goyet (ured.). Handbook of methods for the analysis of the various parameters of the carbon dioxide system in sea water. 2. ORNL/CDIAC-74. Arhivirano s originala (PDF), 25. 5. 2011. Pristupljeno 15. 1. 2021.
Vanjski linkovi
urediTables
- Tables and software for thermophysical properties of seawater, MIT
- G. W. C Kaye, T. H. Laby (1995). "Physical properties of sea water". Tables of physical and chemical constants (16th izd.). Arhivirano s originala, 8. 5. 2019.