SRY
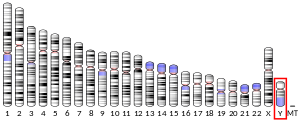
Testis-determinirajući faktor(TDF), odnosno faktor određivanja testisa, znan i i kao regija Y koja određuje spol (SRY) je protein koji veže DNK (poznat i kao genski regulatorni protein / faktor transkripcije) kodiran genom SRY, koji je odgovoran za iniciranje muškog spola određivanje spola u terijskih sisara (placentni sisari i torbari).[5] SRY je bezintronski spolno određujući gen koji na Y-hromosomu.[6] Mutacije u ovom genu dovode do niza poremećaja razvoja spola (DSD) sa različitim efektima na fenotip i genotip jedinke.
TDF je član porodice SOX (gena sličnih kutiji SRY) porodice proteina koji vežu DNK. Kada se kompleksira sa proteinom SF1, TDF djeluje kao faktor transkripcije koji izaziva pojačanu regulaciju ostalih faktora transkripcije, što je najvažnije SOX9-a. Njegov ekspresija uzrokuje razvoj primarnih spolnih vrpci, koji se kasnije razvijaju u seminiferne tubule. Ove vrpce formiraju se u centralnom m dijelu još nediferencirane gonade, pretvarajući je u testis. Sada inducirane Leydigove ćelije testisi počinju lučiti testosteron, dok Sertolijeve proizvode antiMüllerovski hormon.[7] Efekti SRY gena obično se javljaju 6-8 sedmica nakon formiranja fetusa i inhibira rast feminiziranih anatomskih struktura kod muškaraca. Također djeluja na razvijanju dominantnih muških karakteristika.
Razvoj i regulacija gena
urediEvolucija
urediSRY može nastati duplikacijom gena za X hromosom vezanog SOX3 , člana porodice Sox.[8][9] Do ove duplikacije došlo je nakon podjele između monotremmata i Theria. Monotrematima nedostaje SRY, a neki od njihovih spolnih hromosoma imaju homologiju sa spolnim hromosomima ptica.[10] SRY je gen koji se brzo razvija, a njegovu regulaciju je bilo teško proučiti, jer određivanje spola nije visoko konzervirana pojava u životinjskom carstvu.[11] Razlikuje se među vrstama, čak i unutar Marsupialia i Placentalia, koja imaju SRY u svom procesu određivanja spola, djelovanjem SRY . Genska sekvenca se također mijenja; dok je jezgro gena, grupa visoke pokretljivosti (HMG), konzerviran među vrstama, druge regije gena nisu. SRY je samo jedan od četiri gena na ljufdskom Y hromoomu za koja se pokazalo da su nastali iz originalnog Y hromosoma.[12] Ostali geni na ljudskom romosomu Y nastali su iz autosoma koji je spojen sa originalnim Y-onom.[12]
Regulacija
urediGen SRY ima malo zajedničkog sa genima za određivanje spola drugih modelnih organizama, zbog čega su miševi glavni model istraživanja organizama koji se mogu koristiti za njegovo proučavanje. Razumijevanje njegove regulacije je dodatno komplicirano jer čak i među vrstama sisara postoji malo konterviranih proteinskih sekvenci. Jedina konzervirana grupa između miševa i drugih sisara je grupa visoke pokretljivosti (HMG) regije koja je odgovorna za vezivanje DNK. Mutacije u ovoj regiji rezultiraju reverzijom spola, gdje u nekoj fazi jedinka mijenja dotadašnji, u suprotni spol.[13] Budući da ima malo konzerviranih sekvenci, promotor SRY, regulatorni elementi i regulacija nisu dobro shvaćeni. Unutar srodnih grupa sisara postoje homologije u prvih 400-600 parova baza uzvodno od početnog mjesta translacije. In vitro studije promotora ljudskog SRY pokazale su da je za funkciju promotora potrebna regija od najmanje 310 bp uzvodno do početnog translacijskog mesta. Dokazano je da naa ekspresiju ljudskog promotora SRY , utiču vezanje tri transkripcijska faktora, steroidogeni faktor 1 (SF1), specifični protein 1 (transkripcijski faktor Sp1) i Wilmsov tumorski protein 1 (WT1).
Regija promotora ima dva Sp1 vezna mjesta, na –150 i –13 koja funkcioniraju kao regulatorna mjesta. Sp1 je faktor transkripcije koji veže konsenzusne sekvence bogate GC-om, a mutacija mesta vezanja SRY dovodi do smanjenja transkripcije gena za 90%. Studije SF1 rezultirale su manje određenim rezultatima. Mutacije SF1 mogu dovesti do inverzije spola, a delecija do nepotpunog razvoja spolnih žlijezda. Međutim, nije jasno kako SF1 direktno komunicira s promotorom SR1.[14] Promotorska regija također ima dva WT1 mjesta vezanja na –78 i –87 bp kodona ATG. WT1 je transkripcijski faktor koji ima četiri C-kraja cinkovog prsta i regiju N-kraja bogatu Pro/Glu-om i primarno funkcionira kao aktivator. Mutacija cinkovog prsta ili inaktivacija WT1 rezultira smanjenom veličinom muške spolne žlijezde. Delecija gena rezultira potpunom inverzijom (preokretom) spola. Nije jasno kako WT1 funkcionira u regulaciji SRY , ali neka istraživanja sugeriraju da to pomaže u stabilizaciji obrade poruka. Međutim, postoje hipoteze u vezi s ovom, jer je WT1 također odgovoran za ekspresiju antagonista muškog razvoja, DAX1, što znači preokret spola osetljiv na dozu, kritična regija nadbubrežne hipoplazije, na hromozomu X, gen 1. Dodatna kopija DAX1 kod miševa dovodi do reverzije spola. Nije jasno kako DAX1 funkcionira, a predloženo je mnogo različitih puteva, uključujući destabilizaciju transkripcije SRY i vezanje RNK. Postoje dokazi iz rada na suzbijanju muškog razvoja da DAX1 može ometati funkciju SF1, a zauzvrat transkripciju SRY, aktiviranjem korepresora.
Također postoje dokazi da protein GATA, koji veže 4 (GATA4) i FOG2 doprinose aktivaciji SRY, povezivanjem sa njegovim promotorom. Nije jasno kako ovi proteini reguliraju transkripciju SRY , ali FOG2 i GATA4 mutanti imaju značajno niže nivoe SRY transkripcije.[15] FOG-ovi imaju motive na cinkovim prstima koji mogu vezati DNK, ali nema dokaza o interakciji FOG2 sa SRY. Studije sugeriraju da se FOG2 i GATA4 povezuju s proteinima koji prepravljaju nukleosome, što bi moglo dovesti do njihove aktivacije.[16]
Funkcija
urediTokom gestacije, ćelije primordijalne spolne žlijezde koje leže duž urogenitalnog grebena nalaze se u bipotencijalnom stanju, što znači da imaju sposobnost da postanu ili muške ćelije (Sertolijeve i Leydigove ćelije) ili ženske ćelije (folikulske i tekine ćelije). TDF pokreće diferencijaciju testisa, aktivirajući muške specifične faktore transkripcije koji omogućavaju ovim bipotencijalnim ćelijama da se diferenciraju i razmnožavaju. TDF to postiže nadgulacijom SOX9-a, transkripcijskog faktora sa mjestom vezanja DNK vrlo sličnom TDF-ovima. SOX9 dovodi do regulacije faktora rasta fibroblasta 9 (Fgf9), što zauzvrat dovodi do daljnje regulacije SOX9. Kada se dostignu odgovarajući nivoi SOX9, bipotencijalne ćelije spolne žlijezde počinju se diferencirati u Sertolijeve ćelije. Pored toga, ćelije koje eksprimiraju TDF nastavit će se razmnožavati, formirajući primordijalni testis. Iako to predstavlja osnovni niz događaja, ovaj kratki osvrt treba uzeti s oprezom jer postoji mnogo više faktora koji utiču na spolnu diferencijaciju.
Djelovanje u jedru
urediTDF protein sastoji se od tri glavne regije. Centralna regija obuhvata domen HMG (grupa visoke pokretljivosti), koji sadrži nuklearna sekvenca lokalizacije i djeluje kao domen koji veže DNK. Domen C-kraja nema konzerviranu strukturu, a domen N-kraja može se fosforilirati, kako bi se poboljšalo vezanje DNK. Proces započinje sa jedarnom lokalizacijom TDF-a, acetilacijom signalnih područja jdrne lokalizacije, što omogućava vezanje importina β i kalmodulina za TDF, olakšavajući njegov unos u ,edro. Kada se nađu u jedru, TDF i SF1 (steroidogeni faktor 1, drugi regulator transkripcije) slože se i vežu za TESCO (pojačivač jedra Sox9 specifičnog za testise), element testis-specifičnog pojačivača gena Sox9 u prekursorima Sertolijevih ćelija, uzvodno od početnog mjesta transkripcije gena.[17] Konkretno, to je HMG regija TDF -a, koja se veže za manji žlijeb ciljane sekvence DNK, što dovodi do savijanja i odmotavanja DNK. Uspostavljanje ove posebne DNK "arhitekture" olakšava transkripciju gena Sox9. U jedrima Sertolijevih ćelija, SOX9 direktno cilja gen Amh, kao i gen za prostaglandin D-sintazu (Ptgds). Vezanje SOX9 za pojačivač u blizini promotora Amh omogućava sintezu Amh-a, dok vezanje SOX9 za gen Ptgds omogućava proizvodnju prostaglandina D2 (PGD2). Ponovni ulazak SOX9 u jedro olakšava se autokrinom ili parakrinom signalizacijom koju provodi D2 (PGD2). Ponovni ulazak SOX9 u jedro olakšava se autokrinom ili parakrinom signalizacijom koju provodi PGD2.[18] SOX9 protein tada pokreće petlju pozitivne povratne informacije, koja uključuje SOX9, djelujući kao vlastiti faktor transkripcije i rezultirajući sintezom velikih količina SOX9.
SOX9 i diferencijacija testisa
urediSF1 protein sam po sebi dovodi do minimalne transkripcije gena SOX9 u XX i XY bipotencijalnim ćelijama gonada duž urogenitalnog grebena. Međutim, vezanje kompleksa TDF-SF1 za pojačivač specifičan za testise (TESCO) na SOX9 dovodi do značajne regulacije gena samo u XY gonadi, dok je transkripcija u XX gonadi i dalje zanemariva. Dio ove regulacije postiže sam SOX9 kroz petlju pozitivnih povratnih informacija; poput TDF-a, SOX9 kompleksira sa SF1 i veže se za pojačivač TESCO, što dovodi do daljeg ekspresije SOX9 u XY gonadi. Dva druga proteina, FGF9 (faktor rasta fibroblasta 9) i PDG2 (prostaglandin D2), također održavaju ovu regulaciju. Iako njihovi tačni putevi nisu u potpunosti razumljivi, pokazalo se da su neophodni za kontinuiranu ekspresiju SOX9 na nivoima neophodnim za razvoj testisa.
Smatra se da su SOX9 i TDF odgovorni za ćelijsko-autonomnu diferencijaciju potpornih ćelijskih prekursora u spolnim žlijezdama u Sertolijeve ćelije, što je početak razvoja testisa. Pretpostavlja se da su ove početne Sertolijeve ćelije u centru spolne žlijezde polazna tačka talasa FGF9 koji se širi kroz XY gonadu u razvoju, što dovodi do daljnje diferencijacije Sertolijevih ćelija, nadregulacijom SOX9.[19] Smatra se da su SOX9 i TDF odgovorni za mnoge kasnije procese razvoja testisa (poput diferencijacije Leydigovih ćelija, formiranja spolnihvrci i formiranja vaskulature specifične za testise), iako tačni mehanizmi ostaju nejasni.[20] Pokazano je, međutim, da SOX9, u prisustvu PDG2, djeluje direktno na Amh (kodirajući antimilerovski hormon) i sposoban je inducirati stvaranje testisa u XX. Urađeno je na spolnim žlijezdama miševa, ukazujući na njegov vitalni značaj za razvoj testisa.
Uticaj SRY poremećaja na ekspresiju spola
urediEmbrioni su gonadno identični, bez obzira na genetički spol, sve do određene faze razvoja kada faktor određivanja testisa uzrokuje razvoj muških spolnih organa. Tipski muški kariotip je XY, dok je ženski XX. Međutim, postoje izuzeci u kojima glavnu ulogu ima SRY+Y. Osobe sa Klinefelterovim sindromom nasljeđuju normalan Y hromosom i više X hromosoma, uz kariotip XXY. Smatraju se muškarcima.[21] Neuobičajena genetička rekombinacija tokom krosinovera, kada se razvija spermatozoid, može rezultirati kariotipovima koji se ne podudaraju sa njihovom fenotipskom ekspresijom.
Većinu vremena, kada se spermatozoid u razvoju podvrgne se krosing-overu tokom mejoze, gen SRY ostaje na Y hromosomu. Ako se SRY gen prenese u X hromosom, umjesto da ostane na Y-nu, neće početi razvoj testisa. Ovo je poznato kao Swyerov sindrom, karakteriziran XY kariotipom i ženskim fenotipom. Osobe sa ovim sindromom imaju normalno formirane maternice i jajovode, ali spolne žlijezde nisu funkcionalne. Uglavnom se odgajaju kao žene i imaju ženski rodni identitet.[22] Na drugoj strani spektra, XX muški sindrom javlja kada tijelo ima ženske hromosome, a SRY se za jedan od njih veže translokacijom. Osobe sa sindromom XX muškog fenotipa imaju ženski genotip, ali muške fizičke osobine.[23] Osobe s bilo kojim od ovih sindroma mogu imati usporeni pubertet, neplodnost i karakteristike rasta suprotnog spola s kojim se identificiraju. Oni sa XX muškim sindromom mogu razviti dojke, a sa Swyerovim sindromom mogu imati dlake na licu.[22][24]
| Klinefelterov indrom |
|
| Swyerov sindrom | * Osobe s ovim sindromom smatraju se muškarcima
|
| Muški sindrom XX |
|
Iako prisustvo ili odsustvo SRY općenito određuje da li se razvija testis ili ne, sugerira se da postoje i drugi faktori koji utiču na funkcionalnost gene SRY.[25] Prema tome, postoje osobe koje imaju gen SRY, ali se i dalje razvijaju kao žene, bilo zato što je sam gen neispravan ili mutiranili zato što je neispravan jedan od faktora koji tome doprinosi.[26] To se može dogoditi kod osoba koje imaju XY, XXY ili XX SRY pozitivan kariotip.
Pored toga, drugi sistemi za određivanje spola na bazi SRY/TDF osim XY, su procesi koji dolaze nakon što SRY bude prisutan ili odsutan u razvoju embriona. U normalnom sistemu, ako je SRY prisutan za XY, TDF će aktivirati moždinu da razvije spolne žlijezde u testise. Tada će se proizvesti testosteron i pokrenuti razvoj drugih muških spolnih obilježja. Uporedno s tim, ako SRY nije prisutan u paru XX, nedostajaće TDF zbog nedostatka Y hromosoma. Nedostatak TDF-a omogućit će da se korteks embrionskih spolnih žlijezda razvije u jajnike, koji će tada proizvoditi estrogen i dovesti do razvoja drugih ženskih spolnih karakteristika.[27]
Uloga u ostalim bolestima
urediDokazano je da SRY ima interakcije sa androgenim receptorom, a osobe sa XY kariotipom i funkcionalnim SRY genom mogu imati ženski vanjski fenotip zbog osnovnog sindroma neosjetljivosti na androgen (AIS).[28] Osobe s AIS-om nisu u stanju pravilno reagirati na androgene zbog oštećenja gena za androgeni receptor, a pogođene osobe mogu imati potpunu ili djelimičnu AIS.[29] SRY je također povezan s činjenicom da muškarci češće od žena razvijaju bolesti povezane sa dopaminom, kao što su shizofrenija i Parkinsonova bolest. SRY kodira protein koji kontrolira koncentraciju dopamina, neurotransmitera koji prenosi signale iz mozga koji kontroliraju kretanje i koordinaciju.[30] Istraživanje na miševima pokazalo je da je mutacija SOX10, SRY kodiranog transkripcijskog faktora, povezana sa stanjem dominantnog megakolona kod miševa.[31] > Ovaj model miša koristi se za istraživanje veze između SRY i Hirschsprungove bolesti ili urođenog megakolona kod ljudi. Također postoji veza između SRY kodiranog transkripcijskog faktora SOX9 i kampomelne displazije (CD).[32] Ova misense mutacija uzrokuje defektnu hondrogenezu ili proces formiranja hrskavice, a manifestira se kao skeletna CD.[33] Two thirds of 46,XY individuals diagnosed with CD have fluctuating amounts of male-to-female sex reversal.[32]
Upotreba u olimpijskim pregledima
urediJedna od najkontroverznijih upotreba ovog otkrića bila je kao sredstvo za verifikaciju rodnosti na Olimpijskim igrama, u okviru sistema koji je Međunarodni olimpijski komitet implementirao 1992. godine. Sportistima sa SRY genom nije bilo dozvoljeno da učestvuju kao žene, iako sportistima kod kojih je to "otkriven" na Ljetnim olimpijskim igrama 1996 presuđen lažno pozitivni nalaz, nisu diskvalificirani. Tačnije, utvrđeno je da osam učesnica (od ukupno 3387) u ovim igrama imaju gen SRY. Međutim, nakon daljnjeg ispitivanja njihovog genetičkog stanja, sve su potvrđeni kao žene i dozvoljeno im je takmičenje. Utvrđeno je da ovi sportisti imaju ili djelimičnu ili potpunu neosjetljivost na androgen, uprkos tome što imaju SRY gen, što ih čini fenotipski ženama i ne daje im prednost u odnosu na druge takmičarke.[34] Krajem 1990-ih, broj relevantnih profesionalnih društava u Sjedinjenim Državama pozvao je na ukidanje provjere spola, uključujući Američko medicinsko udruženje, navodeći da je korišteni metod nesiguran i neefikasan. Hromosomski pregled je eliminiran od Ljetnih olimpijskih igara 2000.,[35][36][37] ali nakon toga su uslijedili drugi oblici ispitivanja na osnovu nivoa hormona.[38]
Tekuća ustraživanja
urediUprkos napretku postignutom tokom proteklih nekoliko decenija u proučavanju određivanja spola, gena SRY i proteina TDF, još uvijek se radi na daljem razumijevanju ovih područja. Ostaju faktori koje treba identificirati u molekulskoj mreži koja određuje spol, a hromosomske promjene uključene u mnoge druge slučajeve inverzije spola kod čovjeka još uvijek nisu poznate. Nastavlja se potragu za dodatnim genima za određivanje spola, koristeći tehnike kao što je mikromreže skrining gena genitalnog grebena u različitim razvojnim fazama, mutagenezni zasloni kod miševa za fenotipove inverzije spola i identificiranje gena koji kao transkripcijski faktori djeluju na upotrebu hromatinske imunoprecipitacije.
Također pogledajte
urediReference
uredi- ^ a b c GRCh38: Ensembl release 89: ENSG00000184895 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000069036 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Berta P, Hawkins JR, Sinclair AH, Taylor A, Griffiths BL, Goodfellow PN, Fellous M (novembar 1990). "Genetic evidence equating SRY and the testis-determining factor". Nature. 348 (6300): 448–50. Bibcode:1990Natur.348..448B. doi:10.1038/348448A0. PMID 2247149.
- ^ Wallis MC, Waters PD, Graves JA (oktobar 2008). "Sex determination in mammals--before and after the evolution of SRY". Cellular and Molecular Life Sciences. 65 (20): 3182–95. doi:10.1007/s00018-008-8109-z. PMID 18581056.
- ^ Mittwoch U (oktobar 1988). "The race to be male". New Scientist. 120 (1635): 38–42.
- ^ Katoh K, Miyata T (decembar 1999). "A heuristic approach of maximum likelihood method for inferring phylogenetic tree and an application to the mammalian SOX-3 origin of the testis-determining gene SRY". FEBS Letters. 463 (1–2): 129–32. doi:10.1016/S0014-5793(99)01621-X. PMID 10601652.
- ^ Bakloushinskaya, I Y (2009). "Evolution of sex determination in mammals". Biology Bulletin. 36 (2): 167–174. doi:10.1134/S1062359009020095.
- ^ Veyrunes F, Waters PD, Miethke P, Rens W, McMillan D, Alsop AE, Grützner F, Deakin JE, Whittington CM, Schatzkamer K, Kremitzki CL, Graves T, Ferguson-Smith MA, Warren W, Marshall Graves JA (juni 2008). "Bird-like sex chromosomes of platypus imply recent origin of mammal sex chromosomes". Genome Research. 18 (6): 965–73. doi:10.1101/gr.7101908. PMC 2413164. PMID 18463302.
- ^ Bowles J, Schepers G, Koopman P (novembar 2000). "Phylogeny of the SOX family of developmental transcription factors based on sequence and structural indicators". Developmental Biology. 227 (2): 239–55. doi:10.1006/dbio.2000.9883. PMID 11071752.
- ^ a b Graves JA (decembar 2015). "Weird mammals provide insights into the evolution of mammalian sex chromosomes and dosage compensation". Journal of Genetics. 94 (4): 567–74. doi:10.1007/s12041-015-0572-3. PMID 26690510.
- ^ Ely D, Underwood A, Dunphy G, Boehme S, Turner M, Milsted A (novembar 2010). "Review of the Y chromosome, Sry and hypertension". Steroids. 75 (11): 747–53. doi:10.1016/j.steroids.2009.10.015. PMC 2891862. PMID 19914267.
- ^ Harley VR, Clarkson MJ, Argentaro A (august 2003). "The molecular action and regulation of the testis-determining factors, SRY (sex-determining region on the Y chromosome) and SOX9 [SRY-related high-mobility group (HMG) box 9]". Endocrine Reviews. 24 (4): 466–87. doi:10.1210/er.2002-0025. PMID 12920151.
- ^ Knower KC, Kelly S, Harley VR (2003). "Turning on the male--SRY, SOX9 and sex determination in mammals" (PDF). Cytogenetic and Genome Research. 101 (3–4): 185–98. doi:10.1159/000074336. PMID 14684982. Arhivirano s originala, 9. 8. 2017.
- ^ Friedman, Theodore (2011). Advances in Genetics Vol 76. 108: Elsevier Inc. ISBN 9780123864826.CS1 održavanje: lokacija (link)
- ^ Kashimada K, Koopman P (decembar 2010). "Sry: the master switch in mammalian sex determination". Development. 137 (23): 3921–30. doi:10.1242/dev.048983. PMID 21062860.
- ^ Sekido, Ryohei; Lovell-Badge, Robin (2009). "Sex determination and SRY: down to a wink and a nudge?". Trends in Genetics. 25 (1): 19–29. doi:10.1016/j.tig.2008.10.008. PMID 19027189.
- ^ McClelland K, Bowles J, Koopman P (januar 2012). "Male sex determination: insights into molecular mechanisms". Asian Journal of Andrology. 14 (1): 164–71. doi:10.1038/aja.2011.169. PMC 3735148. PMID 22179516.
- ^ Sekido R, Lovell-Badge R (2013). "Genetic control of testis development". Sexual Development. 7 (1–3): 21–32. doi:10.1159/000342221. PMID 22964823.
- ^ Reference, Genetics Home. "Klinefelter syndrome". Genetics Home Reference (jezik: engleski). Pristupljeno 3. 3. 2020.
- ^ a b Reference, Genetics Home. "Swyer syndrome". Genetics Home Reference (jezik: engleski). Pristupljeno 3. 3. 2020.
- ^ "XX Male Syndrome | Encyclopedia.com". www.encyclopedia.com. Pristupljeno 3. 3. 2020.
- ^ Reference, Genetics Home. "46,XX testicular disorder of sex development". Genetics Home Reference (jezik: engleski). Pristupljeno 3. 3. 2020.
- ^ Polanco JC, Koopman P (februar 2007). "Sry and the hesitant beginnings of male development". Developmental Biology. 302 (1): 13–24. doi:10.1016/j.ydbio.2006.08.049. PMID 16996051.
- ^ Biason-Lauber A, Konrad D, Meyer M, DeBeaufort C, Schoenle EJ (maj 2009). "Ovaries and female phenotype in a girl with 46,XY karyotype and mutations in the CBX2 gene". American Journal of Human Genetics. 84 (5): 658–63. doi:10.1016/j.ajhg.2009.03.016. PMC 2680992. PMID 19361780.
- ^ Marieb, Elaine Nicpon, 1936- (2018). Human anatomy & physiology. Hoehn, Katja (Eleventh izd.). [Hoboken, New Jersey]. ISBN 978-0-13-458099-9. OCLC 1004376412.CS1 održavanje: više imena: authors list (link)
- ^ Yuan X, Lu ML, Li T, Balk SP (decembar 2001). "SRY interacts with and negatively regulates androgen receptor transcriptional activity". The Journal of Biological Chemistry. 276 (49): 46647–54. doi:10.1074/jbc.M108404200. PMID 11585838.
- ^ Lister Hill National Center for Biomedical Communications (2008). "Androgen insensitivity syndrome". Genetics Home Reference. U.S. National Library of Medicine.
- ^ Dewing P, Chiang CW, Sinchak K, Sim H, Fernagut PO, Kelly S, Chesselet MF, Micevych PE, Albrecht KH, Harley VR, Vilain E (februar 2006). "Direct regulation of adult brain function by the male-specific factor SRY". Current Biology. 16 (4): 415–20. doi:10.1016/j.cub.2006.01.017. PMID 16488877.
- ^ Herbarth B, Pingault V, Bondurand N, Kuhlbrodt K, Hermans-Borgmeyer I, Puliti A, Wegner M (1998). "Mutation of the Sry-related Sox10 gene in Dominant megacolon, a mouse model for human Hirschsprung disease". Proceedings of the National Academy of Sciences. 95 (9): 5161–5165. Bibcode:1998PNAS...95.5161H. doi:10.1073/pnas.95.9.5161. PMC 20231. PMID 9560246.
- ^ a b Pritchett J, Athwal V, Roberts N, Hanley NA, Hanley KP (2011). "Understanding the role of SOX9 in acquired diseases: lessons from development". Trends in Molecular Medicine. 17 (3): 166–174. doi:10.1016/j.molmed.2010.12.001. PMID 21237710.
- ^ "OMIM Entry - # 114290 - CAMPOMELIC DYSPLASIA". omim.org. Pristupljeno 29. 2. 2020.
- ^ "Olympic Gender Testing". Arhivirano s originala, 4. 6. 2017. Pristupljeno 20. 3. 2021.
- ^ Facius GM (1. 8. 2004). "The Major Medical Blunder of the 20th Century". Gender Testing. facius-homepage.dk. Arhivirano s originala, 26. 1. 2010. Pristupljeno 12. 6. 2011.
- ^ Elsas LJ, Ljungqvist A, Ferguson-Smith MA, Simpson JL, Genel M, Carlson AS, Ferris E, de la Chapelle A, Ehrhardt AA (2000). "Gender verification of female athletes". Genetics in Medicine. 2 (4): 249–54. doi:10.1097/00125817-200007000-00008. PMID 11252710.
- ^ Dickinson BD, Genel M, Robinowitz CB, Turner PL, Woods GL (oktobar 2002). "Gender verification of female Olympic athletes". Medicine and Science in Sports and Exercise. 34 (10): 1539–42, discussion 1543. doi:10.1097/00005768-200210000-00001. PMID 12370551.
- ^ "IOC Regulations on Female Hyperandrogenism" (PDF). International Olympic Committee. 22. 6. 2012. Arhivirano (PDF) s originala, 13. 8. 2012. Pristupljeno 9. 8. 2012.
Dopunska literatura
uredi- Haqq CM, King CY, Ukiyama E, Falsafi S, Haqq TN, Donahoe PK, Weiss MA (decembar 1994). "Molecular basis of mammalian sexual determination: activation of Müllerian inhibiting substance gene expression by SRY". Science. 266 (5190): 1494–500. Bibcode:1994Sci...266.1494H. doi:10.1126/science.7985018. PMID 7985018.
- Goodfellow PN, Lovell-Badge R (1993). "SRY and sex determination in mammals". Annual Review of Genetics. 27: 71–92. doi:10.1146/annurev.ge.27.120193.000443. PMID 8122913.
- Hawkins JR (1993). "Mutational analysis of SRY in XY females". Human Mutation. 2 (5): 347–50. doi:10.1002/humu.1380020504. PMID 8257986.
- Harley VR (2002). "The molecular action of testis-determining factors SRY and SOX9". The Genetics and Biology of Sex Determination. Novartis Found. Symp. Novartis Foundation Symposia. 244. str. 57–66, discussion 66–7, 79–85, 253–7. doi:10.1002/0470868732.ch6. ISBN 978-0-470-86873-7. PMID 11990798.
- Jordan BK, Vilain E (2003). "Sry and the genetics of sex determination". Pediatric Gender Assignment. Adv. Exp. Med. Biol. Advances in Experimental Medicine and Biology. 511. str. 1–13, discussion 13–4. doi:10.1007/978-1-4615-0621-8_1. ISBN 978-1-4613-5162-7. PMID 12575752.
- Oh HJ, Lau YF (mart 2006). "KRAB: a partner for SRY action on chromatin". Molecular and Cellular Endocrinology. 247 (1–2): 47–52. doi:10.1016/j.mce.2005.12.011. PMID 16414182.
- Polanco JC, Koopman P (februar 2007). "Sry and the hesitant beginnings of male development". Developmental Biology. 302 (1): 13–24. doi:10.1016/j.ydbio.2006.08.049. PMID 16996051.
- Hawkins JR, Taylor A, Berta P, Levilliers J, Van der Auwera B, Goodfellow PN (februar 1992). "Mutational analysis of SRY: nonsense and missense mutations in XY sex reversal". Human Genetics. 88 (4): 471–4. doi:10.1007/BF00215684. PMID 1339396.
- Hawkins JR, Taylor A, Goodfellow PN, Migeon CJ, Smith KD, Berkovitz GD (novembar 1992). "Evidence for increased prevalence of SRY mutations in XY females with complete rather than partial gonadal dysgenesis". American Journal of Human Genetics. 51 (5): 979–84. PMC 1682856. PMID 1415266.
- Ferrari S, Harley VR, Pontiggia A, Goodfellow PN, Lovell-Badge R, Bianchi ME (decembar 1992). "SRY, like HMG1, recognizes sharp angles in DNA". The EMBO Journal. 11 (12): 4497–506. doi:10.1002/j.1460-2075.1992.tb05551.x. PMC 557025. PMID 1425584.
- Jäger RJ, Harley VR, Pfeiffer RA, Goodfellow PN, Scherer G (decembar 1992). "A familial mutation in the testis-determining gene SRY shared by both sexes". Human Genetics. 90 (4): 350–5. doi:10.1007/BF00220457. PMID 1483689.
- Vilain E, McElreavey K, Jaubert F, Raymond JP, Richaud F, Fellous M (maj 1992). "Familial case with sequence variant in the testis-determining region associated with two sex phenotypes". American Journal of Human Genetics. 50 (5): 1008–11. PMC 1682588. PMID 1570829.
- Müller J, Schwartz M, Skakkebaek NE (juli 1992). "Analysis of the sex-determining region of the Y chromosome (SRY) in sex reversed patients: point-mutation in SRY causing sex-reversion in a 46,XY female". The Journal of Clinical Endocrinology and Metabolism. 75 (1): 331–3. doi:10.1210/jc.75.1.331. PMID 1619028.
- McElreavey KD, Vilain E, Boucekkine C, Vidaud M, Jaubert F, Richaud F, Fellous M (juli 1992). "XY sex reversal associated with a nonsense mutation in SRY". Genomics. 13 (3): 838–40. doi:10.1016/0888-7543(92)90164-N. PMID 1639410.
- Sinclair AH, Berta P, Palmer MS, Hawkins JR, Griffiths BL, Smith MJ, Foster JW, Frischauf AM, Lovell-Badge R, Goodfellow PN (juli 1990). "A gene from the human sex-determining region encodes a protein with homology to a conserved DNA-binding motif" (PDF). Nature. 346 (6281): 240–4. Bibcode:=4364 1990Natur.346..240S =4364 Provjerite
|bibcode=length (pomoć). doi:10.1038/346240a0. PMID 1695712. Arhivirano s originala, 22. 3. 2021. Pristupljeno 20. 3. 2021. - Berkovitz GD, Fechner PY, Zacur HW, Rock JA, Snyder HM, Migeon CJ, Perlman EJ (novembar 1991). "Clinical and pathologic spectrum of 46,XY gonadal dysgenesis: its relevance to the understanding of sex differentiation". Medicine. 70 (6): 375–83. doi:10.1097/00005792-199111000-00003. PMID 1956279.
- Berta P, Hawkins JR, Sinclair AH, Taylor A, Griffiths BL, Goodfellow PN, Fellous M (novembar 1990). "Genetic evidence equating SRY and the testis-determining factor". Nature. 348 (6300): 448–50. Bibcode:1990Natur.348..448B. doi:10.1038/348448A0. PMID 2247149.
- Jäger RJ, Anvret M, Hall K, Scherer G (novembar 1990). "A human XY female with a frame shift mutation in the candidate testis-determining gene SRY". Nature. 348 (6300): 452–4. Bibcode:1990Natur.348..452J. doi:10.1038/348452a0. PMID 2247151.
- Ellis NA, Goodfellow PJ, Pym B, Smith M, Palmer M, Frischauf AM, Goodfellow PN (januar 1989). "The pseudoautosomal boundary in man is defined by an Alu repeat sequence inserted on the Y chromosome". Nature. 337 (6202): 81–4. Bibcode:1989Natur.337...81E. doi:10.1038/337081a0. PMID 2909893.
- Whitfield LS, Hawkins TL, Goodfellow PN, Sulston J (maj 1995). "41 kilobases of analyzed sequence from the pseudoautosomal and sex-determining regions of the short arm of the human Y chromosome". Genomics. 27 (2): 306–11. doi:10.1006/geno.1995.1047. PMID 7557997.
Vanjski linkovi
uredi- GeneReviews/NCBI/NIH/UW entry on 46,XX Testicular Disorder of Sex Development
- OMIM entries on 46,XX Testicular Disorder of Sex Development
- Genes, sry na US National Library of Medicine Medical Subject Headings (MeSH)
- Sex-Determining Region Y Protein na US National Library of Medicine Medical Subject Headings (MeSH)
- PDBe-KB provides an overview of all the structure information available in the PDB for Human Sex-determining region Y protein