Mezangijska ćelija
Mezangijske ćelije su specijalizirane ćelije u bubregu, koje čine glomerulski mezangij. Zajedno s mezangijskim matriksom, čine vaskularni pol bubrežnog tijelašca.[1] Mezangijske ćelije čini približno 30-40% ukupnih ćelija u glomerulu.[2] Mezangijske ćelije mogu se kategorizirati ili u vanglomerulske ili ekstraglomerulske mezangijske ćelije ili unutarglomerulske ili intraglomerulske mezangijske ćelije , na osnovu njihove relativne lokacije u odnosu na glomerul. Ekstraglomerulske mezangijske čelije nalaze se između aferentne i eferentne arteriole prema vaskularnom polu glomerula.[3] Ekstraglomerulske mezangijske ćelije susjedne su intraglomerulskim mezangijskim ćelijama koje se nalaze unutar glomerula i između kapilara.[4] Primarna funkcija mezangijskih ćelija je uklanjanje zarobljenih ostataka i nakupljenih proteina iz bazne membrane, čime filter ostaje bez ostataka. Pokazalo se da su kontraktilna svojstva mezangijskih ćelija beznačajna u promjeni filtracijskog glomerulskog pritiska.
| Mezangijska ćelija | |
|---|---|
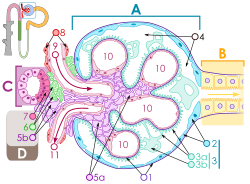 Mezangijske ćelije označene su kao 5a i 5b | |
| Detalji | |
| Prekursor | Mezenhim, stroma ili potporne ćelije glomerula
Lokacija: Glomerulski mezangij bubrega |
| Identifikatori | |
| MeSH | D050527 |
| FMA | 70972 |
| Anatomska terminologija | |
Struktura
urediMezangijske ćelije imaju nepravilne oblike sa spljoštenim cilindričnim tijelima i nastavcima na oba kraja koji sadrže aktin, miozin i aktinin dajući mesangijskim ćelijama kontraktilna svojstva.[5] Sidreni filamenti iz mezangijskih ćelija u glomerulskoj baznoj membrani mogu promijeniti protok kapilara mijenjajući površinu glomerulske ultrafiltracije.[1] Ekstraglomerulskee mezangijske ćelije su u bliskoj vezi sa aferentnim i eferentnnim arteriolskim ćelijama, pomoću međućelijskih spojeva, omogućavajući međućelijsku komunikaciju.[3] Mezangijske ćelije odvojene su međućelijskim prostorima koji sadrže vanćelijski matriks, zvani mesangijski matriks, koji proizvodi mesangijski ćelije.[1] Mezangijski matriks pruža strukturnu potporu mesangiju.[1] Sastoji se od proteina glomerulske matrice kao što su kolagen IV (lanci α1 i α2), kolagen V, kolagen VI, laminin A, B1, B2, fibronektin i proteoglikani.[6]
Razvoj
urediNejasno je da li mezangijske ćelije potiču od mezenhimskih ili strominih ćelija. Međutim, postoje dokazi koji sugeriraju da potiču negdje drugdje izvan glomerula, a zatim migriraju u glomerul tokom razvoja.[7] Ljudski bubrezi fetusa i novorođenčadi obojeni za aktin glatkih mišića (α-SMA), marker za mezangijske ćelije, pokazali su da α-SMA-pozitivne mezenhimske ćelije migriraju prema glomerulu i tokom kasnije faze mogu biti nađene u mesangiju.[5] Moguće je da imaju isto porijeklo kao i potporne ćelije, kao što su pericit i ćelije vaskularnih glatkih mišića, ili čak mogu biti vrsta specijaliziranih vaskularnih ćelija glatkih mišića.[8]
Funkcija
urediFormiranje kapilarnih petlji tokom razvoja
urediTokom razvoja, mezangijske ćelije su važne za formiranje izuvijanih kapilara omogućavajući efikasnu difuziju. Prekursorne endotelne ćelije izlučuju trombocit-izvedeni faktor rasta) (PDGF)-B, a mezangijske ćelije imaju receptore za PDGF. To inducira mezangijske ćelije da se prikače za endotelne ćelije, što dovodi do petlje u razvoju krvnih sudova, što rezultira savijenim kapilarama.[8] Miševi kojima nedostaje faktor rasta PDGF-B ili PDGFRβ ne razvijaju mezangijske ćelije.[8] Kad nema mesangijsskih ćelija , krvni sud postaje jednostruko proširena žila s do 100 puta smanjenom površinom.[8] Za razvoj mezangijskih ćelija, presudan je transkripcijski faktor za PDGFRβ, Tbx18. Bez Tbx18, razvoj mesangijskih ćelija je ugrožen i rezultira stvaranjem proširenih petlji.[8] Progenitori mezangijskih ćelija također su meta PDGF-B -a i signal ih može odabrati da bi se potom razvili u mesangijske ćelije.[9]
Interakcije s drugim bubrežnim ćelijama
urediMezangijske ćelije čine glomerulsku funkcijsku jedinicu sa glomerulskim endotelnim ćelijama i podocitima, putem interakcija molekulskih signalnih puteva koji su neophodni za formiranje glomerulaskog snopa.[1] Mezangijske ćelije pomažu filtraciji, čineći dio struktura glomerulskog kapilarnog snopa koji filtrira tečnosti da bi proizveo urin.[10] Komunikacija između mezangijskih ćelija i vaskularnih glatkih mišićnih ćelija putem spojeva između jazova pomaže u regulaciji procesa tubuloglomerulske povratne informacije i stvaranja urina.[11] > Oštećenje mezangijskih ćelija korištenjem Thy 1-1 antitijela, specifičnog za mesangijske ćelije, dovodi do gubitka sposobnosti vazokonstrikcije arteriola, posredovanih tubuloglomerulskom povratnom spregom.[11]
Regulirajuće kontrakcije kapilarnog protoka
urediMezangijske ćelije se mogu skupiti i opustiti da reguliraju kapilarni protok.[1] To regulira vazoaktivne supstance.[12] Kontrakcija mezangijskih ćelija ovisi o propusnosti ćelijske membrane za ione kalcija, a opuštanje je posredovano parakrinim faktorima, hormonima i cAMP-om.[12] Kao odgovor na kapilarno istezanje, mezangijske ćelije mogu stvarati nekoliko faktora rasta: TGF-1, VEGF i faktor rasta vezivnog tkiva.[1]
Uklanjanje makromolekula
urediMezangij je izložen makromolekulama iz lumena kapilara, jer su odvojeni samo fenestriranim endotelom, bez bazne membrane.[2] Mezangijske ćelije imaju ulogu u ograničavanju akumuliranja makromolekula u mesangijskom prostoru, procesima usvajanja nezavisnih od receptora, kao što su fagocitoza, mikro- i makro - pinocitoza ili procesi koji zavise od receptora, a zatim se transportuju duž mezangijalne stabljike.[1] Veličina, naboj, koncentracija i afinitet za mesangijske ćelijske receptore makromolekula, utiče na način uklanjanja makromolekula.[13] > Trigliceridi mogu proći kroz pinocitozu, a kompleksi antitela IgG mogu dovesti do aktivacije adhezivnih molekula i hemokina u mezangijskim ćelijama.[1]
Klinički značaj
urediDijabetska nefropatija
urediŠirenje mezangijalnog matriksa jedna je od karakteristika dijabetske nefropatije, mada u interakciji učestvuju i druge ćelije, uključujući podocite i endotelne ćelije.[14] Do mesangijske ekspanzije dolazi uslijed povećanog taloženja proteina vanćelijskog matriksa, naprimjer fibronektina, u mezangij.[6] Akumulacija proteina vanćelijskog matriksa nastaje zbog nedovoljne razgradnje matriksnih metaloproteinaza.
Povećani nivoi glukoze rezultiraju aktivacijom metaboličkog puta, što dovodi do povećanog oksidativnog stresa.[2] To zauzvrat rezultira prekomjernom proizvodnjom i akumulacijom krajnjih proizvoda napredne glikozilacije, odgovornih za povećavajući rizik od razvoja glomerulskih bolesti.[15] Mesangial cells grown on advanced glycosylation end product-modified matrix proteins demonstrate increased production of fibronectin and a decrease in proliferation.[15] Ovi faktori na kraju dovode do zadebljanja glomerulske bazne membrane, širenja mezangijalnog matriksa, a zatim i bolesti kao što su glomeruloskleroza i fibroza.[16]
Mesangijske patologije mogu se razviti i tokom rane faze dijabetesa. Glomerulska hipertenzija uzrokuje rastezanje mezangijskih ćelija, što uzrokuje induciranu ekspresiju GLUT1 i posljedično do povećane razine ćelijske glukoze.[16] Ponavljanje ciklusa istezanja i opuštanja mezangijskih ćelija zbog hipertenzije povećava njihovu proliferaciju i proizvodnju vanćelijskoh matriksa, koji se potom može akumulirati i dovesti do glomerulske bolesti.[16]
Također pogledajte
urediReference
uredi- ^ a b c d e f g h i Schlondorff, D; Banas, B (2009). "The Mesangial Cell Revisited: No Cell Is an Island". Journal of the American Society of Nephrology. 20 (6): 1179–1187. doi:10.1681/ASN.2008050549. PMID 19470685.
- ^ a b c Scindia, Y; Deshmukh, U; Bagavant, H (2010). "Mesangial pathology in glomerular disease: targets for therapeutic intervention". Advanced Drug Delivery Reviews. 62 (14): 1337–1343. doi:10.1016/j.addr.2010.08.011. PMC 2992591. PMID 20828589.
- ^ a b Barajas, L (1997). "Cell-specific protein and gene expression in the juxtaglomerular apparatus". Clin Exp Pharmacol Physiol. 24 (7): 520–526. doi:10.1111/j.1440-1681.1997.tb01239.x. PMID 9248671.
- ^ Goligorsky, M; Iijima, K; Krivenko, Y; Tsukahara, H; Hu, Y; Moore, L (1997). "Role of mesangial cells in macula densa to afferent arteriole information transfer". Clin Exp Pharmacol Physiol. 24 (7): 527–531. doi:10.1111/j.1440-1681.1997.tb01240.x. PMID 9248672.
- ^ a b Takano, K; Kawasaki, Y; Imaizumi, T; Matsuura, H; Nozawa, R; Tannji, M; Suyama, K; Isome, M; Suzuki, H; Hosoya, M (2007). "Development of Glomerular Endothelial Cells, Podocytes and Mesangial Cells in the Human Fetus and Infant". The Tohoku Journal of Experimental Medicine. 212 (1): 81–90. doi:10.1620/tjem.212.81. PMID 17464107.
- ^ a b Mason, R; Wahab, N (2003). "Extracellular Matrix Metabolism in Diabetic Nephropathy". Journal of the American Society of Nephrology. 14 (5): 1358–1373. doi:10.1097/01.ASN.0000065640.77499.D7. PMID 12707406.
- ^ Faa, G; Gerosa, C; Fanni, D; Monga, G; Zaffanello, M; Van Eyken, P; Fanos, V (2011). "Morphogenesis and molecular mechanisms involved in human kidney development". J. Cell. Physiol. 227 (3): 1257–1268. doi:10.1002/jcp.22985. PMID 21830217.
- ^ a b c d e Schell, C; Wanner, N; Huber, T (2014). "Glomerular development – Shaping the multi-cellular filtration unit". Seminars in Cell & Developmental Biology. 36 (2): 39–49. doi:10.1016/j.semcdb.2014.07.016. PMID 25153928.
- ^ Lindahl, P; Hellstrom, M; Kalen, M; Karlsson, L; Pekny, M; Pekna, M; Soriano, P; Betsholtz, C (1998). "Paracrine PDGF-B/PDGF-Rbeta signaling controls mesangial cell development in kidney glomeruli". Development. 125 (17): 3313–3322. PMID 9693135.
- ^ Vaughan, M; Quaggin, S (2008). "How Do Mesangial and Endothelial Cells Form the Glomerular Tuft?". Journal of the American Society of Nephrology. 19 (1): 24–33. doi:10.1681/ASN.2007040471. PMID 18178797.
- ^ a b Ren, Y; Carretero, O; Garvin, J (2002). "Role of mesangial cells and gap junctions in tubuloglomerular feedback". Kidney International. 62 (2): 525–531. doi:10.1046/j.1523-1755.2002.00454.x. PMID 12110013.
- ^ a b Stockand, J; Sansom, S (1998). "Glomerular mesangial cells: electrophysiology and regulation of contraction". Physiological Reviews. 78 (3): 723–744. doi:10.1152/physrev.1998.78.3.723. PMID 9674692.
- ^ Schlondorff, D (1996). "Roles of the mesangium in glomerular function". Kidney International. 49 (6): 1583–1585. doi:10.1038/ki.1996.229. PMID 8743459.
- ^ Brunskill, E; Potter, S (2012). "Changes in the gene expression programs of renal mesangial cells during diabetic nephropathy". BMC Nephrol. 13 (1): 70. doi:10.1186/1471-2369-13-70. PMC 3416581. PMID 22839765.
- ^ a b Skolnik, E; Yang, Z; Makita, Z; Radoff, S; Kirstein, M; Vlassara, H (1991). "Human and rat mesangial cell receptors for glucose-modified proteins: potential role in kidney tissue remodelling and diabetic nephropathy". Journal of Experimental Medicine. 174 (4): 931–939. doi:10.1084/jem.174.4.931. PMC 2118966. PMID 1655949.
- ^ a b c Kanwar, Y; Wada, J; Sun, L; Xie, P; Wallner, E; Chen, S; Chugh, S; Danesh, F (2008). "Diabetic Nephropathy: Mechanisms of Renal Disease Progression". Experimental Biology and Medicine. 233 (1): 4–11. doi:10.3181/0705-MR-134. PMID 18156300.