Svjetlački luciferin
Luciferin svjetlaca (također poznat kao tvrdokrilački luciferin) je luciferin, ili spoj koji emituje svjetlost, koji koriste svjetlaci (Lampyridae) , željeznički crvi (Phengodidae), zvjezdasti crvi (Rhagophthalmidae) i bioluminiscentni sistemi insekata grupe Pyrophorini). To je supstrat luciferaze (EC 1.13.12.7), koji je odgovoran za karakterističnu emisiju žute svjetlosti iz mnogih vrsta krijesnica.
| Svjetlački luciferin | |
|---|---|
 | |
| Općenito | |
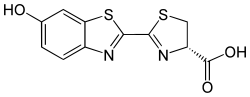
| Hemijski spoj | Svjetlački luciferin |
| Druga imena | D-(−)-Luciferin, luciferin svjetlaca IUPAC-ime: (4S)-2-(6-hidroksi-1,3-benzotiazol-2-il)-4,5-dihidrotiazol-4-karboksilna kiiselina |
| Molekularna formula | C11H8N2O3S2 |
| CAS registarski broj | 2591-17-5 |
| SMILES | O=C(O)[C@@H]1/N=C(\SC1)c2sc3cc(O)ccc3n2 |
| Kratki opis | Bioluminiscentni luciferin kod svitaca |
| Osobine1 | |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
Kao i kod svih drugih luciferina, za izazivanje svetlosti je neophodan kisik; međutim, također je utvrđeno da su za emisiju svetlosti potrebni adenozin-trifosfat (ATP) i magnezij[1][2]
Svojstva
urediUtvrđeno je da je kristalni luciferin fluorescentan, apsorbira ultraljubičasto svjetlo s maksimumom na 327 nm i emituje svjetlost s maksimumom na 530 nm. Vidljiva emisija se javlja nakon relaksacije oksiluciferina iz singletnog pobuđenog stanja do njegovog osnovnog stanja.[3] Alkalni rastvori uzrokovali su crveni pomak apsorpcije vjerovatno zbog deprotonacije hidroksil grupe na benzotiazolu, ali nisu utjecale na emisiju fluorescencije. Utvrđeno je da luciferil-adenilat (AMP ester luciferina) spontano emituje svetlost u rastvoru.[4]
Različite vrste svitacaca koriste isti luciferin, međutim boja emitovane svjetlosti može se značajno razlikovati. Svjetlost iz Photuris pennsylvanica je izmjerena na 552 nm (zeleno-žuta) dok je izmjereno da Pyrophorus plagiophthalamus emituje svjetlost na 582 nm (narandžasta) u ventralni organ. Takve razlike su vjerovatno zbog pH promjena ili razlika u primarnoj strukturi luciferaze.[5] Modifikacija supstrata luciferina krijesnice dovela je do emisije "crvenog pomaka" (emisije do talasne dužine od 675 nm).[6]
Biološka aktivnost
urediSinteza svjetlačkog luciferina in vivo nije u potpunosti shvaćena. Proučen je samo posljednji korak enzimskog puta, a to je reakcija kondenzacije D-cisteina sa 2-cijano-6-hidroksibenzotiazolom, ista reakcija koja se koristi za proizvodnju sintetskog spoja.[7] To je potvrđeno radioobilježavanjem atoma u dva spoja i identifikacijom "enzima koji regenerira luciferinski".[8]
U svjetlacima, oksidacija luciferina, koju kataliziraju luciferaze, daje peroksi spoj 1,2-dioksetan. Dioksetan je nestabilan i spontano se raspada do ugljik dioksida i pobuđenih ketona, koji oslobađaju višak energije, emitujući svjetlost (bioluminiscencija)[9]
Luciferin svjetlaca i modificirani supstrati oponašaju masne kiseline i korišteni su za lokalizaciju amida masnokiselinski hidrolaza (FAAH) in vivo.[10] Luciferin krijesnica je supstrat ABCG2 transportera i korišten je kao dio bioluminiscentnog predstavljanja visoke preciznosti za skrining na inhibitore transportera.[11]
Reference
uredi- ^ McElroy WD (1947). "The Energy Source for Bioluminescence in an Isolated System". Proc Natl Acad Sci USA. 33 (11): 342–345. Bibcode:1947PNAS...33..342M. doi:10.1073/pnas.33.11.342. PMC 1079070. PMID 16588763.
- ^ Green A, McElroy WD (1956). "Function of adenosine triphosphate in the activation of luciferin". Arch Biochem Biophys. 64 (2): 257–271. doi:10.1016/0003-9861(56)90268-5. PMID 13363432.
- ^ Marques SM, Joaquim (2009). "Firefly Bioluminescence: A Mechanistic Approach of Luciferase Catalyzed Reactions". IUBMB Life. 61 (1): 6–17. doi:10.1002/iub.134. PMID 18949818. S2CID 21583225.
- ^ Rhodes WC, McElroy WD (1958). "The synthesis and function of luciferyl-adenylate and oxyluciferyl-adenylate". J Biol Chem. 233 (6): 1528–1537. doi:10.1016/S0021-9258(18)49367-2. PMID 13610868.
- ^ Seliger HH, Buck JB, Fastie WG, McElroy WD (1964). "The Spectral Distribution of Firefly Light". J Gen Physiol. 48 (1): 95–104. doi:10.1085/jgp.48.1.95. PMC 2195396. PMID 14212153.
- ^ Kiyama M, Saito R, Iwano S, Obata R, Niwa H, Maki SA (2016). "Multicolor Bioluminescence Obtained Using Firefly Luciferin". Current Topics in Medicinal Chemistry. 16 (24): 2648–2655. doi:10.2174/1568026616666160413135055. PMID 27072707.
- ^ White EH, Worther H, Field GF, McElroy WD (1965). "Analogs of Firefly Luciferin". J. Org. Chem. 30 (7): 2344–2348. doi:10.1021/jo01018a054.
- ^ Gomi K, Kajiyama N (2001). "Oxyluciferin, a Luminescence Product of Firefly Luciferase, Is Enzymatically Regenerated into Luciferin". J Biol Chem. 276 (39): 36508–36513. doi:10.1074/jbc.M105528200. PMID 11457857.
- ^ Aldo Roda Chemiluminescence and Bioluminescence: Past, Present and Future, p. 57, Royal Society of Chemistry, 2010, ISBN 1-84755-812-7
- ^ Mofford DM, Adams ST, Kumar Reddy GS, Randheer Reddy G, Miller SC (2015). "Luciferin Amides Enable in Vivo Bioluminescence Detection of Endogenous Fatty Acid Amide Hydrolase Activity". J. Am. Chem. Soc. 137 (27): 8684–8687. doi:10.1021/jacs.5b04357. PMC 4507478. PMID 26120870.
- ^ "Identification of Inhibitors of ABCG2 by a Bioluminescence Imaging-Based High-Throughput Assay". Cancer Res. 69.
Vanjski linkovi
uredi- Bioluminescence Page showing major luciferin types