Mangan peroksidaza
U enzimologiji, mangan peroksidaza (EC broj 1.11.1.13) jeste enzim koji katalizira hemijsku reakciju:
- 2 Mn(II) + 2 H+ + H2O2 2 Mn(III) + 2 H2O
Tri supstrata ovog enzima su Mn(II), H+ i H2O2, dok su njegova dva proizvoda Mn(III) i H2O.
Ovaj enzim pripada porodici oksidoreduktaza, tačnije onima koje djeluju na peroksid kao primalac (peroksidazama). Sistematsko ime ove klase enzima je Mn(II):vodik-peroksid oksidoreduktaza. Druga uobičajena imena, između ostalih, su peroksidaza-M2 i "peroksidaza zavisna od Mn" (koja oksidira NADH). Ona uključuje jedan kofaktor, hem. Za aktivnost ovog enzima neophodan je ion kalcija, Ca2+.
Neke vrste gljiva poput Cyathus stercoreus luče ovaj enzim koji im pomaže u degradaciji lignina.
Otkriće i opis
urediMangan peroksidaza (često se označava skraćenicom MnP) otkrivena je 1985. godine. Otkrili su je dvije grupe naučnika okupljenih oko Michaela H. Golda[1] i Ronalda Crawforda,[2] u gljivi Phanerochaete chrysosporium. Njen protein je genetski sekvenciran 1989. u P. chrysoporium.[3] Za enzim se smatralo da je jedinstven unutar Basidiomycota, jer do tada nije otkriveno da ga prirodno ne proizvodi niti jedna vrsta bakterija, plijesni ili kvasaca.
Mehanizam reakcije
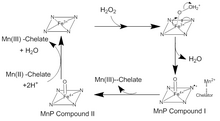
urediMnP kataliza se dešava u seriji nepovratnih oksidacijsko-redukcijskih reakcija (redoks reakcija) koja slijedi takozvani ping-pong mehanizam sa kinetikom drugog reda.[4] U prvom koraku katalitičkog ciklusa, vodik-peroksid H2O2 ili neki organski peroksid spaja se na aktivno mjesto na MnP. Tako se kisik iz H2O2 veže na ion željeza Fe(III) u kofaktoru hema dajuću kompleks željezo-peroksida. Dva elektrona prelaze sa iona Fe3+ na peroksid, razbijajući vezu kisik-peroksid te gradeći vodu i kompleks radikala Fe(IV) okso-porfirin. Ovaj oksidirani međuspoj poznat je kao MnP spoj I. Zatim se MnP spoj I veže s monoheliranim ionom Mn(II), koji donira elektron da bi ugasio radikal i oformio Mn(III) MnP spoj II, odnosno kompleks Fe(IV) okso-porfirina. Zatim MnP spoj II oksidira sljedeći ion Mn(II) do Mn(III) a reducira se reakcijom dva iona H+ a željezo se veže kisikom. Ovo reformira Fe(III) ion u hemu i otpušta drugu molekulu vode.[5] Postoji mnogo devijacija od ovog tradicionalnog katalitičkog ciklusa. MnP spoj I se može koristiti za oksidaciju slobodnog Mn(II), ferocijanida, kao i fenola i drugih aromatskih spojeva.[6]
Reference
uredi- ^ Glenn JK, Gold MH (1. 11. 1985). "Purification and characterization of an extracellular Mn(II)-dependent peroxidase from the lignin-degrading basidiomycete, Phanerochaete chrysosporium". Arch. Biochem. Biophys. 242 (2): 329–41. doi:10.1016/0003-9861(85)90217-6. PMID 4062285.
- ^ Paszcynski A, Huynh V-B, Crawford R, (1. 8. 1985). "Enzymatic activities of an extracellular, manganese- dependent peroxidase from Phanerochaete chrysosporium". FEMS Microbiol. Lett. 29 (1–2): 37–41. doi:10.1111/j.1574-6968.1985.tb00831.x.CS1 održavanje: dodatna interpunkcija (link) CS1 održavanje: više imena: authors list (link)
- ^ Pribnow D, Mayfield MB, Nipper VJ, Brown JA, Gold MH (1. 3. 1989). "Characterization of a cDNA encoding a manganese peroxidase, from the lignin-degrading basidiomycete Phanerochaete chrysosporium". J. Biol. Chem. 264 (9): 5036–40. PMID 2925681.CS1 održavanje: više imena: authors list (link)[mrtav link]
- ^ Wariishi H, Valli K, Gold MH (1. 11. 1992). "Manganese(II) oxidation by manganese peroxidase from the basidiomycete Phanerochaete chrysosporium. Kinetic mechanism and role of chelators". J. Biol. Chem. 267 (33): 23688–95. PMID 1429709.CS1 održavanje: više imena: authors list (link)[mrtav link]
- ^ Hofrichter M (1. 4. 2002). "Review: lignin conversion by manganese peroxidase (MnP).". Enzyme and Microbial Technology. 30 (4): 454–66. doi:10.1016/S0141-0229(01)00528-2.
- ^ Heinfling A, Ruiz-Dueñas FJ, Martínez MJ, Bergbauer M, Szewzyk U, Martínez AT (1. 5. 1998). "A study on reducing substrates of manganese-oxidizing peroxidases from Pleurotus eryngii and Bjerkandera adusta". FEBS Lett. 428 (3): 141–6. doi:10.1016/s0014-5793(98)00512-2. PMID 9654123.CS1 održavanje: više imena: authors list (link)
