Dušični iperit
Dušični iperiti su citotoksični organski spojevi sa hloretilaminskom (Cl(CH2)2NR2) funkcionalnom grupom.[1] Iako su prvobitno proizvedeni kao hemijska ratna sredstva,[2][3] bili su prvi hemoterapeutski agensi za lečenje raka.[4] Dušični iperiti su nespecifični DNK agensi za alkilaciju.


Hemijski rat
urediTokom Drugog svetskog rata dušični iperiti su proučavani na Yale School of Medicine pod vođstvom Alfreda Gilmana i Louisa Goodmana i klasifikovani su za klinička ispitivanja dejstva dušićnih iperita na ljudima za liječenje limfoma, započeta u decembru 1942.[5] Također tokom Drugog svetskog rata, incident tokom zračnog napada na Bari, Italija, doveo je do oslobađanja iperita koji je pogodio nekoliko stotina vojnika i civila.[6] Medicinski pregled preživjelih pokazao je smanjen broj limfocita.[7] Nakon što je Drugi svjetski rat završen, incident u Bariju i studije Yale grupe su se na kraju spojile što je dovelo do traženja drugih sličnih spojeva. Zbog svoje upotrebe u prethodnim studijama, dušični iperit poznat kao "HN2" postao je prvi hemoterapijski lijek mustin.
Dušični iperiti nisu povezani sa biljkom gorušice ili njenom oštrom esencijom, alil izotiocijanatom; ime dolazi od oštrog mirisa preparata hemijskog oružja.[8]
Primjeri
urediDušičnoiperitni lijek mustin (HN2), više nije uobičajeno u upotrebi u svojoj originalnoj IV formulaciji zbog prevelike toksičnosti. Ostali razvijeni dušični iperiti uključuju ciklofosfamid, klorambucil, uramustin, melfalan i bendamustin.[9] Bendamustin se nedavno ponovo pojavio kao održiv hemoterapeutski tretman.[10]
Dušični iperiti koji se mogu koristiti u svrhe hemijskog ratovanja strogo su regulisani. Njihove oznake oružja su:[11]
- HN1: Bis(2-hloretil)etilamin
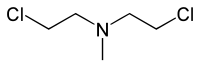
- HN2: Bis(2-hloretil)metilamin
- HN3: tris(2-kloroetil)amin
Nor-iperit se može koristiti u sintezi piperazinskih lijekova. Na primjer, mazapertin, aripiprazol i fluanizon. Canfosfamid je takođe napravljen od noriperita.
Pripremljeni su i neki dušični iperiti od opijata, iako nije poznato da su antineoplastični. Primjeri uključuju klornaltreksamin i hloroksimorfamin.
Mehanizam djelovanja
urediDušični iperiti (NM) formiraju ciklične aminijske ione (aziridinijski prstenovi) unutarmolekulskim izmeštanjem hlorida aminskim gušikom. Ova grupa aziridinija zatim alkiluje DNK kada je napadne N-7 nukleofilni centar na guaninskoj bazi. Drugi napad nakon istiskivanja drugog hlora formira drugi korak alkilacije koji rezultira formiranjem međulančanih poprečnih veza (ICL) kao što je pokazano početkom 1960-ih. U to vrijeme je predloženo da se ICL formiraju između N-7 atoma guaninskog ostatka u 5'-d(GC) sekvenci.[12][13] Later it was clearly demonstrated that NMs form a 1,3 ICL in the 5’-d(GNC) sequence.[14][15][16][17]
Snažan citotoksični efekt uzrokovan stvaranjem ICL je ono što NM čini efikasnim hemoterapeutskim agensom. Drugi spojevi koji se koriste u hemoterapiji raka a imaju sposobnost da formiraju ICL su cisplatin, mitomicin C, karmustin i psoralen.[18]
Dušični iperiti su moćn i postojana pjenušava sredstva. HN1, HN2, HN3 su stoga klasifikovani kao Spiska 1 supstanci unutar Konvencije o hemijskom oružju.[19] Stoga je proizvodnja i upotreba strogo ograničena.[20]
Reference
uredi- ^ "Mustards". The IUPAC Compendium of Chemical Terminology. 2014. doi:10.1351/goldbook.M04071.
- ^ Nitrogen mustard gas was stockpiled by several nations during the Second World War, but it was never used in combat.Daniel C. Keyes; Jonathan L. Burstein; Richard B. Schwartz; Raymond E. Swienton (2004). Medical Response to Terrorism: Preparedness and Clinical Practice. Lippincott Williams & Wilkins. str. 16. ISBN 978-0781749862 – preko books.google.com.
- ^ Centers for Disease Control and Prevention (4. 4. 2013). "Facts About Nitrogen Mustards". cdc.gov. Arhivirano s originala, 3. 9. 2013. Pristupljeno 12. 9. 2013.
- ^ Chabner, Bruce A.; Roberts, Thomas G. (2005). "Chemotherapy and the war on cancer". Nature Reviews Cancer. 5 (1): 65–72. doi:10.1038/nrc1529. PMID 15630416. S2CID 205467419.
- ^ Gilman A (maj 1963). "The initial clinical trial of nitrogen mustard". Am. J. Surg. 105 (5): 574–8. doi:10.1016/0002-9610(63)90232-0. PMID 13947966.
- ^ Jules Hirsch, MD; Journal of the American Medical Association (2006). "An Anniversary for Cancer Chemotherapy". JAMA. jamanetwork.com. 296 (12): 1518–1520. doi:10.1001/jama.296.12.1518. PMID 17003400.
- ^ Hirsch J (septembar 2006). "An anniversary for cancer chemotherapy". JAMA. 296 (12): 1518–20. doi:10.1001/jama.296.12.1518. PMID 17003400.
- ^ Ghorani-Azam, Adel; Balali-Mood, Mahdi (1. 12. 2015). "Clinical Pharmacology and Toxicology of Mustard Compounds". Basic and Clinical Toxicology of Mustard Compounds. Springer Science+Business Media. str. 64. ISBN 9783319238746. Pristupljeno 12. 3. 2019 – preko Google Books.
- ^ Mattes, W. B.; Hartley, J. A.; Kohn, K. W. (1986). "DNA sequence selectivity of guanine–N7 alkylation by nitrogen mustards". Nucleic Acids Research. 14 (7): 2971–2987. doi:10.1093/nar/14.7.2971. PMC 339715. PMID 3960738.
- ^ Cheson BD, Rummel MJ (mart 2009). "Bendamustine: rebirth of an old drug". J. Clin. Oncol. 27 (9): 1492–501. doi:10.1200/JCO.2008.18.7252. PMID 19224851.[trajno mrtav link]
- ^ University of Durham. "SCHEDULE 1 CHEMICALS" (PDF). dur.ac.uk.
- ^ Geiduschek EP (juli 1961). ""Reversible" DNA". Proc. Natl. Acad. Sci. U.S.A. 47 (7): 950–5. Bibcode:1961PNAS...47..950G. doi:10.1073/pnas.47.7.950. PMC 221307. PMID 13704192.
- ^ Brookes P, Lawley PD (septembar 1961). "The reaction of mono- and di-functional alkylating agents with nucleic acids". Biochem. J. 80 (3): 496–503. doi:10.1042/bj0800496. PMC 1243259. PMID 16748923.
- ^ Millard JT, Raucher S, Hopkins PB (1990). "Mechlorethamine Cross Links Deoxyguanosine Residues at 5'-GNC Sequences in Duplex DNA Fragments". Journal of the American Chemical Society. 112 (6): 2459–60. doi:10.1021/ja00162a079.
- ^ Rink SM, Solomon MS, Taylor MJ, Rajur SB, McLaughlin LW, Hopkins PB (1993). "Covalent structure of a nitrogen mustard-induced DNA interstrand cross-link: An N7-to-N7 linkage of deoxyguanosine residues at the duplex sequence 5'-d(GNC)". Journal of the American Chemical Society. 115 (7): 2551–7. doi:10.1021/ja00060a001.
- ^ Dong Q, Barsky D, Colvin ME, et al. (decembar 1995). "A structural basis for a phosphoramide mustard-induced DNA interstrand cross-link at 5'-d(GAC)". Proc. Natl. Acad. Sci. U.S.A. 92 (26): 12170–4. Bibcode:1995PNAS...9212170D. doi:10.1073/pnas.92.26.12170. PMC 40318. PMID 8618865.
- ^ Bauer GB, Povirk LF (mart 1997). "Specificity and kinetics of interstrand and intrastrand bifunctional alkylation by nitrogen mustards at a G-G-C sequence". Nucleic Acids Res. 25 (6): 1211–8. doi:10.1093/nar/25.6.1211. PMC 146567. PMID 9092631.
- ^ Guainazzi, A.; Schärer, O. D. (2010). "Using synthetic DNA interstrand crosslinks to elucidate repair pathways and identify new therapeutic targets for cancer chemotherapy". Cellular and Molecular Life Sciences. 67 (21): 3683–3697. doi:10.1007/s00018-010-0492-6. PMC 3732395. PMID 20730555.
- ^ Organisation for the Prohibition of Chemical Weapons. "Chemical Weapons Convention: Schedule 1 Toxic chemicals". opcw.org. Arhivirano s originala, 7. 6. 2013.
- ^ United States Department of State, Bureau of Arms Control, Verification and Compliance; United States Department of Commerce, Bureau of Industry and Security (maj 2004). "Introduction to Industry Implementation of the Chemical Weapons Convention" (PDF). cwc.gov. Arhivirano s originala (PDF), 20. 10. 2013. Pristupljeno 12. 9. 2013.CS1 održavanje: više imena: authors list (link)
Dopunska literatura
uredi- Stanford University School of Medicine (2013). "Topical Nitrogen Mustard (Mustargen)". stanford.edu.
- University of California, Los Angeles (2002). "Brassica alba or Sinapis nigra". ucla.edu.
Šablon:Dušik-iperit Šablon:Hemijsko oružje Šablon:Unutarćelijski hemotherapeutski agensi Šablon:Detoksikacijski agensi za antineoplazijski tretman