Difosfor
Difosfor je neorganska supstanca sa hemijskom formulom P2. Za razliku od dušikove grupe susjedni dušik, koji sačinjava stabilnu N2 molekulu s trostrukom vezom dušika na dušik, fosfor više ide na tetraedarski obrazac P4, jer su P-P pi-veze visokoenergetske. Difosfor je vrlo reaktivan s energijom razlaganja veze (117 kcal/mola ili 490 kJ/mol) koja je upola manja od dušikove. Udaljenost veza je izmjerena na 1,8934 Å.[1][2]
| Difosfor | |
|---|---|
  | |
| Općenito | |
| Hemijski spoj | Difosfor |
| Druga imena | IUPAC ime: Difosfor |
| Molekularna formula | P2 |
| CAS registarski broj | 12185-09-0 |
| SMILES | P#P |
| InChI | 1/P2/c1-2 |
| Osobine1 | |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
Difosfor nastaje zagrijavanjem žutog fosfora na 1100 kelvina. Ipak, ostvaren je izvjesni napredak i nastale su diatomske molekule i homogena otopina u normalnim uslovima, uz korištenje nekih prijelaznih metalnih kompleksa na temelju, primjerice, volframa i niobija).
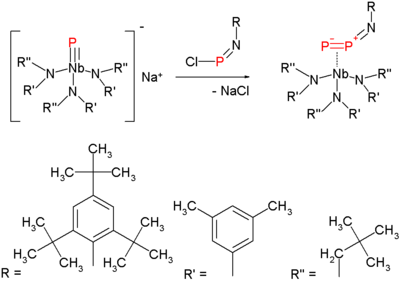
Molekula je privukla pažnju 2006. godine, kada se pojavila nova metoda za njenu sintezu pri blažim temperaturama.[3] Ova metoda je varijacija na isključenje dušika u azidu sa nastankom nitrena. Sinteza difosforovog prekursora sastoji se u reagiranju terminalnog niobij fosfida sa hloroiminofosfanom:
Zagrijavanje ovog spoja na 50 °C i 1,3-cikloheksadiena služi kao rastvarač i kao hvatajući reagens isključenog difosfora, koji je reaktivan, jer stvara dvostruku Diels-Alder proizvod i niobij imido spoj:
Također nastaje isti imido spoj kada se termoliza vrši u toluenu, ali je zatim sudbina difosfora nepoznata.[4] [5][6][7] Predloženo je da se P2 formira kao međuproizvod u fotolizi P4, a u prisustvu 2,3-dimetil-1,3-butadiena ponovo nastaje difosfan. Do danas nema ni neposrednih dokaza za nastanak P2 preko fotolize P4.
Bilo je objavljeno nastanak difosfora iz difosfor bisantracenskog adukta. Postoji i izvještaj o sintezi stabilizovanog kationa HP2+.
Također pogledajte
urediReference
uredi- ^ "Diphosphorus (CHEBI:33472)". Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ^ Huber, K. P.; Herzberg, G. (1979). Molecular Spectra and Molecular Structure. IV: Constants of Diatomic Molecules. New York: Van Nostrand. ISBN 0442233949.CS1 održavanje: upotreba parametra authors (link)
- ^ A Retro Diels–Alder Route to Diphosphorus Chemistry: Molecular Precursor Synthesis, Kinetics of P2 Transfer to 1,3-Dienes, and Detection of P2 by Molecular Beam Mass Spectrometry Alexandra Velian, Matthew Nava, Manuel Temprado, Yan Zhou, Robert W. Field, and Christopher C. Cummins Journal of the American Chemical Society 2014 136 (39), 13586-13589 doi:10.1021/ja507922x
- ^ Piro, Nicholas A.; Figueroa, Joshua S.; McKellar, Jessica T.; Cumnins, Christopher C. (1. 9. 2006). "Triple-Bond Reactivity of Diphosphorus Molecules". Science. 313 (5791): 1276–1279. Bibcode:2006Sci...313.1276P. doi:10.1126/science.1129630. PMID 16946068. Pristupljeno 21. 7. 2013.
- ^ Rathenau, G. (juni 1937). "Optische und photochemische versuche mit phosphor" [Optical and photochemical trials with phosphorus]. Physica (jezik: German). 4 (6): 503–514. Bibcode:1937Phy.....4..503R. doi:10.1016/S0031-8914(37)80084-1. Pristupljeno 21. 7. 2013.CS1 održavanje: nepoznati jezik (link)
- ^ Tofan, Daniel; Cummins, Christopher C. (26. 8. 2010). "Photochemical incorporation of diphosphorus units into organic molecules". Angewandte Chemie International Edition. 49 (41): 7516–7518. doi:10.1002/anie.201004385. Pristupljeno 21. 7. 2013.
- ^ Protonation of carbene-stabilized diphosphorus: complexation of HP2+ Yuzhong Wang, Hunter P. Hickox, Yaoming Xie, Pingrong Wei, Dongtao Cui, Melody R. Walter, Henry F. Schaefer III and Gregory H. Robinson Chem. Commun., 2016, doi:10.1039/C6CC01759B