Arsenat
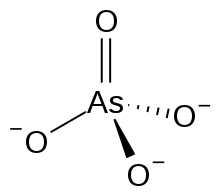
Arsenat[1][2] je anion čija je formula AsO43-. Arsenati su soli koje sadrže ovaj anion. U kiseloj sredini arsenat daje arsenatnu kiselinu H3AsO4.
Arsenat lako reaguje sa metalima i formira metalna jedinjenja arsenata.[3][4] Arsenat je umjereni oksidator i akceptor elektrona, sa elektrodnim potencijalom od +0,56 V za njegovu redukciju u arsenit.[5] Zbog arsena koji ima istu valenciju i sličan atomski radijus kao fosfor, arsenat dijeli sličnu geometriju i reaktivnost sa fosfatom.[6] Arsenat može zamijeniti fosfat u biohemijskim reakcijama i toksičan je za većinu organizama.[6][7]
Ioni
uredi- u jako kiselim uslovima, egzistira kao arsenatna kiselina: H3AsO4;
- u slabo kiselim uslovima, postoji kao ion dihidrogen arsenat, H2AsO4−;
- u slabo bazičnim uslovima postoji kao ion hidrogen arsenat HAsO42−;
- i, najzad, u jako bazičnim uslovima, postoji kao arsenatni ion AsO43−.
Reference
uredi- ^ PubChem. "Arsenate ion". pubchem.ncbi.nlm.nih.gov (jezik: engleski). Pristupljeno 16. 4. 2024.
- ^ "Arsenate mineral | Structure, Occurrence, Chemistry | Britannica". www.britannica.com (jezik: engleski). Pristupljeno 16. 4. 2024.
- ^ "Arsenate mineral | Britannica". www.britannica.com (jezik: engleski). Pristupljeno 2. 4. 2023.
- ^ Waalkes, Michael P. (2019), Straif (ured.), "Arsenic and metals", Tumour Site Concordance and Mechanisms of Carcinogenesis, IARC Scientific Publications, Lyon (FR): International Agency for Research on Cancer, ISBN 978-92-832-2217-0, pristupljeno 2. 4. 2023 Missing
|editor1=(pomoć) - ^ "P1: Standard Reduction Potentials by Element". Chemistry LibreTexts (jezik: engleski). 2. 12. 2013. Pristupljeno 29. 3. 2023.
- ^ a b Pollutants, National Research Council (US) Committee on Medical and Biological Effects of Environmental (1977). Chemistry of Arsenic (jezik: engleski). National Academies Press (US).
- ^ Elias, Mikael; Wellner, Alon; Goldin-Azulay, Korina; Chabriere, Eric; Vorholt, Julia A.; Erb, Tobias J.; Tawfik, Dan S. (2012). "The molecular basis of phosphate discrimination in arsenate-rich environments". Nature (jezik: engleski). 491 (7422): 134–137. Bibcode:2012Natur.491..134E. doi:10.1038/nature11517. ISSN 1476-4687. PMID 23034649.