ATP-hidroliza
ATP-hidroliza ili hidroliza ATP je proces kataboličke reakcije kojoj se hemijska energija koja je pohranjena u visokoenergetske fosfoanhidridne veze u adenozin-trifosfatu (ATP) oslobađa nakon cijepanja ovih veza, naprimjer u mišićima, proizvodeći rad u obliku memehaničke energije. Proizvod je adenozin-difosfat (ADP) i anorganski fosfat (Pi). ADP se može dalje hidrolizirati da bi se dobila energija, adenozin-monofosfat (AMP) i drugi neorganski fosfat (Pi).[1] Hidroliza ATP-a je konačna veza između energije dobijene iz hrane ili sunčeve svjetlosti i korisnog rada kao što je kontrakcija mišića, uspostavljanje elektrohemijskog gradijenta preko membrana i biosintetskih procesa neophodnih za održavanje života.
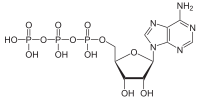
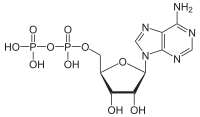

Opis i tipskii udžbenik označavaju anhidridne veze kao ""visokoenergetske veze"". P-O veze su u stvari prilično jake (~30 kJ/mol jače od C-N veza)[2][3] a njih nije posebno lahko slomiti. Kao što je navedeno u nastavku, energija se oslobađa hidrolizom ATP-a. Međutim, kada su P-O veze prekinute, potreban je "unos" energije. Formiranje novih veza i nižeenergetskog anorganskog fosfata uz oslobađanje veće količine energije smanjuje ukupnu energiju sistema i čini ga stabilnijim.[1]
Hidroliza fosfatnih grupa u ATP-u je posebno egzhotermna, jer je rezultirajući neorganski molekulski ion fosfata u velikoj mjeri stabiliziran višestrukim rezonantnim strukturama, stvarajući proizvode (ADP i P< sub>i) manje energije od reaktanta (ATP). Visoka gustoća negativnog naboja povezana sa tri susjedne fosfatne jedinice ATP-a također destabilizira molekulu, čineći je višeenergetskom. Hidroliza ublažava neke od ovih elektrostatskih odbijanja, oslobađajući korisnu energiju u procesu izazivajući konformacijske promjene u strukturi enzima.
Kod ljudi, otprilike 60 % energije oslobođene hidrolizom ATP-a proizvodi metaboličku toplinu, a ne pokreće stvarne reakcije koje se odvijaju.[4] Zbog kiselo-baznih svojstava ATP-a, ADP-a i neorganskog fosfata, hidroliza ATP-a ima učinak na snižavanje pH reakcijskog medija. Pod određenim uslovima, visoki nivoi hidrolize ATP-a mogu doprineti laktoacidozi.
Količina proizvedene energije uredi
Hidroliza terminalne fosfoanhidridne veze je visoko egzoterman proces. Količina oslobođene energije zavisi od uslova u određenoj ćeliji. Konkretno, energija koja se oslobađa ovisi o koncentracijama ATP-a, ADP-a i Pi. Kako koncentracije ovih molekula odstupaju od vrijednosti u ravnoteži, vrijednost Gibbsove slobodne energije promjene (ΔG) će biti sve drugačija. U standardnim uslovima (koncentracije ATP, ADP i Pi su jednake 1M, koncentracija vode je jednaka 55 M) vrijednost ΔG je između -28 do -34 kJ/mol .[5][6]
Raspon vrijednosti ΔG postoji jer ova reakcija ovisi o koncentraciji kationa Mg2+, koji stabiliziraju molekulu ATP-a. Ćelijsko okruženje također doprinosi razlikama u vrednosti ΔG jer hidroliza ATP-a zavisi ne samo od proučavane ćelije, već i od okolnog tkiva, pa čak i od odjeljka unutar ćelije. Varijabilnost vrijednosti ΔG je stoga za očekivati.[6]
Odnos između standardne Gibbsove promjene otkriva slobodne energije ΔrGo i hemijske ravnoteže. Ovaj odnos je definisan jednadžbom ΔrGo = –RT ln(K), gdje je K ' je konstanta ravnoteže, koja je jednaka reakcijskom kvocijentu Q u ravnoteži. Standardna vrijednost ΔG za ovu reakciju je, kao što je spomenuto, između –28 i -đ–34 kJ/mol; međutim, eksperimentalno određene koncentracije uključenih molekula otkrivaju da reakcija nije u ravnoteži.[6] S obzirom na ovu činjenicu, poređenje između konstante ravnoteže, K, i reakcijskog kvocijenta, Q, pruža uvid. K uzima u obzir reakcije koje se odvijaju u standardnim uslovima, ali u ćelijskom okruženju koncentracije uključenih molekula (ATP, ADP i Pi) su daleko od standardnih 1 M. Zapravo, koncentracije se prikladnije mjere u mM, što je manje od M za tri reda veličine.[6] Koristeći ove nestandardne koncentracije, izračunata vrijednost Q je mnogo manje od jednog. Povezujući Q sa ΔG, koristeći jednadžbu ΔG = ΔrGo + RT ln(Q), gdje je ΔrGo standardna promjena Gibbsove slobodne energije za hidrolizu ATP-a, to je utvrdili da je veličina ΔG mnogo veća od standardne vrijednosti. Nestandardni uslovi ćelije zapravo rezultiraju povoljnijom reakcijom.[7]
U jednoj posebnoj studiji, da bi se odredio ΔG in vivo kod ljudi, izmjerena je koncentracija ATP-a, ADP-a i Pi pomoću nuklearne magnetne rezonance.[6] U ljudskim mišićnim ćelijama u mirovanju, koncentracija ATP-a je bila oko 4 mM, a koncentracija ADP-a bila je oko 9 μM. Unos ovih vrijednosti u gornje jednačine daje ΔG = –64 kJ/mol. Nakon ishemije, kada se mišić oporavlja od vježbanja, koncentracija ATP-a je samo 1 mM, a koncentracija ADP-a je oko 7 μM. Stoga bi apsolutni ΔG bio čak –69 kJ/mol.[8]
Upoređujući standardnu vrijednost ΔG i eksperimentalnu vrijednost ΔG, može se vidjeti da je energija oslobođena hidrolizom ATP-a, mjerena kod ljudi, skoro dvostruko veća od energije proizvedeno pod standardnim uslovima.[6][7]
Također pogledajte uredi
Reference uredi
- ^ a b Lodish, Harvey (2013). Molecular cell biology (7th izd.). New York: W.H. Freeman and Co. str. 52, 53. ISBN 9781464109812. OCLC 171110915.
- ^ Darwent, B. deB. (1970). "Bond Dissociation Energies in Simple Molecules", Nat. Stand. Ref. Data Ser., Nat. Bur. Stand. (U.S.) 31, 52 pages.
- ^ "Common Bond Energies (D". www.wiredchemist.com. Pristupljeno 4. 4. 2020.
- ^ Berne & Levy physiology. Berne, Robert M., 1918-2001., Koeppen, Bruce M., Stanton, Bruce A. (6th, updated izd.). Philadelphia, PA: Mosby/Elsevier. 2010. ISBN 9780323073622. OCLC 435728438.CS1 održavanje: others (link)
- ^ "Standard Gibbs free energy of ATP hydrolysis - Generic - BNID 101989". bionumbers.hms.harvard.edu. Pristupljeno 25. 1. 2018.
- ^ a b c d e f Philips, Ron Milo & Ron. "» How much energy is released in ATP hydrolysis?". book.bionumbers.org (jezik: engleski). Pristupljeno 25. 1. 2018.
- ^ a b "ATP: Adenosine Triphosphate". cnx.org. Pristupljeno 16. 5. 2018.
- ^ Wackerhage, H.; Hoffmann, U.; Essfeld, D.; Leyk, D.; Mueller, K.; Zange, J. (decembar 1998). "Recovery of free ADP, Pi, and free energy of ATP hydrolysis in human skeletal muscle". Journal of Applied Physiology. 85 (6): 2140–2145. doi:10.1152/jappl.1998.85.6.2140. ISSN 8750-7587. PMID 9843537. S2CID 2265397.
Dopunska literatura uredi
- Syberg, F.; Suveyzdis, Y.; Kotting, C.; Gerwert, K.; Hofmann, E. (2012). "Time-Resolved Fourier Transform Infrared Spectroscopy of the Nucleotide-binding Domain from the ATP-binding Cassette Transporter MsbA: ATP Hydrolysis ID The Rate-Limiting Step in the Catalytic Cycle". Journal of Biological Chemistry. 278 (28): 23923–23931. doi:10.1074/jbc.M112.359208. PMC 3390668. PMID 22593573.
- Zharova, T. V.; Vinogradov, A. D. (2003). "Proton-Translocating ATP-synthase of Paracoccus denitrificans: ATP- Hydrolytic Activity". Biochemistry. Moscow. 68 (10): 1101–1108. doi:10.1023/A:1026306611821. PMID 14616081. S2CID 19570212.
- Kamerlin, S. C.; Warshel, A. (2009). "On the energetics of ATP hydrolysis in solution". Journal of Physical Chemistry. B. 113 (47): 15692–15698. doi:10.1021/jp907223t. PMID 19888735.
- Bergman, C.; Kashiwaya, Y.; Veech, R. L. (2010). "The effect of pH and Free Mg2+ on ATP Linked Enzymes and the Calculation of Gibbs Free Energy of ATP Hydrolysis". Journal of Physical Chemistry. B. 114 (49): 16137–16146. doi:10.1021/jp105723r. PMID 20866109.
- Berg, J. M.; Tymoczko, J. L.; Stryer, L. (2011). Biochemistry (International izd.). New York: W. H. Freeman. str. 287.